Статья опубликована в рамках: II Международной научно-практической конференции «Научное сообщество студентов: МЕЖДИСЦИПЛИНАРНЫЕ ИССЛЕДОВАНИЯ» (Россия, г. Новосибирск, 16 апреля 2012 г.)
Наука: Биология
Секция: Экология и природопользование
Скачать книгу(-и): Часть I, Часть II, Часть III, Часть IV, Часть V
дипломов
СРАВНИТЕЛЬНЫЙ ЭКОАНАЛИЗ КАК ИНСТРУМЕНТ ИЗМЕРЕНИЯ ГИДРОХИМИЧЕСКИХ ПОКАЗАТЕЛЕЙ ВОДНЫХ ОБЪЕКТОВ
Трофимова Анна Владимировна
студентка 2 курса, кафедры Безопасности жизнедеятельности,
экологии и физического воспитания ЮТИ НИ ТПУ, г.Юрга,
E-mail:torosjaneno@mail.ru
Торосян Вера Федоровна
научный руководитель к.пед.н., доцент ЮТИ НИ ТПУ, г.Юрга
Вся духовная жизнь человека нераздельно связана с природой. Острота современных проблем взаимодействия общества и природы поставила ряд новых задач перед образованием и педагогикой, которые призваны готовить учащихся, не только преодолеть последствия негативных воздействий человека на природу и оптимизировать это воздействие, а и прививать другим бережное и уважительное отношение к природе. При этом экологическая культура, которая включает в себя совокупность знаний и умений, взглядов и убеждений, мотивов и действий, связанных с необходимостью разумного, рационального природопользования, с поиском путей сбережения и улучшения окружающей природной среды, является качественным показателем практического отношения учащихся к природе.
Вода является своеобразным материалом, обладающим чрезвычайно ценными свойствами, обеспечивающими существование живых организмов на Земле и развитие процессов их жизнедеятельности. Велика роль воды в историческом процессе геологического преобразования нашей планеты. И, конечно же, без воды деятельность человеческого общества немыслима. Реки выполняют важнейшую работу по очистке от загрязнений территорий городов — растворению и выносу за их пределы всего, что растворяется или может быть перемещено во взвешенном состоянии.
Великий Гиппократ когда-то сказал: «Человек рождается здоровым. Болезни в него входят с тем, что он ест и пьет» И с этим, в какой-то степени, трудно не согласиться, потому что жители любого города наверняка озабочены вопросом: насколько безопасна вода, вытекающая из кранов?
В воде многих рек обнаружены такие химические вещества, как летучие хлорорганические соединения, соединения мышьяка, кадмия, никеля, хрома, которые определяют канцерогенный риск, риск заболеваний системы крови, кроветворных органов. И хотя содержание каждого из них не превышает ПДК, коэффициент суммации по санитарно-токсикологическим показателям превышает предельно-допустимый в 1,5-3 раза.
Городские станции контроля осуществляют проверку качества воды поверхностных источников водоснабжения. Сравнительный анализ значений качественных характеристик воды, например, посезонно за 10 лет весьма большой (для нас людей, но не для реки) период может характеризовать потенциал реки к самоочищению.
В соответствии с геохимическими представлениями тип воды определяется содержанием катионных и анионных элементов. А основным инструментом определения состояния и свойств воды является ее качественный и количественный анализ.
По результатам химического анализа воды реки (архив СЭС), можно проанализировать сезонный ход гидрохимических параметров воды реки, таких как pH,содержание азота и фосфора, БПК, ХПК.
pHводы – показатель среды, его величина имеет большое значение для химических и биохимических процессов. От него зависит развитие и жизнедеятельность водных растений, устойчивость форм миграции элементов, агрессивное действие воды на металлы и бетон. Содержание ионов водорода определяется соотношением концентрации угольной кислоты и ее ионов. При большом количестве растворенного СО2 воды имеют кислую реакцию рН<6,5. Величина рН для речных вод обычно в пределах 6,5- 8,5
Кислород – один из важнейших растворимых в воде газов. Главным источником получения кислорода являются процессы адсорбции его из атмосферы и продуцирования в результате фотосинтетической деятельности водных организмов.
Потребление кислорода в воде связано с химическими и биохимическими процессами окисления органических веществ. Содержание кислорода в поверхностных водах от 0 до 14 мг/л.
БПК (мгО2/л) – биологическое потребление кислорода – это его количество, затраченное на окисление органических веществ (ОВ), которые в свою очередь являются прижизненными выделениями обитающих в воде организмов, их посмертными остатками, а также водорастворимым гумусом почвенного и планктонного происхождения. Кроме этого ОВ попадают в реку со сточными водами. БПК определяют в пробе воды через 5 суток после ее отбора.
Известно, что БПК ≈ 1,1÷1,9 - вода чистая
2÷2,9 - умеренно загрязненная
3÷3,9 - вода загрязненная
Более 4- очень грязная
ХПК – химическое потребление кислорода или бихроматная окисляемость — это то количество кислорода, которое расходуется для окисления всех ОВ, содержащихся в загрязненной воде, даже тех которые микроорганизмы окислять не могут. Единица измерения мгО2/л.
Важным гидрохимическим показателем воды является комплекс азот и фосфор – это биогенные элементы. Они определяют продуктивность водных объемов. Для воды содержание азота определяется в виде:
Молекулярного N2
Нитрат иона NO3
Нитрит иона NO2
Аммонийный азот NH4
Органические соединения азота (мочевина, пептиды, аминокислоты и т.д.)
Азот поступает в воду в основном в процессе лизиса и автолизиса клеток отмерших организмов, главным образом фитопланктона. Азот содержащие соединения выделяют при жизни водоросли, зоопланктоны и другие гидробионты. А также азот поступает в поверхностные воды с атмосферными осадками, стоками сельскохозяйственными и бытовыми. Понижение содержания азотсодержащих соединений связано с их потреблением фитопланктоном, бактериями и процессами денитрификации
Известно, что для оценки загрязнения крупных водных объектов широко используют такой интегральный показатель, как индекс загрязненности воды (обычно ИЗВ считают по 6 элементам).
В расчетах данного проекта используются не 6, а 13 показателей, для более комплексной оценки качества воды, причем подбор ингредиентов учитывает специфику промышленных объектов города.
Перечень ингредиентов:
|
1. Нефтепродукты |
ПДК= 0,05 мг/л |
|
2. Железо общее |
ПДК= 0,1 мг/л |
|
3. Цинк,Zn+2 |
ПДК=1,0 мг/л |
|
4. Хром,Cr+6 |
ПДК=0,05 мг/л |
|
5. Медь,Cu+2 |
ПДК=1,0 мг/л |
|
6. БПК |
ПДК = 3 мг/л |
|
7. Свинец |
ПДК= 0,01 мг/л |
|
8. Марганец |
ПДК= 0,1 мг/л |
|
9. ХПК |
ПДК=15 мг/л |
|
10. Аммиак |
ПДК=1,5 мг/л |
|
11. Нитриты |
ПДК=0,08 мг/л |
|
12. Формальдегид |
ПДК=0,05 мг/л |
|
13. Фосфаты |
ПДК=0,05 мг/л |
Создание базы данных по промышленным объектам города, и их ранжирование по степени воздействия на окружающую среду позволяет выявить факторы техногенного воздействия на реку. В качестве одного из них можно рассматривать, например, шлаковый отвал металлургического производства, а следовательно, необходимо экспериментально определить кинетическое взаимодействие между содержанием ионов металлов в шлакоотвале и их поступлением в воду реки.
Металлургические шлаки — это основная масса отходов металлургических процессов. Они являются продуктами высокотемпературного взаимодействия компонентов исходных материалов. Химический состав и структура металлургических шлаков изменяются в зависимости от состава пустой породы, особенностей металлургического производства, условий охлаждения и др. Шлаковый режим, определяемый количеством и составом шлака, оказывает влияние на качество стали, стойкость футеровки и производительность сталеплавильного агрегата. В процессе выплавки стали шлак выполняет несколько важных функций: связывает все оксиды, образующиеся в процессе окисления примесей; служит передатчиком кислорода из печной атмосферы к жидкому металлу; участвует в передаче тепла металлу; защищает металл от насыщения газами, содержащимися в атмосфере печи.
Наибольшее негативное воздействие шлаковые отвалы оказывают на водные объекты – подземные и поверхностные воды. С поверхностным стоком загрязняющие вещества поступают в поверхностные воды реки, изменяя их химический состав, увеличивая концентрацию сульфат- иона, железа общего, марганца и др.. Атмосферные осадки инфильтруются через тело отвала, насыщаются водорастворимыми компонентами и загрязняют грунтовые воды. Влияние отвала на атмосферу и грунт зависит от зернового состава складированных отходов и измельчения при длительном хранении. Пылевидные шлаковые частицы разносятся ветром на прилегающие территории, накапливаются в верхнем слое почвы. Анализы снега на территории промышленной зоны завода могут показать содержание Mn2+ и Fe3+ Вопросы влияния шлаковых отвалов металлургических предприятий на объекты гидросферы, эмиссия загрязняющих веществ из шлаков в водные объекты в настоящее время изучены недостаточно, отсутствует системный подход к данной проблеме, позволяющий оценить их реальную экологическую опасность.
Далее в статье мы приводим результаты экспериментальных исследований, выполненных учащимися в рамках НИР, проводимой совместно со студентами технического ВУЗа
Химический состав шлака является важной характеристикой для оценки его гидравлической активности. Поэтому необходимо провести серию исследовательских экспериментов по выявлению эмиссии ионов тяжелых металлов (ТМ) Mn2+ и Fe3+ в модельные водные среды. Модельные водные среды – это 300мл H2Oдистиллированной и 150 г шлака. В результате исследования эмиссии ионов Fe3+и Mn2+ в модельном растворе с pH=4,8 можно выявить их кинетическую зависимость.
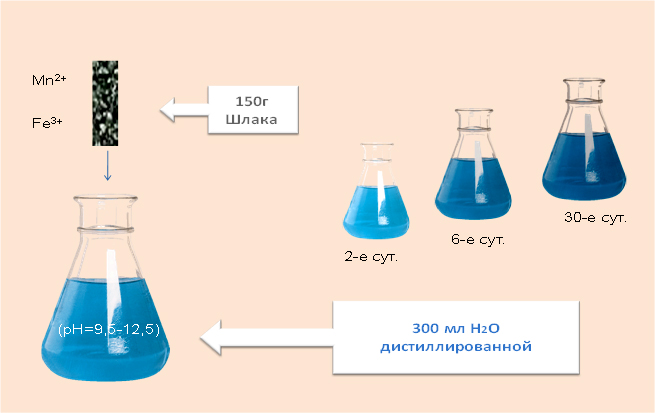
Рис1. Модельный водный раствор
Эксперимент должен выполнятся в статическом режиме в течение 30 суток. Анализ содержания Mn2+ и Fe3+ выполняется на 2 -е, 4-е, 6-е, 9-е и 30 сутки. Водная вытяжка из тела отвала шлака характеризуется щелочной реакцией среды (рН=9,5-12,5), высокой общей минерализацией. Анализ количества эмиссионных ионов Mn2+ и Fe3+в растворе определяется методом фотоколориметрии
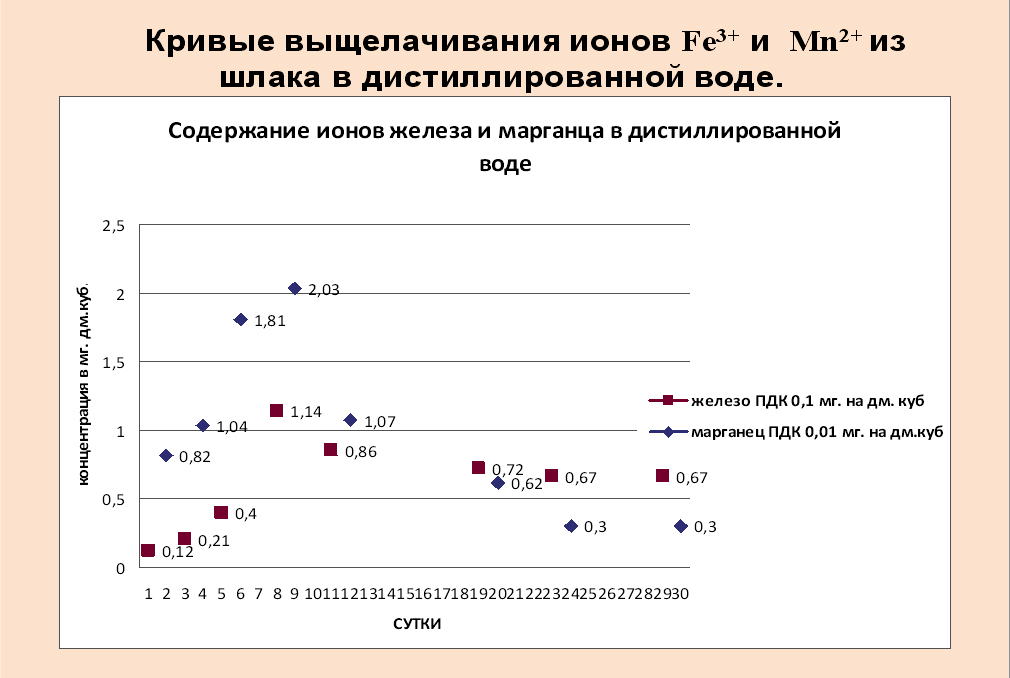
Рис.2 Выщелачивание ионовFe3+ и Mn2+ в дистиллированной воде
Результаты исследования эмиссий ТМ в дистиллированную воду можно представить графически как, например, на рис 2.
В результате экспериментов, установлено, что кривые выщелачивания ТМ имеют ярко выраженный экстремальный характер, что можно объяснить следующим образом. В первые 2- суток наряду с ионами ТМ происходит выделение из образцов ионов Ca2+, Mg2+, сульфидов, приводящее к повышению pHсреды и образованию в дальнейшем труднорастворимых гидроксидов Ca(OH)2 , Mn(OH)2 , Fe(OH)2 , Mg(OH)2 и сульфидов MnS, CaS, CrOHSи др. ТМ. А в результате происходит связывание ионов Fe3+и Mn2+ и образование нерастворимых соединений. О чем говорит понижение содержания ионов Fe3+ и Mn2+ в растворе одновременно на 9 сутки.
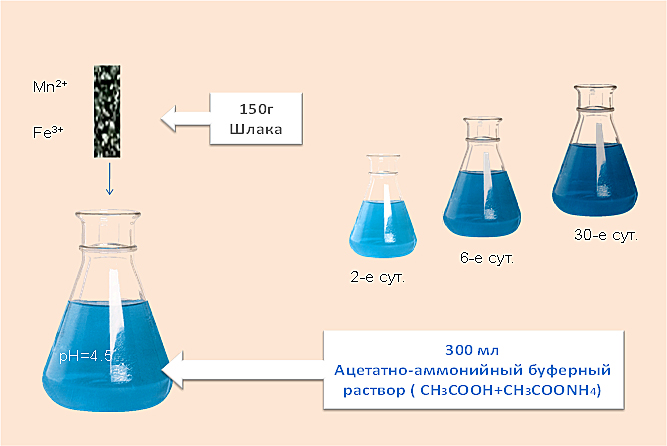
Рис 3. Модельныйацетатно-аммонийного буферный раствор CH3COOH+CH3COONH4
Мы проводили также исследования эмиссии ионов Fe+3 и Mn2+ в растворе ацетатно-аммонийного буферного раствора CH3COOH+CH3COONH4(уксусная кислота и ацетат аммония) pH=4,8, который имитировал агрессивную среду. Результаты приведены в табл1.
Таблица 1
Эмиссия ионов Fe+3 и Mn2+ в ацетатно-аммонийном буферном растворе CH3COOH+CH3COONH4
|
Сутки |
Концентрация мг/дм3 |
||
|
Fe3+ |
Mn2+ |
||
|
2 |
0,07 |
0,06 |
|
|
4 |
0,12 |
0,15 |
|
|
6 |
0,18 |
0,20 |
|
|
9 |
0,29 |
0,28 |
|
|
10 |
0,30 |
0,47 |
|
|
12 |
0,30 |
0,82 |
|
|
15 |
0,30 |
0,82 |
|
|
24 |
0,30 |
0,82 |
|
|
30 |
0,30 |
0,82 |
|
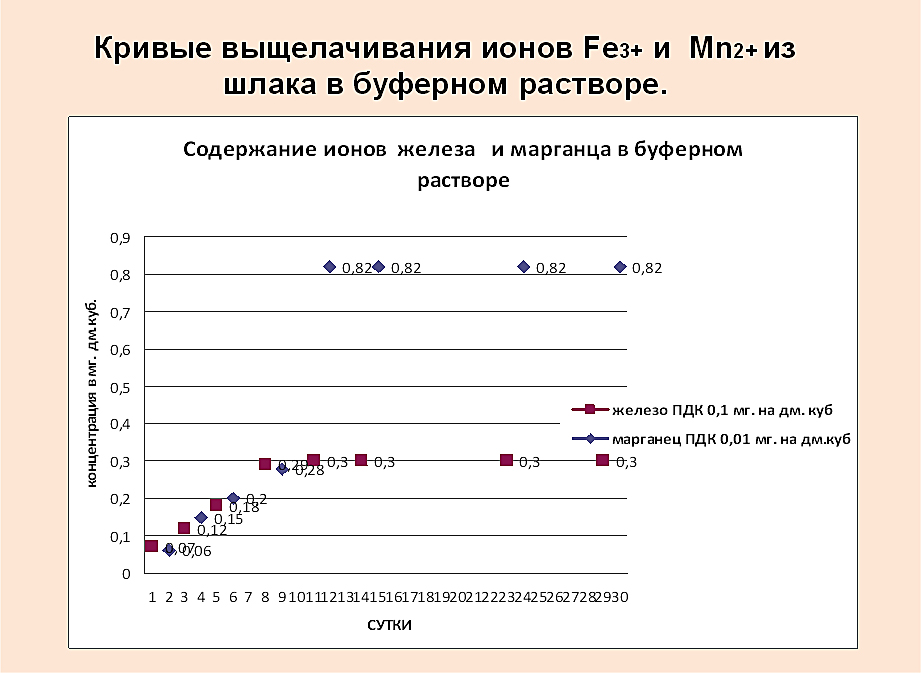
Рис.4. Выщелачивание ионовFe3+ и Mn2+ в ацетатно-аммонийном буферном растворе CH3COOH+CH3COONH4
Результаты анализа эксперимента показали, что эмиссия ионов Fe3+ в течение 10 суток возрастала , а Mn2+ в течение первых 12 суток возрастала, а затем оставалась постоянной. Т.к. в кислой среде, очевидно, не образовывались малорастворимые соединения. Fe3+ и Mn2+
Рассчитывая значения константы скорости реакции эмиссии исследуемых металлов в буферный раствор по формуле 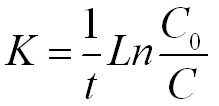 , подставляя в нее данные эксперимента, мы убедились, что полученные значения константы скорости мало отличаются друг от друга. Мы вычислили среднее значение константы скорости реакции. В результате можно утверждать, что исследуемые реакции эмиссии ТМ в буферном растворе подчиняются кинетической зависимости первого порядка табл.2.
, подставляя в нее данные эксперимента, мы убедились, что полученные значения константы скорости мало отличаются друг от друга. Мы вычислили среднее значение константы скорости реакции. В результате можно утверждать, что исследуемые реакции эмиссии ТМ в буферном растворе подчиняются кинетической зависимости первого порядка табл.2.
Таблица 2.
Кинетические зависимости эмиссий тяжелых металлов из шлака в агрессивной среде( pH=4,8).
|
Показатель |
|
Время, сутки |
||||||||
|
|
2 |
4 |
6 |
9 |
10 |
12 |
15 |
24 |
30 |
|
|
|
|
Железо,Fe3+ |
||||||||
|
Концентрация, мг/дм3 |
0,07 |
0,12 |
0,18 |
0,29 |
0,30 |
0,30 |
0,30 |
0,30 |
0,30 |
|
|
Ln C |
-2,66 |
-2,12 |
-1,72 |
-1,24 |
-1,2 |
-1,2 |
-1,2 |
-1,2 |
-1,2 |
|
|
Кинетическое уравнение |
|
LnC= -2,66+0,14t |
||||||||
|
Показатель |
|
Время, сутки |
||||||||
|
|
2 |
4 |
6 |
9 |
10 |
12 |
15 |
24 |
30 |
|
|
|
|
Марганец, Mn2+ |
||||||||
|
Концентрация, мг/дм3 |
0,06 |
0,15 |
0,20 |
0,28 |
0,47 |
0,82 |
0,82 |
0,82 |
0,82 |
|
|
Ln C |
-2,81 |
-1,9 |
-1,61 |
-1,27 |
-0,76 |
-0,20 |
-0,20 |
-0,20 |
-0,20 |
|
|
Кинетическое уравнение |
|
LnC= -2,81+0,2t |
||||||||
При этом было выявлено, что эмиссия ионов Fe3+и Mn2+в модельном растворе с pH=4,8 подчиняется кинетической зависимости первого порядка, скорость эмиссии Mn2+выше скорости эмиссии Fe3+.
Моделирование процесса эмиссии ионов Fe3+и Mn2+в различные водные среды позволяет выявлять кинетические зависимости, необходимые для экологической оценки и прогноза воздействия металлургических шлакоотвалов на объекты гидросферы.
Список литературы:
- Г.М. Рогов, О.Д. Лукашевич, В.К. Попов, Водно-экономические проблемы г. Томска в контексте экологической безопасности. Безопасность жизнедеятельности. —2008. —№ 1 —с.25—29.
-
Фюлленберг Г. Загрязнение природной среды. Введение в экологическую химию / Г. Фюлленберг; Пер. с нем. А. В. Очкина; Под ред. К. Б. Заборенко. — М.: Мир, 1997. — 232 с.
дипломов

