Статья опубликована в рамках: XIII Международной научно-практической конференции «Естественные и математические науки в современном мире» (Россия, г. Новосибирск, 09 декабря 2013 г.)
Наука: Математика
Секция: Дифференциальные уравнения, динамические системы и оптимальное управление
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
МАТЕМАТИЧЕСКАЯ МОДЕЛЬ СОЛИДНОЙ ОПУХОЛИ
Жукова Ирина Валерьевна
аспирант Санкт-Петербургского государственного университета, РФ, г. Санкт-Петербург
E-mail: zhira428@mail.ru
Колпак Евгений Петрович
д-р физ.-мат. наук, профессор Санкт-Петербургского государственного университета, РФ, Санкт-Петербург
E-mail:
MATHEMATICAL MODEL OF SOLID TUMOUR
Irina Zhukova
post-graduate student of St. Petersburg State University, Russia St. Petersburg
Eugeniy Kolnak
doctor of Physics and Mathematics, professor of St. Petersburg State University, Russia St. Petersburg
АННОТАЦИЯ
Разработана математическая модель злокачественной опухоли, представляющая собой задачу Коши для системы обыкновенных дифференциальных уравнений. Проанализирована устойчивость стационарных решений, построены численные решения. Дана оценка влияния химиотерапии на рост опухоли.
ABSTRACT
Mathematical model of cancer tumour which represents a Cauchy problem for system of ordinary differential equations was developed. Stability of stationary solutions was analyzed, numerical solutions were built. Evaluation of chemotherapy’s influence on tumor growth was given.
Ключевые слова: математическое моделирование; дифференциальные уравнения.
Keywords: mathematical modeling; differential equations.
Новообразования продолжают оставаться одним из менее изученных заболеваний всех млекопитающих, включая человека, и являются одной из основных причин их ранней смертности. В России около 15 % всех смертей среди населения приходится на долю онкологических заболеваний. По мнению специалистов, злокачественные новообразования продолжают оставаться практически неизлечимыми [6, с. 8—11]. Одним из подходов в поиске эффективного пути лечения является математическое моделирование.
Первые математические модели злокачественной опухоли представляли собой задачу Коши для системы обыкновенных дифференциальных уравнений. В моделях учитывались опухолевые, здоровые и погибшие клетки, питание, различные ингибирующие вещества, ответ иммунной системы [15—17]. Затем были предложены модели типа диффузия-адвекция-реакция, в которых опухоль рассматривалась как система с распределенными параметрами [2, 3, 12—14, 18—20].
Клетки здорового организма смертны, «запрограммированная» смерть (апоптоз) является окончанием жизненного цикл. В свою очередь, основной особенностью клеток злокачественной опухоли является отсутствие апоптоза [1, 6, 15, 17]. Поскольку опухолевые клетки не отличаются от здоровых, то иммунная система с трудом их распознает [15]. С ростом опухоли ее клетки группируются, образуя различные пространственные структуры (сфероиды, трубки, нити, диски и т. п.) [6, 15]. Внутренние клетки образовавшейся структуры начинают гибнуть в силу недостаточного питания, внешние опухолевые клетки продолжают размножаться, оттесняя от себя здоровые клетки. В процессе роста опухоли, как делящиеся клетки, так и все погибшие из организма не выносятся, образуя «солидную» опухоль [6, 8, 9, 17]. Т. е., злокачественная опухоль представляет собой независимое образование из ядра погибших клеток, окруженного слоем непрерывно делящихся клеток опухоли. В силу своей автономности к окружающим тканям, опухолевые клетки проникают в окружающие ткани, разрушая их и создавая новые точки роста.
В рассматриваемой модели опухоли учитывается три типа клеток: непрерывно делящиеся (опухолевые), нормальные (здоровые) и погибшие [14]. Предполагается, что апоптоз у делящихся клеток отсутствует. Нормальные клетки в отсутствие делящихся размножаются по логистическому закону [7]. В процессе роста делящиеся клетки выделяют токсичные вещества, оказывающие ингибирующее влияние на нормальные клетки [6, 8, 9, 17]. Погибшие клетки оказывают ингибирующее влияние на нормальные и делящиеся. Ткань опухоли считается мало сжимаемой. Поэтому равновесные концентрация нормальных клеток в отсутствие делящихся и погибших и концентрация погибших в отсутствие делящихся и нормальных должны быть одинаковыми и ниже принимаются равными единице.
В качестве одного из методов лечения опухолей является химиотерапия [6, 8, 9, 17]. В рассматриваемой модели злокачественного образования на нормальные клетки ингибирующее влияние оказывают как делящиеся клетки, так и погибшие. Поэтому в модели учитывается «химиотерапия» постоянного воздействия только на делящиеся и погибшие клетки.
Пусть ![]() — количество делящихся клеток,
— количество делящихся клеток, ![]() — нормальных клеток,
— нормальных клеток, ![]() — погибших. С учетом введенных обозначений система дифференциальных уравнений, описывающая рост «солидной» опухоли, имеет следующий вид:
— погибших. С учетом введенных обозначений система дифференциальных уравнений, описывающая рост «солидной» опухоли, имеет следующий вид:
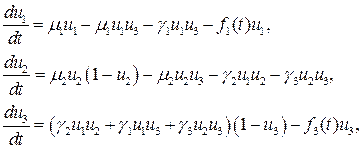 (1)
(1)
В первом уравнении слагаемое ![]() — скорость «собственного» роста делящихся клеток, слагаемое
— скорость «собственного» роста делящихся клеток, слагаемое ![]() — скорость ингибирования погибшими клетками делящихся, слагаемое
— скорость ингибирования погибшими клетками делящихся, слагаемое ![]() —скорость вытеснения делящихся клеток погибшими. Слагаемое
—скорость вытеснения делящихся клеток погибшими. Слагаемое ![]() во втором уравнении — скорость изменения численности нормальных клеток,
во втором уравнении — скорость изменения численности нормальных клеток, ![]() — скорость ингибирования делящимися клетками здоровых,
— скорость ингибирования делящимися клетками здоровых, ![]() — скорость ингибирования нормальных клеток погибшими,
— скорость ингибирования нормальных клеток погибшими, ![]() — скорость вытеснения нормальных клеток погибшими. Скорость роста мертвых клеток (третье уравнение в (1)) пропорциональна
— скорость вытеснения нормальных клеток погибшими. Скорость роста мертвых клеток (третье уравнение в (1)) пропорциональна ![]() . Множитель
. Множитель ![]() отражает тот факт, что заполнение функционального пространства, занимаемого погибшими клетками, происходит тем медленнее, чем больше его наполнение.
отражает тот факт, что заполнение функционального пространства, занимаемого погибшими клетками, происходит тем медленнее, чем больше его наполнение. ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() — положительные константы, характеризующие скорости реакций. Неотрицательные функции
— положительные константы, характеризующие скорости реакций. Неотрицательные функции ![]() и
и ![]() описывают поступление химических препаратов, влияющих, соответственно, на скорость роста делящихся клеток и на скорость накопления погибших. При этом предполагается, что скорость гибели делящихся клеток пропорциональна их концентрации и концентрации химических препаратов. Это же предположение относится и к скорости распада погибших клеток при действии на них химиопрепаратов.
описывают поступление химических препаратов, влияющих, соответственно, на скорость роста делящихся клеток и на скорость накопления погибших. При этом предполагается, что скорость гибели делящихся клеток пропорциональна их концентрации и концентрации химических препаратов. Это же предположение относится и к скорости распада погибших клеток при действии на них химиопрепаратов.
В отсутствие делящихся и погибших клеток из уравнений (1) следует уравнение для роста нормальных клеток 5, 7]
![]()
В этой модели изменения численности нормальных клеток предполагается, что скорость их рождения равна ![]() , а гибель происходит со скоростью
, а гибель происходит со скоростью ![]() .
.
В качестве начальных условий будут рассматриваться условия при ![]() :
: ![]() ,
, ![]() ,
, ![]() , где
, где ![]() — малая величина. Эти начальные условия подразумевают, что в начальный момент времени в функциональном пространстве нормальных клеток (погибшие клетки отсутствуют) возникает небольшое количество делящихся клеток.
— малая величина. Эти начальные условия подразумевают, что в начальный момент времени в функциональном пространстве нормальных клеток (погибшие клетки отсутствуют) возникает небольшое количество делящихся клеток.
Система уравнений (1) при ![]() и
и ![]() имеет три стационарные точки
имеет три стационарные точки
1. ![]() ,
, ![]() ,
, ![]()
2. ![]() ,
, ![]() ,
, ![]()
3. ![]() ,
, ![]() ,
, ![]() — любое.
— любое.
Третья стационарная точка имеет физический смысл только в том случае, если ![]() . В первой стационарной точке матрица Якоби правой части уравнений (1) имеет собственное значение
. В первой стационарной точке матрица Якоби правой части уравнений (1) имеет собственное значение ![]() . То есть эта стационарная точка неустойчива в линейном приближении. В малой окрестности второй стационарной точки малые возмущения решения
. То есть эта стационарная точка неустойчива в линейном приближении. В малой окрестности второй стационарной точки малые возмущения решения ![]() ,
, ![]() и
и ![]() удовлетворяют системе уравнений
удовлетворяют системе уравнений
![]() ,
,
![]()
![]() .
.
Решение этих уравнений представляется в виде
![]() ,
, ![]() ,
,
![]()
Возмущения ![]() и
и ![]() должны быть положительными в силу физического смысла решения. Поскольку
должны быть положительными в силу физического смысла решения. Поскольку ![]() и
и ![]() убывающие по модулю функции, стремящиеся к
убывающие по модулю функции, стремящиеся к ![]() при
при ![]() , то
, то ![]() возрастающей функцией времени не будет и малым значением
возрастающей функцией времени не будет и малым значением ![]() будут соответствовать и малые значения
будут соответствовать и малые значения ![]() при достаточно больших значениях
при достаточно больших значениях ![]() . То есть это положение равновесия будет устойчивым. Таким образом, в рассматриваемой модели происходит постепенное вытеснение нормальных клеток погибшими.
. То есть это положение равновесия будет устойчивым. Таким образом, в рассматриваемой модели происходит постепенное вытеснение нормальных клеток погибшими.
Численное решение уравнений (1) осуществлялось в среде математического пакета MatLab [5] с использованием встроенных функций. На рис. 1 показано изменение функций ![]() ,
, ![]() и
и ![]() (численное решение уравнений (1)) во времени при
(численное решение уравнений (1)) во времени при ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() . Как следует из анализа численных результатов концентрация погибших клеток непрерывно растет, концентрация делящихся клеток сначала растет, а затем начинает убывать. Концентрация нормальных клеток монотонно уменьшается.
. Как следует из анализа численных результатов концентрация погибших клеток непрерывно растет, концентрация делящихся клеток сначала растет, а затем начинает убывать. Концентрация нормальных клеток монотонно уменьшается.
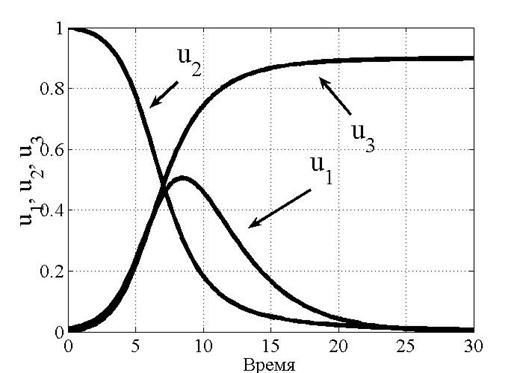
Рисунок 1. Динамика изменения функций ![]() ,
, ![]() ,
, ![]()
При наличии химиотерапии функции ![]() и
и ![]() задают «программу лечения». Для случая
задают «программу лечения». Для случая ![]() и
и ![]() стационарные точки системы уравнений (1) находятся как положительное решение системы алгебраических уравнений
стационарные точки системы уравнений (1) находятся как положительное решение системы алгебраических уравнений
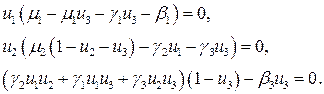
При ![]() первое уравнение будет удовлетворено только при
первое уравнение будет удовлетворено только при ![]() . В этом случае при
. В этом случае при ![]() третье уравнение будет удовлетворяться только при
третье уравнение будет удовлетворяться только при ![]() . Т.е., при этих условиях реализуется стационарная точка
. Т.е., при этих условиях реализуется стационарная точка ![]() ,
, ![]() ,
, ![]() . Собственные значения матрицы Якоби в этой стационарной точке
. Собственные значения матрицы Якоби в этой стационарной точке ![]() ,
, ![]() ,
, ![]() будут в этом случае отрицательными и, соответсвенно, стационарная точка будет устойчивой. Т. о., для уничтожение делящихся клеток необходимо, чтобы скорость их уничтожения была больше скорости их роста. При этом возможно и уничтожение погибших клеток, если скорость их уничтожения препаратами будет больше скорости их накопления.
будут в этом случае отрицательными и, соответсвенно, стационарная точка будет устойчивой. Т. о., для уничтожение делящихся клеток необходимо, чтобы скорость их уничтожения была больше скорости их роста. При этом возможно и уничтожение погибших клеток, если скорость их уничтожения препаратами будет больше скорости их накопления.
Список литературы:
1.Акоев И.Г. Биофизика познает рак. М.: Наука, 1988. — 160 с.
2.Астанин С.А., Лобанов А.И. Трехмерная модель роста неваскуляризированной опухоли в ткани // Математика. Компьютер. Образование. — 2005. — Ч. 1. — C. 759—769.
3.Астанин С.А., Колобов А.В., Лобанов А.И., Пименова Т.П., Полежаев А.А., Соляник Г.И. Влияние пространственной гетерогенности среды на рост и инвазию опухоли. Анализ методами математического моделирования // Медицина в зеркале информации. М.: Наука, 2008. — С. 188—223.
4.Балыкина Ю.Е., Колпак Е.П. Введение в Matlab. СПб: Соло. 2013. — 302 с.
5.Балыкина Ю.Е., Колпак Е.П. Математические модели функционирования фолликула щитовидной железы // Вест. С.-Петерб. ун-та. Сер. 10: Прикладная математика, информатика, процессы управления. — 2013. — Вып. 3. — С. 20—31.
6.Васильев Ю.М. Биология злокачественного роста. М.: Наука. 1965. — 180 с.
7.Горбунова Е.А., Колпак Е.П. Математические модели одиночной популяции // Вест. С.-Петерб. ун-та. Сер. 10: Прикладная математика, информатика, процессы управления. — 2012. — Вып. 4. — С. 18—30.
8.Долгих В.Т. Опухолевый рост: учеб. пособие/В.Т. Долгих. Ростов н/Д.: Феникс, 2007. — 160 с.
9.Жимулев И.Ф. Общая и молекулярная генетика. Новосибирск: Изд-во Новосиб. ун-та, 2002. — 459 с.
10.Колбин А.С., Курылев А.А., Павлыш А.В., Проскурин М.А., Балыкина Ю.Е. Научный анализ исходов в онкологии. Особенности фармакоэкономической экспертизы // Мед. техн. Оценка и выбор. — 2012. — Т. 2 (8). — С. 87—93.
11.Колбин А.С., Сидоренко С.В., Балыкина Ю.Е. Исследования в области новых антибактериальных средств — есть ли перспективы? // Педиатрическая фармакология. — 2010. — Т. 7. — № 5. — С. 12—16.
12.Колобов А.В., Губернов В.В., Полежаев А.А. Автоволны в модели роста инвазивной опухоли // Биофизика. — 2009. — Т. 54. — Вып. 2. — C. 334—342.
13.Колобов А.В., Полежаев А.А. Влияние случайной подвижности злокачественных клеток на устойчивость фронта опухоли // Компьютерные исследования и моделирование. — 2009. — T. 1 — № 2. — С. 225—232.
14.Колобов А.В., Анашкина А.А., Губернов В.В., Полежаев А.А. Математическая модель роста опухоли с учетом дихотомии миграции и пролиферации // Компьютерные исследования и моделирование. — 2009. — Т. 1. — № 4. — с. 415—422.
15.Моисеенко В.М., Блинов Н.Н., Хансон К.П. Биотерапия при злокачественных новообразованиях // Российский онкологический журнал. — 1997. — № 5. — C. 7—59.
16.Слепков В.А., Суховольский В.Г., Хлебопрос З.Г. Популяционная динамика в моделировании роста раковых опухолей // Биофизика. — 2007. — Т. 52. — Вып. 4. — С. 733—740.
17.Эммануэль Н.М. Кинетика экспериментальных опухолевых процессов. М.:Наука, 1977. — 419 с.
18.Byrne H.M., Breward C.J.W., Lewis C.E. The role of cell-cell interactions in a two-phase model for avascular tumour growth // Journal of Mathematical Biology. — 2001. — Vol. 45. — № 2. — P. 125—131.
19.Chaplain M.A.J., Sherratt J.A. A new mathematical model for avascular tumor growth // Journal of Mathematical Biology. — 2000. — Vol. 43. — № 4. — P. 291—312.
20.Mohammed Shuker Mahmood, Silvia Mahmood, Dusan Dobrota // Formulation and numerical simulations of a continuum model of avascular tumor growth // Mathematical Biosciences. — 2011. — Vol. 231. — № 2. — P. 159—171.

