Статья опубликована в рамках: V Международной научно-практической конференции «Научное сообщество студентов XXI столетия. ЕСТЕСТВЕННЫЕ НАУКИ» (Россия, г. Новосибирск, 25 октября 2012 г.)
Наука: Биология
Секция: Экология
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
отправлен участнику
ТЕХНОЛОГИЧЕСКИЕ АСПЕКТЫ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ПРОДУЦИРОВАНИЯ СЕРОВОДОРОДА ПРИРОДНЫМИ ШТАММАМИ ИЛОВЫХ БАКТЕРИЙ
Минниахметов Вадим Радикович
студент 4 курса, кафедра «Промышленной экологии и химии»,
КФ МГТУ им. Н.Э. Баумана г. Калуга
E-mail: lamppost100@gmail.com
Шемель Ирина Геннадиевна
научный руководитель, старший преподаватель КФ МГТУ им. Н.Э. Баумана г. Калуга
Восстановление микроорганизмами полностью или частично окисленных соединений минеральной серы в анаэробных условиях за счет окисления органического вещества или водорода называют микробной сульфатредукцией.
Геологическая роль сульфатредуцирующих бактерий, прежде всего, связана с образуемым ими конечным продуктом восстановления сульфата, химически высокореакционным сероводородом. В последнее время широко обсуждается вопрос использования процесса сульфатредукции в биоремедиационных технологиях [2].
Сульфатредуцирующие бактерии используют органические вещества (CH2O) или водород в качестве донора электрона и сульфат в качестве акцептора электрона при получении энергии [7]. Конечный продукт сульфатредукции, сероводород, реагирует с ионами металлов, осаждая их в виде практически нерастворимых сульфидов (в общем виде):
![]()
![]()
где Me2+ = Fe2+; Cu2+; Ni2+; Co2+; Cd2+; Zn2+; Pb2+
В результате деятельности сульфатвосстанавливающих бактерий из сточных вод осаждаются сульфиды кобальта, никеля, кадмия, железа, свинца, цинка и другие.
Редуцирующие сульфат бактерии являются облигатными анаэробами. Из литературы известно, что сульфатредукцию вызывают также и факультативные анаэробы. В результате их деятельности хорошо растворимые токсичные сульфаты восстанавливаются до практически нерастворимых, выпадающих в осадок форм. Именно они находят применение в очистке сточных вод.
Сульфатредукторы — одна из самых древних физиологических групп бактерий и они широко распространены по всему миру. Существует большое количество видов сульфатредуцирующих бактерий (СРБ). Некоторые из них показаны в таблице 1.
Таблица 1
Виды сульфатредуцирующих бактерий
|
Роды и виды |
Морфология и раз меры клеток, мкм |
Расположение жгутиков |
Содержание ГЦ в ДНК в % |
|
Desulfovibrio D. africanus D. baarsii D. desulfuricans D. gigas D. vulgaris D. salexigens |
Искривленные палочки сигмоидные или пиралевидные 0,5-1,0 х 2,0-10,0 |
Полярное (один жгутик или пучок) |
46,1-61,2 |
|
Desulfotomaculum D. acetoxidans D. nigrificans D. orients D. ruminis Desulfomonas |
Прямые или изо- гнутые палочки 0,3-1,5 х 3,0-9,0 образуют эндоспоры Прямые и слегка
|
Перитрихальное реже полярное |
37,0-45,5 |
|
Desulfomonas D. pigra |
Прямые и слегка изогнутые палочки 0,8-1,0 х 2,5-10,0 Палочки и элипсо-
|
Неподвижны |
66,0 67,0 |
|
Desulfobacter D. postgatei |
Палочки и элипсо- видные 1,0-2,0 х 1,7-3,5
|
полярное (один жгутик или жгутиков нет) |
45,9 |
|
Desulfobulbus D. propionicus Desulfococcus D. multivarans |
Элипсовидные 1,0 – 1,3 х 2,0 Сферические 1,5-2,0
|
Нет жгутиков или полярное. некоторые штаммы подвижны |
59,9 |
В Калужской области имеются природные штаммы иловых бактерий, продуцирующих сероводород, на основе которых возможна последующая селекция на элективных средах высокоактивного штамма сульфатредуцирующих бактерий [5], обеспечивающих стабильный прирост биомассы и высокую степень очистки сточных вод гальванических производств. Для проведения эксперимента были отобраны пробы воды, объемом 10 л и ила объемом 2,5 л (рис.1 б, в). с сероводородных озер, около города Калуги. Озера представляют собой два небольших пруда, находящихся на территории калужского пригородного лесничества (рис. 1 а). Для взятия проб сточной воды проводили отбор средней смешаной пробы за 1 час. При этом взятие проб осуществлялось в различных местах водной поверхности.



а б в
Рисунок. 1. Отбор проб сероводородной воды
а — внешний вид сероводородных озер, б — отбор ила, в — проба ила
В экосистеме сероводородных озер Калужской области температура сниженная. В течение теплого времени года она составляет 4—8. В зимнее время года озера не замерзают. Большинство сульфатредуцирующих бактерий хорошо растут при температуре 25—30. Для отдельных видов оптимальная температура несколько выше (37—46). Необходимо было проверить способность СРБ продуцировать сероводород в условиях лабораторного содержания.
В основу технологии положен принцип стимуляции развития сульфат — редуцирующих бактерий в анаэробных условиях обогащением среды доступным для них органическим веществом. В этих целях предпочтительно использование дешёвых и доступных органических соединений.
В среде для выращивания этих микроорганизмов часто добавляют редуцирующие вещества (дитионин и др.). Обычно среды содержат также в значительном количестве сульфаты и железо(FeS), который выпадает в осадок. Это имеет значение для детоксикации сероводорода, а также позволяет судить о росте сульфатредуцирующих бактерий, т. к. осадок сульфида имеет черный цвет. В то же время присутствие небольшого количества сульфида может быть важно для роста сульфатредуцирующих бактерий, поскольку он относится к числу восстановителей.
Для проведения эксперимента были приготовлены модельные колонии на основе 3 рабочих растворов, содержащих соответственно 0, 50 и 100 мл ила. Также были специально отобраны 2 колонии, в которые добавлялся избыток сульфата в количестве 0,5 и 1 г. В проведенном эксперименте в качестве питательной среды использовалась среда Ван-Дель-Дена (таблица 2). Питательная смесь вносилась регулярно каждые 3 суток во все экспериментальные колонии. Для сравнения были поставлены опыты с контрольными колониями, в которых не содержалось ни питательной среды, ни сульфатов в течение всего периода наблюдения.
Таблица 2
Состав питательной среды
|
Название компонента |
Концентрация, г/л |
|
CH3COONa |
5 |
|
MgSO4 |
1 |
|
K2HPO4 |
0,5 |
В течение исследуемого периода времени наблюдались следующие изменения: во всех рабочих растворах наблюдалось появление побочных продуктов жизнедеятельности бактерий в виде тонкой белой пленки на поверхности воды, наиболее заметной в растворах с 100 и 50 мл ила. Также при открытии крышки появлялся отчетливый запах сероводорода. В контрольных растворах образования пленки не наблюдалось, а запах был выражен намного слабее.
В данном исследовании ставилась цель изучить условия продуцирования сероводорода сульфатредуцирующими бактериями в модельных растворах. Количественные характеристики процесса определяли по протеканию реакции образования сульфида свинца на фильтровальной бумаге, смоченной раствором ацетата свинца. В результате протекания реакции
![]()
бумага окрашивалась в темный цвет, который соответствует сульфиду свинца. По оттенку окраски бумаги можно судить и о концентрации образующегося в результате сульфатредукции сероводорода.
Количественную оценку осуществляли с использованием программы Adobe Photoshop. Проводили фотографирование образцов во влажном состоянии бытовым фотоаппаратом Canon ISUS 210, затем фотографические снимки переводили в файлы с расширением *.CR 2, поскольку данные изображения не подлежат редактированию программными средствами. Цветовая характеристика цветного изображения имеет 3 параметра — R,G,B, дающие вклад по основным цветам (красному, зеленому, синему). Для монохромного изображения величины цветовых параметров выравниваются (R=G=B), характеристикой серого изображения является яркость. Для каждого результата анализа фиксировали значения в 3 произвольных точках и находили среднее, результаты приведены в таблице.
Таблица 3
Результаты измерения яркости
|
Дата |
Без питания |
С питанием 30мл. 1 раз в 3 дня |
|||||
|
контрольная проба |
вариация количества ила, мл |
вариация содержания сульфат-ионов, мг |
|||||
|
без ила |
100 мл ила |
0 |
50 |
100 |
0,5 |
1 |
|
|
24.сен |
235,7 |
242,3 |
228,3 |
229,0 |
202,0 |
177,7 |
222,0 |
|
27.сен |
229,0 |
227,3 |
218,3 |
195,7 |
155,3 |
194,7 |
203,7 |
|
29.сен |
225,3 |
234,0 |
209,3 |
152,3 |
110,3 |
142,7 |
155,3 |
|
05.окт |
224,3 |
237,3 |
189,7 |
114,0 |
107,7 |
126,3 |
151,3 |
|
08.окт |
185,7 |
151,0 |
75,0 |
99,0 |
57,0 |
133,7 |
133,7 |
|
11.окт |
173,7 |
145,3 |
137,0 |
97,0 |
83,3 |
55,7 |
71,7 |
Известно, что цветовая характеристики черного цвета имеет минимальное значение яркости B(000), в то время как белый цвет имеет максимальную яркость (255). Таким образом можно оценить интенсивность и оттенок цветового изображения. Зная, что соединения сульфида свинца имеют темную окраску, можно таким образом оценить количество продуцируемого сероводорода .
Далее результаты были преобразованы, для получения значения насыщенности цвета.
![]() , (1)
, (1)
где A — значения насыщенности цвета,
B1, B2, B3 — значения яркости в 3 произвольных точках.
По результатам были построены графики, которые показаны на рис. 3 и 4.
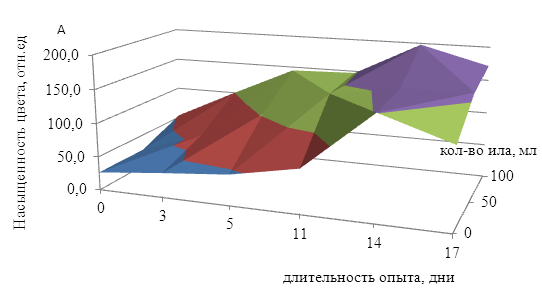
Рисунок 3. График изменения содержания сульфид-ионов в пробах с различным содержанием ила
Из графика 3 видно, что для всех условий рост идет равномерно, наибольшее содержание сероводорода на всем протяжении эксперимента наблюдалось в рабочем растворе, содержащем 100 мл ила.
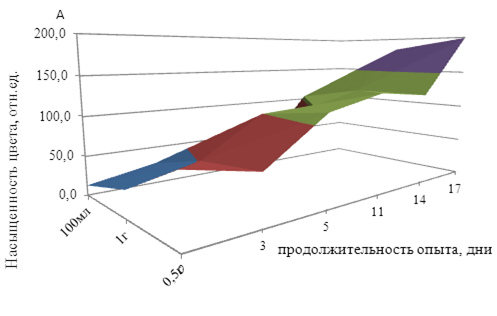
Рисунок. 4. Диаграммы результатов деятельности бактерий в зависимости от исходного содержания сульфат-ионов
Из рисунка 4 видно неоднозначное изменение концентрации образующихся сульфид-ионов. Процесс идет неравномерно. Наилучние условия достигаются при 0,5 г сульфат ионов.
Таким образом, в эксперименте было показано, что природные штаммы иловых бактерий устойчиво размножаются и существуют на питательных средах в течение длительного периода времени, обеспечивают прирост биомассы и продуцирование сероводорода.
Одновременно проводили моделирование процесса потребления субстрата бактериальными клетками [6]. Была создана программа, производящая расчет по справочным данным и построение графиков зависимости скорости потребления субстрата от его концентрации. Для этого использовали стандартные возможности Microsoft Office Excel (программирование на языке VBA) с использованием библиотеки Microsoft Forms 2.0 Object Library.
Стандартными процедурами была создана форма для ввода 4 переменных и их описания, а также управляющих кнопок «подробнее», «далее», «отмена». Затем добавили 4 поля ввода для переменных: «Константа удельной скорости утилизации субстрата внутри клетки», «Константа проницаемости клеточной стенки», «Толщина клеточной стенки», «Плотность сухого вещества клеточной стенки». Для вывода на экран форм и обработки данных был составлен ряд макросов. Каждый макрос представляет собой процедуру, которую вызывают при нажатии кнопок.
Программа использует для расчета:
· константу удельной скорости утилизации субстрата внутри клетки, с-1 — ( 0,11) . 10-4;
· константу проницаемости клеточной стенки, см/с — (0,11) .10-5;
· толщину клеточной стенки, см — 1. 10-5 5 . 10-6;
· плотность сухого вещества клеточной стенки, г/см3 — 0,2 0,8.
После введения всех промежуточных данных в рабочий лист производится построение графика (рис. 5 а).
Для проверки полученных расчетов был построен график зависимости насыщенности от концентрации субстрата для пробы, содержащей 100 г ила.
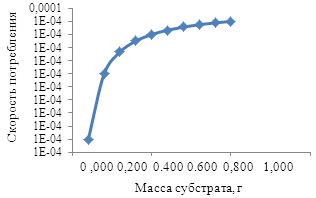
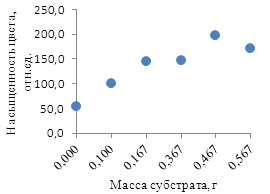
а б
Рисунок 5. Результаты экспериментов:
а — компьютерное моделирование, б — натурный
Таким образом показано, что расчеты по математическим моделям описываемых процессов потребления субстрата идентичны результатам поставленных экспериментов. На их основе определены наиболее благоприятные условия жизнедеятельности модельной колонии сульфатредуцирующих бактерий (удельные величины на 1 л воды):
1. количество ил —100 мл,
2. содержание сульфат-ионов — 0,05 г,
3. содержание основных ионов в воде — N-0,01, P— 0,01 г , C — 0,1 г,
4. частота внесения питательных веществ — 1 раз/72 час.
Список литературы:
1.Гринин А.С., Новиков В.Н. Промышленные и бытовые отходы: Хранение, утилизация, переработка. — Калуга, изд-во МГТУ им. Н.Э. Баумана, 2002. — С. 214.
2.Кафаров В.В. Принципы создания безотходных технологий химических производств. — М.: Химия, 1982. — С. 285.
3.Минниахметов В.Р. Перспективы использования военных объектов для резервации и переработки отходов // Безопасность жизнедеятельности: наука, образование,практика:материалы II Межрегиональной научно-практической конференции с международным участием (28 ноября 2011 года, Южно-Сахалинск): сборник научных статей — Южно-Сахалинск: изд-во СахГУ, 2012. — с. 108—110.
4.Минниахметов В.Р. Технологические основы комплексной переработки отходов различного происхождения с использованием метано — и сульфатредуцирующих бактерий // Сборник материалов Международной научно-практической конференции и школы молодых ученых и студентов «Образование и наука для устойчивого развития», посвященная 40-летию проведения Конференции ООН по окружающей среде и развитию и выходу доклада Римского клуба «Пределы роста» — М.: РХТУ им. Д.И. Менделеева, 2012. — ч. 1. — С. 53—58.
5.Минниахметов В.Р. Окунев Д.С. Наумов И.И. Влияние размеров и формы бактериальной клетки на скорость потребления субстрата // Наукоемкие технологии в приборо — и машиностроении и развитие инновационной деятельности в вузе: Материалы региональной научно-технической конференции, 18—19 апреля 2012 г. Т. 2 — М., Изд. МГТУ им. Н.Э.Баумана, 2012. — С. 29—33.
6.Окунев Д.С. Минниахметов В.Р. Оптимизация условий роста микроорганизмов на моносубстрате // Наукоемкие технологии в приборо — и машиностроении и развитие инновационной деятельности в вузе: Материалы региональной научно-технической конференции, 18-19апреля 2012 г. Т. 2 — М., Изд. МГТУ им. Н.Э. Баумана, 2012. — С. 23—29.
7.Теппер Е.З. Практикум по микробиологии: Учебное пособие для вузов. — 5-е изд., перераб. и доп. — М.: Дрофа, 2004. — 256 с.
отправлен участнику

