Статья опубликована в рамках: XXIV Международной научно-практической конференции «Технические науки - от теории к практике» (Россия, г. Новосибирск, 07 августа 2013 г.)
Наука: Технические науки
Секция: Химическая техника и технология
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
ХИМИЧЕСКОЕ ОБЕСПЕЧЕНИЕ НОВОЙ ТЕХНОЛОГИИ ИЗВЛЕЧЕНИЯ МЕТАЛЛОВ ИЗ ТЕХНОГЕННЫХ ОТХОДОВ
Хентов Виктор Яковлевич
д-р хим. наук, профессор Южно-Российского государственного технического университета, г. Новочеркасск
E-mail: vkhentov@mail.ru
Великанова Лидия Николаевна
канд. хим. наук, доцент Южно-Российского государственного технического университета, г. Новочеркасск
Сёмченко Владимир Владимирович
канд. хим. наук, доцент Южно-Российского государственного технического университета, г. Новочеркасск
Хуссейн Ханаа Хассан
аспирант Южно-Российского государственного технического университета, г. Новочеркасск
CHEMICAL SECURITY NEW EXTRACTIVE METALLURGY INDUSTRIAL WASTE
Victor Khentov
doctor of Chemical Sciences, Professor of South-Russian State Technical University, Novocherkassk
Lidiya Velykanova
candidate of Chemical Sciences, Associate Professor of South-Russian State Technical University, Novocherkassk
Vladimir Semchenko
candidate of Chemical Sciences, Associate Professor of South-Russian State Technical University, Novocherkassk
Khan Hussain
Graduate student of South-Russian State Technical University, Novocherkassk
АННОТАЦИЯ
Разработаны основы химического обеспечения новой технологии извлечения металлов из техногенного сырья. Метод извлечения металлов базируется на донорно-акцепторном взаимодействии нуль-валентных металлов и их ковалентных соединений с органическим лигандом в неводном растворителе. Из комплексных соединений металл может быть выделен электрохимически, термическим разложением комплекса, восстановлением сильным восстановителем. Комплексообразование может быть использовано для реставрации нанесенных катализаторов, ионселективных электродов, снятия отложений с поверхности химической аппаратуры.
ABSTRACT
The fundamentals of chemical ensure the new technology of extraction of metals from industrial wastes. Method of extraction of metals based on the donor-acceptor interaction zero-valent metals and their compounds with covalent ligand in non-aqueous organic solvent. Transferred from the dissolved state in the metal complex can be recovered by thermal decomposition of the complex, a strong reduction of a reducing agent and electrochemically. Complexation can be used for restoration of supported catalysts, ion-selective electrodes, removing deposits on the surface of chemical apparatus.
Ключевые слова: донорно-акцепторные системы; неводные растворители; структурные параметры твердого тела; мицеллярный катализ; ; критическая концентрация мицеллообразования; рециклинг металлов.
Keywords: donor-acceptor system; non-aqueous solvents; solid structural parameters; micellar catalysis; critical micelle concentration; recycle of metals.
Производственная деятельность человека привела к значительному накоплению техногенных отходов. Основными производителями отходов являются горнодобывающие, металлургические, топливно-энергетические, химические и электрохимические предприятия. Значительное количество отходов приходится на пылевые выбросы промышленных предприятий, отвалы горнодобывающей и металлургической промышленности, зольные отходы тепловых электростанций. В техногенных отходах, которые геологи называют техногенными залежами, содержатся разнообразные металлические элементы. Это металлы платиновой группы, золото, серебро и другие самые разнообразные переходные металлы. Металлические элементы в отходах находятся в свободном состоянии и в виде ковалентных химических соединений. Металлы содержатся в отработанных катализаторах, шламах гальванических предприятий, в золошлаковых отходах, в дымовых газах.
К сожалению, существующие гидрометаллургические методы исчерпали свои возможности. Перевод металлических элементов в растворенное состояние при малом содержании в отходах может быть произведен на основе использования неводных донорно-акцепторных систем. Установлено, что нуль-валентные металлы и их ковалентные соединения активно взаимодействуют с органическим лигандом, растворенным в неводном растворителе [5, 9, 10, 11]. В табл. 1 представлены кинетические параметры, демонстрирующие эффективность взаимодействия ряда соединений с салицилальанилином в диметилформамиде.
Таблица 1.
Скорость взаимодействия V, энергия активации Еа [10]
|
Соединение |
V·106, моль/(см2∙ч) |
Еа, кДж/моль |
Соединение |
V·106, моль/(см2∙ч) |
Еа, кДж/моль |
|
Cu2O |
1,27 |
54,0 |
Ni2O3 |
0,04 |
143,0 |
|
CuO |
0,50 |
71,0 |
CoO |
0,56 |
137,4 |
|
Cu(OH)2 |
14,85 |
19,5 |
Co2O3 |
0,11 |
129,0 |
|
(CuOH)2CO3 |
18,80 |
43,3 |
FeO |
0,33 |
150,9 |
|
Cu3(PO4)2 |
0,05 |
54,3 |
Fe2O3 |
0,30 |
139,0 |
|
Cu2S |
1,97 |
18,3 |
MoO3 |
0,97 |
141,0 |
|
CuS |
1,29 |
38,9 |
WO3 |
0,74 |
114,4 |
|
NiO |
0,21 |
150,0 |
Ag2S |
3,70 |
51,1 |
Донорно-акцепторная система позволяет извлекать металлы из бедного рудного сырья (табл. 2) [3, 10, 11].
Таблица 2.
Скорость извлечения металла V (моль/г·ч), энергия активации Ea (кДж/моль), степень извлечения α (%)
|
Рудное сырье |
Формула |
V·105 |
Ea |
α |
|
Халькопирит |
CuFeS2 |
64,00 |
53±2 |
37,61 |
|
Халькозин |
Cu2S |
148,00 |
18,3±1 |
81,39 |
|
Ковеллин |
CuS |
76,00 |
38,9±2 |
85,60 |
|
Борнит |
Cu5FeS4 |
22,00 |
117±3 |
47,60 |
|
Куприт |
Cu2O |
19,00 |
36±1 |
63,33 |
|
Тенорит |
CuO |
59,00 |
68±2 |
70,60 |
|
Малахит |
(CuOH)2CO3 |
24,00 |
43±4 |
79,89 |
|
Шпинель |
CuFe2O4 |
3,33 |
171±3 |
72,47 |
|
Гематит |
Fe2O3 |
3,75 |
98±2 |
76,70 |
|
Магнетит |
Fe3O4 |
0,13 |
87±3 |
69,59 |
|
Сидерит |
FeCO3 |
1,50 |
69±2 |
72,34 |
|
Ванадит |
Pb5(VO4)3Cl |
58,00 |
45±4 |
50,71 |
|
Аргентит |
Ag2S |
183,00 |
- |
76,00 |
Реакционная способность лиганда в полярных растворителях существенно возрастает. Найдена связь константы донорно-акцепторного взаимодействия нуль-валентного металла с салицилальанилином k и параметра полярности растворителя Димрота-Райхардта ЕТ [10]:
ln k = aET + b,
где: a и b — эмпирические коэффициенты.
Подобные зависимости получены и для других металлов. Причем коэффициенты этих зависимостей для растворителей, содержащих и не содержащих кислород, заметно различаются. Очевидно, что электрофильность растворителя в донорно-акцепторном взаимодействии играет важнейшую роль.
В смешанных растворителях происходит изменение сольватации лиганда, что отражается на скорости донорно-акцепторного взаимодействия (рис. 1) [8].
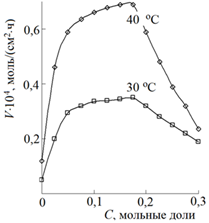
Рисунок 1. Зависимость скорости V взаимодействия компактной меди с 0,01 М раствором салицилальанилина в диметилформамиде от концентрации воды С
Особый интерес вызывает применение в качестве неводного растворителя микрогетерогенных организованных сред на основе поверхностно-активных веществ (ПАВ) [4]. С этими средами связано проявление мицеллярного катализа. Мицеллы, играющие роль микрореакторов, появляются при введении в воду ПАВ при концентрациях превышающих критическую концентрацию мицеллообразования (ККМ). Для неводных растворителей ККМ возрастает на несколько порядков. Этот результат получен авторами при изучении вязкости и поверхностного натяжения. Введение в диметилформамид оксиэтилированного изооктилфенола RC6H4O(CH2CH2O)nH, где n = 7 (число присоединенных молей оксида этилена), R — гидрофобный углеводородный радикал С6-С10, ККМ при 20 оС была достигнута при 15-ти процентном содержании ПАВ. В такой организованной среде с содержанием лиганда салицилальанилина (0,1 моль/л), скорость донорно-акцепторного взаимодействия при 20 оС возросла в три раза.
Важную роль в процессе донорно-акцепторного взаимодействия играют структурные параметры твердого тела. Установлена связь энергии активации Ea реакции взаимодействия переходного металла с салицилальанилином (0,01 М) в диметилформамиде и физическими параметрами, характеризующими твердое тело (работа выхода Aвых, энергия сублимации Eсуб, теплота образования оксидов при 298 К H, энергия связи элемента Eсв, температура плавления Tпл, температура кипения Tкип, поверхностная энергия зародыша кристаллизации W, атомная концентрация элемента Cат). В табл. 3 представлены корреляционные зависимости. Расчеты выполнены на основании данных приведенных в [12].
Таблица 3.
Корреляционные зависимости между энергии активации Ea и физическими параметрами металлов, коэффициент корреляции R
|
Физический параметр металла |
Функциональная зависимость |
R |
|
Авых, эВ |
Еа = 1048,56–223,27Авых |
0,74 |
|
Eсуб, кДж/моль |
Еа = –298,95 + 0,90Eсуб |
0,74 |
|
H, кДж/моль |
Еа = -36,60 + 0,40H |
0,74 |
|
Eсв, кДж/моль |
Еа = –426,380 + 5,396Есв |
0,90 |
|
Тпл, оС |
Еа = –333,323 + 0,315Тпл |
0,96 |
|
Ткип, оС |
Еа = –1008,945 + 0,401Ткип |
0,83 |
|
W, эрг/см2 |
Еа = –278,004 + 1,695W |
0,96 |
|
Cат., 1022, см-3 |
Еа = –1334,403 + 162,576Cат |
0,92 |
Для химического восстановления переходных металлов из комплексных соединений может быть использован сильный восстановитель гидразин:
N2H4 – 2e ® N2 + 4H+ −1,16 B.
Восстановление металла происходит по схеме:
Меz+(растворитель–лиганд) + N2H4® Me¯ + N2 + 4H+(растворитель–лиганд).
Скорость реакции может быть вычислена по количеству выделившегося азота.
При термическом разложении комплексного соединения образуются в высокодисперсном состоянии металл и его оксид. Соотношение продуктов разложения зависит от природы металла, структуры комплекса и кинетических параметров термической обработки. При терморазложении биметаллических комплексов могут быть получены нано частицы металлических сплавов.
Электроосаждение металла может быть выполнено из неводных растворов комплексных соединений. Неводный растворитель в области потенциалов от +1 до ‒2 В электрохимически устойчив.
Донорно-акцепторные системы нашли использование в реставрационных процессах. Реставрацию отработанного катализатора производят раствором лиганда в неводном растворителе [13]. В результате образуются комплексные соединения переходных металлов. Затем производят пропитку пористого носителя и восстановление комплекса до металла. Одновременно может быть получен оксид металла.
Донорно-акцепторные системы были использованы для реставрации Cu-селективных электродов [6]. С целью восстановления чувствительности электродов проводили их обработку в растворах салицилальанилина в диметилформамиде, промывку и сушку. Изменение чувствительности Cu-селективных электродов демонстрирует табл. 4.
Таблица 4.
Изменение чувствительности Cu-селективных электродов
|
Чувствительность, мВ/pCu |
Примечания |
|
26 |
Механическое формование электрода |
|
15 |
После 17 лет эксплуатации электрода |
|
35 |
После реставрации |
Донорно-акцепторные системы были использованы для удаления оксидов с поверхности металлических деталей [1] и удаления тонкопленочных покрытий с отбракованных оптических изделий [2].
Список литературы:
1.А. с. 1216252 СССР: Кл. С 23 F 1/28. Состав для снятия окалины с поверхности никеля / В.Я. Хентов, Л.Н. Великанова, Л.К. Ефимова и др. — Заявл. 13.01.84; Опубл. 07.03.86, Бюл. № 9.
2.А. с. 1686034 СССР: Кл. С 09 К 13/08 Состав для снятия тугоплавких покрытий на основе d-элементов IV-группы с металлических деталей / Ш.А. Фурман, В.Я. Хентов, Ю.В. Власов, Л.Н. Великанова. — Заявл. 24.07.89; Опубл. 23.10.91, Бюл. № 39.
3.Великанова Л.Н., Семченко В.В., Хентов В.Я. Кинетические закономерности извлечения металлов из техногенного сырья. // Журнал прикладной химии. — 2011. — Т. 84. — Вып. 9. — С. 1418—1423.
4.Вережников В.Н. Организованные среды на основе коллоидных поверхностно-активных веществ. — Издательско-полиграфический центр Воронежского государственного университета. — 2008. — 74 с.
5.Кужаров А.С., Хентов В.Я. О взаимодействии высокодисперсных переходных металлов с салицилальанилином // Координационная химия, — 1979. — № 4. — С. 601.
6.Патент 2186378 РФ: Кл. 7 G 01 № 27/30 Способ получения и регенерации мембраны Cu-селективного электрода / Л.Н. Великанова, И.И. Волченко, М.С. Липкин и др. — Заявл. 03.07.02; Опубл. 27.07.02, Бюл. № 21.
7.Семченко В.В., Великанова Л.Н., Хентов В.Я. Влияние природы растворителя на кинетику донорно-акцепторного взаимодействия меди с салицилальанилином. // Известия вузов. Северо-Кавказский. регион. Технические науки. — 1998. — № 2. — С. 55—58.
8.Семченко В.В. Особенности кинетики координационного взаимодей-ствия d-металлов и их соединений с 2-окси-1-бензилиденанилином в апротонных и смешанных растворителях: Дис.…к. х. н. — Нальчик, 2009. — 129 с.
9.Хентов В.Я., Великанова Л.Н., Кужаров А.С., Верещака В.В. Донорно-акцепторное взаимодействие меди, никеля и их труднорастворимых соединений с салицилальанилином. // Интенсификация процессов переработки минерального сырья. — М.: — Наука. — 1981. — С. 156—159.
10.Хентов В.Я., Великанова Л.Н., Семченко В.В., Слабинская А.Б. Извлечение металлов из техногенного сырья. // Журнал прикладной химии. — 2007. — Т. 80. — Вып. 7. — С. 1057—1062.
11.Хентов В.Я., Великанова Л.Н., Семченко В.В., Егорова Н.А. Решение проблемы рециклинга металлов на основе донорно-акцепторных систем. // Экология и промышленность России. — 2009. — Март. — С. 48—49.
12.Хентов В.Я. Корреляционный анализ в неорганической химии. Задания для работы с персональным компьютером: учебное пособие. Новочеркасск: Юж.-Рос. гос. техн. ун-т (НПИ), 2007. — 187 с.
13.Хентов В.Я., Липкина Т.В., Липкин М.С. Основы регенерации металлсодержащих катализаторов. // Безопасность жизнедеятельности. Охрана труда и окружающей среды: Межвуз. сб. науч. тр. — Ростов-н/Д.: РГАСХМ, 2001. — Вып. 5. — С. 111—112.
дипломов

