Статья опубликована в рамках: XXXIII Международной научно-практической конференции «Научное сообщество студентов XXI столетия. ТЕХНИЧЕСКИЕ НАУКИ» (Россия, г. Новосибирск, 30 июня 2015 г.)
Наука: Технические науки
Секция: Металлургия
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
ИССЛЕДОВАНИЕ ВЛИЯНИЯ КОКСА В АТМОСФЕРЕ ПЕЧИ НА ОКИСЛЕНИЕ СТАЛИ
Жиденко Алексей Иванович
E -mail: lexsey1236@y andex.ru
Лавриненко Кирилл Владиславович
Зубова Дарья Евгеньевна
Е-mail : Dasha 8121995@mail.ru
студенты 2 курса, кафедры металлургии и металловедения, факультета ММТ СТИ (филилал) НИТУ МИСиС, РФ, г. Старый Оскол
Ряполов Вадим Владимирович
студент 3 курса, кафедры металлургии и металловедения, факультета ММТ СТИ (филилал) НИТУ МИСиС, РФ, г. Старый Оскол
Тимофеева Анна Стефановна
научный руководитель, канд. техн. наук, доцент кафедры ММ СТИ НИТУ МИСиС, РФ, г. Старый Оскол
E -mail: uked @yandex.ru
Под окислением стали понимают процесс взаимодействия газов (воздуха, продуктов сгорания топлива или контролируемой атмосферы) с железом, сопровождающийся образованием слоя оксидов на поверхности металла. Применительно к нагреву стали в пламенных печах перед обработкой давлением основными окислительными газами являются: углекислый газ (СО2), кислород (О2), водяной пар (Н2О). Реакции окисления железа экзотермические и происходят следующим образом:
Fe + 0,5О2 = FeO, (1.1)
3FeO + 0,5О2 = Fe3О4, (1.2)
2Fe3О4+ 0,5О2 = 3Fe2О3, (1.3)
Fe + CО2 = FeO + CO, (1.4)
Fe + H2О = FeO + H2, (1.5)
3FeO + CО2 = Fe3О4+ CO, (1.6)
3FeO + H2О = Fe3О4+ H2. (1.7)
В порядке убывания активности окислительные газы пламенных печей можно расположить следующим образом: О2, воздух, Н2О, СО2. Способность атмосферы взаимодействовать с железом определяется соотношениями СО2/С0 и Н2О/Н2, зависящими от коэффициента расхода воздуха и температуры, которые могут быть определены из соответствующих для различных видов топлив диаграмм. Безокислительный нагрев стали под обработку давлением может быть достигнут в атмосфере продуктов сгорания природного газа с коэффициентом расхода воздуха 0,45—0,52, коксового газа — 0,40—0,45, бутан-пропановой смеси — 0,54, мазута — 0,6. Увеличение коэффициента избытка воздуха более 1,1, как правило, не влияет на интенсивность окалинообразования, поскольку в этом случае процесс окисления лимитирует не скорость подвода молекул кислорода к поверхности окалины, а их диффузия через нее к поверхности металла [1].
Характерно, что в некоторых случаях увеличение коэффициента расхода воздуха приводит даже к снижению угара. Это явление связано с тем, что водяной пар в топочных газах иногда интенсифицирует окисление больше, чем кислород воздуха, поэтому разбавление продуктов сгорания, содержащих значительное количество Н2О, приводит к снижению окалинообразования [1].
Окисление зависит от температуры, марки стали, времени нахождения заготовки в печи, атмосферы печи и других. Нами, на кафедре ММ ведутся исследования окисления стали в лабораторных условиях.
Мы провели эксперименты по исследованию окалинообразования в металле при изменении скорости нагрева металла, а так же изменении рабочей атмосферы в печи.
Для экспериментов брали углеродистую сталь, образцы которой выполнены в виде цилиндров радиусом 10,5 мм и высотой 50 мм. Цилиндры взвешивались до начала эксперимента на весах с точностью до 0,01 г, определялись точно размеры с помощью электронного штангенциркуля, а затем помещались в печь SNOL 7,2/1300.
1 эксперимент: печь нагрева была запрограммирована на нагрев до 950 оС и выдержка до 3часов.
2 эксперимент: нагрев до 1100оС и выдержка до 3часов.
3 эксперимент: нагрев до 1200оС и выдержка до 3часов.
4 эксперимент: нагрев до 1100оС с коксом и выдержка до 3 часов.
5 эксперимент: нагрев до 1200оС с коксом и выдержка до 3 часов.
Для более точного результата эксперимента в печь производили посадку после нагрева печи одинаковых образцов и по размеру и по марке стали. Через каждые 90 минут, затем через 135 минут и через 180 минут по 2 образца забирали из печи.

Рисунок 1. Эксперименты по определению окалинообразования металла при нагреве
Таким образом, первые 2 образца находились в течение 90минут в печи под воздействием температур, указанных в экспериментах выше, следующие 2 образца находились в печи в течение 135 минут, затем 2 образца — 180 минут, причем все при одной и той же температуре.
Каждый образец после печи взвешивался на весах (рис. 2).

Рисунок 2. Взвешивание образца на весах
Результаты для каждого варианта расчета окалины усреднялись. После взвешивания образцы охлаждались естественным путем (рис. 3).

Рисунок 3. Охлаждение образцов
При полном охлаждении образцов с них снималась окалина и образец вновь взвешивался. Окалина находилась по разности массы образца после нагрева сразу и после очистки от окалины. Результаты экспериментов представлены в таблицах.
Таблица 1.
Результаты эксперимента при температуре 950 оС
|
мин |
Масса нач. г M 0 |
Масса после нагрева M 1 |
Изменение массы после нагрева m ,г |
Масса после очистки M 2,г |
масса окалины,г |
|
90 |
177.9 |
178,8 |
0.9 |
175,9 |
0,9 |
|
135 |
154,4 |
157,9 |
3.5 |
154,8 |
3,1 |
|
180 |
148,6 |
151,6 |
3 |
146,9 |
4,7 |
Таблица2.
Результаты эксперимента при температуре 1100 оС
|
мин |
Масса нач. г M 0 |
Масса после нагрева M 1 |
Изменение массы после нагрева m ,г |
Масса после очистки M 2,г |
Масса окалины, г |
|
90 |
231,7 |
233 |
1,3 |
230,3 |
2,7 |
|
135 |
232,1 |
234.3 |
2,2 |
226,0 |
8,3 |
|
180 |
232,1 |
235.4 |
3,3 |
224,2 |
11,2 |
Таблица 3.
Результаты эксперимента при температуре 1200 оС
|
мин |
Масса нач. г M 0 |
Масса после Нагрева M 1 |
Изменение массы после нагрева m ,г |
Масса после очистки M 2,г |
масса окалины, г |
|
90 |
134,2 |
134,7 |
0,5 |
132,3 |
2,4 |
|
135 |
134,1 |
136 |
1,9 |
125,8 |
10,2 |
|
180 |
134,4 |
137 |
2,6 |
124,1 |
12,9 |
Таблица 4.
Результаты эксперимента с коксом при температуре 1100 оС
|
мин |
Масса нач. г M 0 |
Масса после Нагрева M 1 |
Изменение массы после нагрева m ,г |
Масса после очистки M 2,г |
масса окалины, г |
|
90 |
226,6 |
228,2 |
1,6 |
225,2 |
3 |
|
135 |
222,6 |
224,5 |
1,9 |
214,9 |
9,6 |
|
180 |
215,5 |
217,7 |
2,2 |
205,6 |
12,1 |
Таблица 5.
Результаты эксперимента с коксом при температуре 1200 оС
|
мин |
Масса нач. г M 0 |
Масса после Нагрева M 1 |
Изменение массы после нагрева m ,г |
Масса после очистки M 2,г |
масса окалины, г |
|
90 |
134,2 |
134,7 |
0,5 |
132,1 |
2,6 |
|
135 |
133,8 |
137 |
3,2 |
124,4 |
12,6 |
|
180 |
134,4 |
137 |
2,6 |
123.6 |
13,4 |
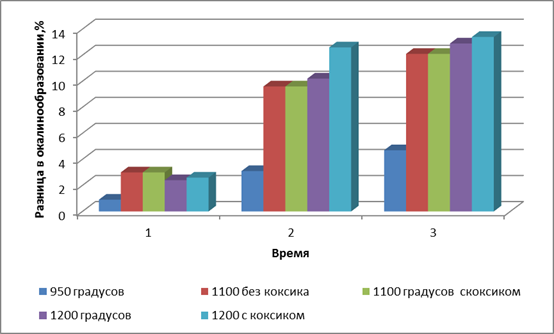
Рисунок 4. Влияние времени на рост окалины (1 — время 90 минут; 2 — время 135 минут; 3 — время 180 минут)
Анализируя данные экспериментов, можно сделать вывод, что с увеличением времени, масса окалины возрастает, причем, чем больше температура, тем быстрее происходит окисление. Так же масса окалины увеличивается и при атмосфере коксового газа. Это можно объяснить тем, что коксовый газ содержит CO2, который способствует окалинообразованию. Так как при взаимодействии с железом СО2 образует оксид железа FeO.
По данным таблицы видно, что при температуре 1200 оС окалинообразование на 1,8 % больше (рис. 4) — значит надо уменьшить в газе СО2, а это можно сделать, если сгорает газ с недожогом, а затем углекислый газ дожечь после печи и отправить тепло на рекуператор.
Список литературы:
1.Темлянцев М.В., Михайленко Ю.Е. Окисление и обезуглероживание стали в процессах нагрева под обработку давлением. М.: Теплотехник, 2006. — 200 с.
дипломов

