Статья опубликована в рамках: VII Международной научно-практической конференции «Научное сообщество студентов XXI столетия. ТЕХНИЧЕСКИЕ НАУКИ» (Россия, г. Новосибирск, 25 декабря 2012 г.)
Наука: Технические науки
Секция: Материаловедение
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
отправлен участнику
МОРФОЛОГИЯ КАЛЬЦИЙ-ФОСФАТНЫХ ПОКРЫТИЙ, СФОРМИРОВАННЫХ ПРИ РАЗЛИЧНЫХ РЕЖИМАХ ВЫСОКОЧАСТОТНОГО МАГНЕТРОННОГО НАПЫЛЕНИЯ
Мальчихина Алёна Игоревна
студент 2 курса магистратуры, кафедра водородной энергетики и плазменных технологий ТПУ, г. Томск
Е-mail:
Богомолова Наталья Николаевна
студент 3 курса, кафедра водородной энергетики и плазменных технологий ТПУ, г. Томск
Твердохлебов Сергей Иванович
научный руководитель, канд. физ.-мат. наук, доцент ТПУ, г. Томск
Современное медицинское материаловедение нацелено на создание новых материалов, которые могут быть использованы в имплантологии. Такие области медицины, как эндопротезирование, стоматология, ортопедия, травматология нуждаются в разработке материалов для имплантатов. К этим материалам предъявляются высокие требования по биосовместимости, механическим параметрам, стабильности свойств, срокам использования в человеческом организме [3].
Для лечения костных травм в современной медицине используются имплантаты, изготовленные на основе разрешенных для этих целей материалов (к ним относятся, например, титан, сплавы титана, специальные легированные стали и их сплавы), способных выдерживать значительные механические нагрузки, прикладываемые к костному сегменту в процессе жизнедеятельности организма. Но при длительном пребывании имплантатов в среде организма они подвергаются коррозионному воздействию. В результате на их поверхности возникают продукты коррозии на основе ионов металлов, которые диффундируют в прилегающие биоструктуры, вызывая металлоз. Это приводит к появлению вокруг имплантатов фиброзной капсулы, способствующей расшатыванию имплантатов и воспалению тканей. В результате этих процессов появляются различные осложнения, затрудняющие остеоинтеграцию и снижающие результативность лечения. В целом, современные имплантаты характеризуются высокой механической совместимостью с костной тканью, но при этом они имеют ограниченную биологическую совместимость. Доказано, что основное влияние на процесс образования костных тканей на поверхности имплантата оказывают три фактора: химический состав имплантата, поверхностная энергия и морфологическая структура [5]. Эти факторы определяют результат остеоинтеграции в целом, а также отдельных ее этапов: осаждения, миграции, пролиферации и дифференцировки клеток [6]. Поверхность костных имплантатов с целью быстрейшего заживления травмы должна быть биоактивной, что можно достичь с помощью нанесения специальных покрытий. Покрытие должно иметь хорошую адгезию и обеспечивать прочное сцепление имплантата с костью. Наиболее подходящим для создания покрытий материалом являются кальций-фосфатные (КФ) соединения, так как они соответствуют составу и структуре кости.
Морфология поверхности имплантата является одним из параметров, влияющих на адгезию биологических клеток к нему, поэтому, в зависимости от назначения, оптимальной может быть шероховатая или идеально гладкая поверхность.
Согласно ГОСТ 9.407-84 [2], который можно применить и к покрытиям для медицинских имплантатов, оно должно быть равномерным, однородным, без пор, трещин, отслаиваний и пузырей.
Поверхность имплантата для остеосинтеза должна быть без посторонних включений, обладать достаточной шероховатостью для обеспечения хорошей остеоинтеграции [1]. Поэтому морфология покрытий является одним из параметров, определяющих способность остеобластов прикрепляться к поверхности имплантата. Увеличение шероховатости биологически совместимых покрытий на имплантатах для остеосинтеза в микромасштабе (по сравнению с гладкими) придает им большую поверхностную энергию, смачиваемость и может являться дополнительным стимулирующим фактором роста тканей посредством прикрепления и пролиферации остеогенных клеток на поверхности КФ покрытия, что в конечном итоге позволяет достичь увеличения площади костной интеграции [4].
Для напыления тонких КФ магнетронных покрытий в данной работе использовалась промышленная установка «Катод 1М», в вакуумной камере которой размещался штатный высокочастотный магнетронный источник с мишенью из синтетического гидроксиапатита. Питание магнетрона осуществлялось от ВЧ генератора с максимальной мощностью 4 кВт и рабочей частотой 13,56 МГц. Покрытия формировались при режимах, указанных в таблице 1.
Таблица 1.
Режимы напыления КФ покрытий
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
* газовая смесь аргона с кислородом в пропорции 1:1 при суммарном давлении 0,3 Па, далее в тексте данный режим будет обозначаться (Ar + О2).
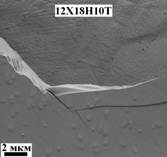
Для изучения влияния режимов напыления на морфологию КФ покрытий использовались подложки кремния (100) с 14 классом шероховатости поверхности и подложки из нержавеющей стали 12Х18Н10Т с 13 классом шероховатости. Изображения КФ покрытий получены с помощью автоэмиссионного растрового электронного микроскопа RAITH 150-TWO, морфология и шероховатость покрытий — с помощью атомно-силового микроскопа «Solver-HV». Электронно-микроскопические исследования скола КФ покрытий, сформированных на кремнии в различных режимах (см. рис. 1), демонстрируют, что в пленках по всей глубине отсутствуют поры и морфологические дефекты (трещины, сколы), отражающие субструктурные изменения. Анализ поверхности КФ покрытий, сформированных на пластинах кремния при различных режимах напыления (см. рис. 2), показал, что все исследованные покрытия являются равномерными, сплошными, без трещин, пузырей и сколов, однако имеют разную шероховатость (см. рис. 2, 2 ряд) (табл. 2). КФ покрытие увеличивает микрошероховатость исходной полированной кремниевой подложки, максимальная шероховатость характерна для КФ пленок, сформированных в режиме Ar+O2. По результатам измерений шероховатости поверхности стали 12Х18Н10Т до и после оксидирования (см. табл. 2) можно констатировать, что оксидный слой толщиной 0,15 мкм фактически не меняет исходную шероховатость стальных подложек. Изображения стали 12Х18Н10Т с КФ покрытием, которое сколото с части поверхности подложки (см. рис. 3, 1,2 ряд), демонстрируют, что тонкая КФ пленка повторяет морфологию подложки, изменяя её микрошероховатость
(см. рис. 3 — 3,4 ряд и табл. 2): при напылении в атмосфере Ar микрошероховатость уменьшается, сглаживаются микровыступы исходной подложки; при напылении в атмосфере смеси газов Ar+O2 микрошероховатость существенно увеличивается, что может быть связано с более интенсивным процессом зародышеобразования пленок в реактивной среде; при напылении в атмосфере O2 микрошероховатость остается неизменной.
а б с



Рисунок 1. Торцевые изображения сколов КФ покрытий, сформированных на Si (100) в атмосфере: Ar (а); Ar+O2 (б); O2 (в); толщина покрытия 1,6-0,1 мкм
а б с






Рисунок 2. Внешний вид (1 ряд) и морфология КФ покрытий (2 ряд), сформированных на Si в атмосфере: Ar (а); Ar+O2 (б); O2 (в)
Аr Ar+O2 O2


↓увеличение ↓увеличение ↓увеличение






3D 3D 3D
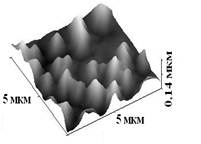


Рисунок 3. Внешний вид и морфология КФ покрытий (толщина 1,6-0,1 мкм), полученных в различных режимах на 12Х18Н10Т: в первом ряду КФ покрытия (нижняя половина рисунка) и поверхность стали, с которой скололи покрытие; во втором ряду КФ покрытия при большем увеличении; в третьем ряду морфология, в четвертом ряду трехмерное изображение КФ покрытий
Таблица 2.
Шероховатость образцов
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
Проведенные исследования показали, что морфология КФ покрытий, сформированных методом ВЧ магнетронного распыления, существенным образом зависит от состава рабочего газа. Для получения на поверхности имплантатов ВЧ магнетронных КФ покрытий с наибольшей микрошероховатостью, необходимой для прикрепления и пролиферации остеогенных клеток, рекомендуется использовать смесь рабочих газов аргона и кислорода в пропорции 1:1 при суммарном давлении 0,3 Па.
Авторы выражают благодарность Шестерикову Евгению Викторовичу за нанесение покрытий и помощь при проведении исследований.
Список литературы:
1.Васильев М.А., Беда В.И., Гурин П.А. Физиологический отклик на состояние поверхности металлических дентальных имплантатов. — Львов: ГалДент, 2010. — 118 c.
2.ГОСТ 9.407-84. Покрытия лакокрасочные. Метод оценки внешнего вида. — Введ 1985-01-07. — М.: Стандартинформ, 1985. — 8 с.
3.Орловский В.П., Суханова Г.Е., Ежова Ж.А., Родичева Г.В. Гидроксилапатитная биокерамика // Ж. неорганической химии. — 1991. — т. 36. — № 6. — C. 683—689.
4.Davies J.E. Mechanisms of Endosseous Integration // Int. J. Prosthodont. 1998. Vol. 11. P. 391—401.
5.Davies J.E: Mechanisms of endosseous integration. Int J Prosthodont 1998: 11(5) 391-401, Gehrke P, Neugebauer J: Implant surface design: Using biotechnology to enhance osteointegration. Dent Implantol Update 2003. — 14(8). — P. 57—64.
6.Schwartz Z., Boyan B.D.: Underlying mechanisms at the bone-biomaterial interface. J Cell Biochem 1994; 56(3): 340-347, Kieswetter K, Schwartz Z, Dean D.D., Boyan B.D.: The role of implant surface characteristics in the healing of bone. Critical Revues in Oral Biology and Medicine. — 1996. — № 7. — P. 329—345.
отправлен участнику

