Статья опубликована в рамках: XXX Международной научно-практической конференции «Научное сообщество студентов XXI столетия. ЕСТЕСТВЕННЫЕ НАУКИ» (Россия, г. Новосибирск, 07 апреля 2015 г.)
Наука: Медицина
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
СОЗДАНИЕ ЗАПИРАТЕЛЬНОГО АППАРАТА НИЖНЕГО СЕГМЕНТА МАТКИ У БОЛЬНЫХ ИНВАЗИВНЫМ РАКОМ ШЕЙКИ МАТКИ ПОСЛЕ РАДИКАЛЬНОЙ ТРАНСАБДОМИНАЛЬНОЙ ТРАХЕЛЭКТОМИИ
Разаева Нургуль Абдижалиловна
студент, лечебный факультет, СибГМУ, РФ, г. Томск
E-mail:
Чернышова Алена Леонидовна
научный руководитель, д-р мед. наук, ведущий научный сотрудник отделения гинекологии ФГБНУ «Томский НИИ онкологии», РФ, г. Томск
Введение. Рак шейки матки занимает второе место в структуре онкогинекологической патологии, а в возрастной категории от 15 до 54 лет является доминирующей локализацией, при этом в последние годы наблюдается негативная тенденция — рост заболеваемости женщин репродуктивного возраста, с ежегодным приростом на 2—7 %. В настоящее время активно развиваются новые медицинские технологии в лечении РШМ. Становится очевидным, что при начальных стадиях опухолевого процесса радикальность расширенных операций значительно превосходит необходимую. В настоящее время активно разрабатываются органосохраняющие медицинские технологии лечения РШМ у женщин детородного возраста, что является приоритетным направлением клинической онкологии [1; 2; 8]. В частности, при лечении больных РШМ IA2–IB2 стадий (FIGO) стали применяться операции в объеме радикальной трансабдоминальной трахелэктомии. Доказана онкологическая эффективность подобных операций, имеются сообщения об успешном наступлении беременности и родов после их проведения [3; 10].
Одним из актуальных и нерешенных вопросов является необходимость укрепления нижнего сегмента матки и формирование «запирательного» аппарата для вынашивания последующей беременности в условиях отсутствия шейки матки. Недостаточность запирательной функции перешейка матки (истмико-цервикальная недостаточность) может привести к механическому опусканию и пролабированию плодного пузыря, что создает условия для его инфицирования. Кроме того, возможно внедрение плодного пузыря в зону анастомоза, что способствует как дальнейшему его расширению и нарастанию угрозы прерывания беременности, так и развитию несостоятельности маточно-влагалищного анастомоза. В настоящее время на начальных сроках беременности у здоровых женщин в случае развития истмико-цервикальной недостаточности общепринятым является метод наложения циркляжа на шейку матки. Разумеется, в случае экстирпации шейки матки данная операция во всех модификациях неосуществима. Для категории больных раком шейки матки после проведения радикальной трахелэктомии циркляж в области нижнего сегмента матки накладывают обычно в период с 8-й до 17-й недели беременности. Вместе с тем, активно обсуждается возможность профилактики несостоятельности маточно-влагалищного анастомоза в раннем и позднем послеоперационном периоде, а также непосредственно во время операции. Однако, известные способы наложения циркляжа в зоне нижнего сегмента матки с использованием в качестве шовного материала лавсана, шелка, капрона, хромированного кетгута нельзя признать достаточно эффективными.
Применение любого из вышеперечисленных материалов, так или иначе, создает дополнительные условия для инфицирования и соответственно требует назначения антибактериальной терапии. При этом необходимо учитывать возможность неблагоприятного воздействия лекарственных (антибактериальных) средств на плод. К наиболее частым осложнениям в результате оперативного лечения истмико-цервикальной недостаточности после трахелэктомии с наложением швов относятся: прорезывание тканей зоны анастомоза, образование пролежней с дальнейшим формированием свищей, а также поперечные или круговые разрывы [9].
В доступной литературе отсутствуют источники, где были бы представлены достаточно эффективные варианты укрепления нижнего сегмента матки с целью формирования запирательного аппарата матки непосредственно во время радикальной абдоминальной трахелэктомии. Целью нашего исследования явилось — разработка способа формирования запирательного аппарата матки у больных раком шейки матки после радикальной абдоминальной трахелэктомии.
Материал и методы исследования. В исследование вошли 26 больных раком шейки матки I стадии, находившихся в репродуктивном возрасте, получивших лечение в объеме радикальной трансабдоминальной трахелэктомии в отделении онкогинекологии ФГБУ «НИИ онкологии» с 2012 по 2014г. Больные раком шейки матки I стадии были разделены на следующие подстадии: Iа1 стадия — 7 больных (27 %); Iа2 — 8 (31 %); Ib1 — 11 пациенток (42 %). Морфологически у всех пациенток, включенных в исследование, был плоскоклеточный неороговевающий рак различной степени дифференцировки. Средний возраст больных составил 28,7±4,5 лет.
В ходе проведения оперативного лечения в объеме радикальной абдоминальной трахелэктомии после наложения маточно-влагалищного анастомоза проводилось укрепление нижнего сегмента матки с помощью сетки из сверхэластичной нити никелида титана (рис. 1а,б), проводилась установка и фиксация сетки из никелида титана с моделированием ее по месту установки в границах от нижнего сегмента матки до верхней трети влагалища (рис. 2 а,б). Фиксацию сетки проводили четырьмя отдельными швами по периметру.
А) Б)
Б)
Рисунок 1. (а,б). Сверхэластичный сетчатый имплантат из никелида титана
А)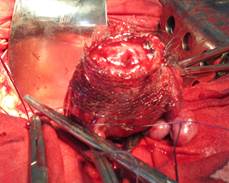 Б)
Б)
Рисунок 2. а. Вид операционной раны: фиксация сетчатого имплантата вокруг нижнего сегмента матки. б. Окончательный вид операционной раны
Размеры сетки из никелида титана (марка ТН-1): ширина 4—5 см, длина 7—8 см, диаметр нити 0,1—0,08 мм, размеры ячейки сетки 3—5 мм. Длина сетчатого имплантата в пределах 5—7 см, что соответствует анатомии дефекта и позволяет сделать не менее одного полного оборота вокруг анастомоза с небольшим перекрытием.
Этапы операции показаны на рис. 3. После удаления дистальной части шейки матки и верхней трети влагалища (рис. 3а) между ними формируют анастомоз путем прошивания непрерывной нитью по периметру, после чего его обматывают сетчатым имплантатом (рис. 3б, с). Сетчатый имплантат сплетен в виде чулка шириной 4—5 см из сверхэластичной никелид-титановой нити диаметром 0,08—0,1 мм с размером ячеек от 3 до 5 мм. Длина имплантата составляет 7—8 см. Фиксацию имплантата с целью первичной иммобилизации производили четырьмя отдельными швами по периметру.
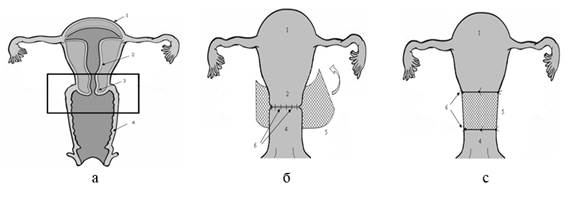
Рисунок 3. а — схематически изображена область операционной зоны при органосохраняющем лечении инвазивного рака шейки матки; б — схематически изображена зона наложения и фиксации имплантата; с — схематически изображена операционная рана после фиксации имплантата. Цифрами обозначены: 1 — тело матки, 2 — цервикальный канал, 3 — шейка, 4 — влагалище, 5 — сетчатый имплантат. 6 — швы
Предлагаемый способ был разработан и апробирован в гинекологическом отделении ФГБУ «НИИ онкологии» СО РАМН (положительное решение о выдаче патента от 5.03.2014 г.).
Динамическое наблюдение за данной категорией больных в послеоперационном периоде проводилось с помощью ультразвукового мониторинга органов малого таза. Кроме того, в послеоперационном периоде проводилась оценка состояния нижнего сегмента матки и зоны анастомоза методом обзорной рентгенографии.
Обсуждение результатов исследования. Сверхэластичные сетчатые имплантаты из никелида титана в настоящее время находят широкое применение в медицинской практике, в том числе и у онкологических больных. Достижения в технологии изготовления тонких нитей из сверхэластичного никелида титана позволяют изготавливать из них сетчатые структуры, приближающиеся по эластичности к традиционным шовным и перевязочным материалам. Вместе с тем, имплантаты из никелид-титановой нити обладают рекордной биосовместимостью и вживляемостью, что снимает вопрос об их последующем удалении, как это требуется при использовании традиционных материалов [10].
Целесообразность использования сетчатого имплантата из сверхэластичного никелида титана обусловлена его биомеханическими свойствами: он не рассасывается, срастается с окружающими тканями и обеспечивает устойчивость тканей к избыточной деформации. Применительно к проблеме укрепления маточно-влагалищного анастомоза имплантат берет на себя основную функцию «запирательного» аппарата матки и обеспечивает функциональную опору и устойчивость маточно-влагалищного анастомоза к воздействию внутриматочного и внутрибрюшинного давления. Имея развитую поверхность, сетка несет основную нагрузку, равномерно распределяет ее по площади анастомоза, исключает возможность локальной концентрации усилий и связанных с ними разрывов или пролежней и свищей.
Важным моментом является способность сетки из сверхэластичной нити никелида титана повторять форму любой поверхности без предварительной деформации, что применительно к решаемой проблеме позволяет зафиксировать маточно-влагалищный анастомоз непосредственно в ходе операции, обеспечивая необходимый «запирательный» эффект. Сетка из нити никелида титана с эффектом сверхэластичности участвует во всех деформационных процессах окружающих ее тканей, так как способна многократно возвращаться в исходное состояние, обеспечивая пластичность и надежную прочность сформированного анастомоза, что важно с учетом планируемой беременности у данной категории больных. При этом сетчатый имплантат не мешает срастаться прилегающим друг к другу матке и пузырно-влагалищной фасции.
Выбор толщины нити в пределах 0,08—0,1 мм обусловлен, с одной стороны, достигнутыми на данный момент технологическими возможностями изготовления тонких нитей — порядка 0,08 мм, с другой стороны — необходимостью обеспечения достаточной эластичности сетчатой структуры. При диаметре нити более 0,1 мм эластичность имплантата признается недостаточной. Развитие технологии получения никелид-титановой нити позволяет прогнозировать переход на более тонкие нити [10].
Размеры ячейки в пределах 3—5 мм обусловлены, с одной стороны, возможностью переплетения нити, обладающей конечной эластичностью, с другой стороны — возможностью предотвращения пролабирования тканей в просветы сетки. Ширина сетчатого имплантата в пределах 4—5 см соответствует анатомии дефекта, обеспечивая покрытие тканей по обе стороны анастомоза. Плетение имплантата в виде чулка обеспечивает отсутствие травмирующих торчащих концов металлических нитей, и кроме того возможность адаптации чулка по ширине соответственно конфигурации дефекта. Длина сетчатого имплантата в пределах 5—7 см соответствует анатомии дефекта, позволяя сделать не менее одного полного оборота вокруг анастомоза с небольшим перекрытием. Наложение сетчатой структуры, облегающей зону анастомоза, обеспечивает непосредственно в момент операции перенос напряжений с швов на имплантат, что в значительной степени снимает вероятность негативных последствий. Фиксация имплантата поверхностными швами не связана с созданием травмирующих проколов и создает минимальные усилия, поскольку лишь иммобилизует имплантат на ближайший момент, предотвращая его соскальзывание.
Кроме того, важным моментом ведения данной категории больных является динамическое наблюдение в послеоперационном периоде с оценкой анатомической и функциональной состоятельности анастомоза. В этом плане использование сетки из сверхэластичного никелида титана достаточно оправдано, так как не создает препятствий для ультразвукового мониторинга в различные периоды динамического наблюдения за больными. Кроме того, с учетом рентгеноконтрастности данного материала возможно проведение обзорной рентгенографии с целью оценки состояния анастомоза.
Таким образом, в настоящее время органосохраняющее лечение в объеме радикальной абдоминальной трахелэктомии занимает достойное место среди хирургических вмешательств, выполняемых в современной онкогинекологии. Перспективным направлением исследований является оценка онкологической эффективности и анализ отдаленных результатов после проведенных радикальных трахелэктомий различных модификаций, разработка реабилитационных мероприятий, включающих психологические, физиотерапевтические, лекарственные аспекты. Большой интерес представляют исследования, посвященные оценке особенностей фертильности, течения беременности, перинатальных исходов, а также качества жизни больных после проведенного органосохраняющего лечения.
Список литературы:
1.Адамян Л.В., Жордания К.И., Белобородов С.М. Репродуктивная функция у онкологических больных. Как сохранить возможность иметь детей //Вопросы онкологии. — 2004. — № 503. — С. 279—292.
2.Антипов В.А., Е.Г. Новикова, О.С. Балахонцева, А.С. Шевчук. Особенности функциональной и анатомической реабилитации после радикальной абдоминальной трахелэктомии // Проблемы репродукции. — 2010. — № 1. — С. 103—107.
3.Антипов В.А., Е.Г. Новикова, О.С. Балахонцева, А.С. Шевчук. Радикальная абдоминальная трахелэктомия: технические аспекты // Вопросы онкологии. —2010. — Том 56. — № 1. — С. 36—42.
4.Чойнзонов Е.Л., Писарева Л.Ф., Жуйкова Л. Д. Злокачественные новообразования в Томской области в 2004—2009 гг. Оценка качества диагностики. // Сибирский онкологический журнал. — 2011. — № 3. — С. 29—34.
5.Dargent D. Radical trachelectomy: an operation that preserves the fertility of young women with invasive cervicalcancer // Bull. Acad. Natl. Med. 2001. Vol.185(7). — P. 1295—304.
6.Dargent D. Using radical trachelectomy to preserve fertility in early invasive cervical cancer // Contemporary OB/GYN 2000. May. — P. 23—49.
7.Karam A., Feldman N., Holschneider C.H. Neoadjuvant cisplatin and radical cesarean hysterectomy for cervical cancer in pregnancy // Nat. Clin. Pract. Oncol. — 2007. — Vol. 4. — P. 375—380.
8.Palaia I., Pernice M., Graziano M. Neoadjuvant chemotherapy plus radical surgery in locally advanced cervical cancer during pregnancy: a case report // Am. J. Obstet. Gynecol. — 2007. — Vol. 197. — P. e5—e6.
9.Salafia CM, Minior VK, Lopez-Zeno JA, Whittington SS, Pezzullo JC, Vintzileos AM. Relationship between placental histo Int.J. Med. Sci. 2010. 20:67-71.
10.Ungar L. Update on radical abdominal trachelectomy. Abstracts of International Video Workshop on radical surgery in gynecological oncology. Prague 2008. — Р. 15—19.
дипломов

