Статья опубликована в рамках: XIII Международной научно-практической конференции «Научное сообщество студентов XXI столетия. ЕСТЕСТВЕННЫЕ НАУКИ» (Россия, г. Новосибирск, 07 ноября 2013 г.)
Наука: Медицина
Секция: Фармакология, Фармация.
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
отправлен участнику
РАЗРАБОТКА ОПТИМАЛЬНОГО МЕТОДА ПОЛУЧЕНИЯ 5,7-ДИХЛОР-4,6-ДИНИТРОБЕНЗОФУРОКСАНА С КОНТРОЛЕМ КАЧЕСТВА ИСХОДНОГО СЫРЬЯ И ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ СИНТЕЗА
Хузиахметова Алсу Нафисовна
аспирант, кафедра Химии и технологии органических соединений азота КНИТУ, г. Казань
Бикмухаметова Зиля Нафисовна
студент 4курса, кафедра Химии и технологии органических соединений азота КНИТУ, г. Казань
E-mail:
Юсупова Луиза Магдануровна
научный руководитель, профессор, д-р хим. наук, кафедра Химии и технологии органических соединений азота КНИТУ, г. Казань
Лекарственный препарат «Димиксан», компонентами которого являются 5,7-дихлор-4,6-динитробензофуроксан (ДХДНБФО) и 4,6-дихлор-5-нитробензофуроксан, был разработан сотрудниками кафедры ХТОСА КНИТУ. Препарат является эффективным для лечения паразитарных, вирусных, грибковых заболеваний [1].
«Димиксан» прошел все этапы доклинических испытаний, в результате которых было установлена его безвредность (LD50 5000 мг/кг живого веса, III класс опасности). Данный препарат является высокоэффективным для лечения паразитарных заболеваний. Установлена лечебная доза для лечения демодекоза 0,1—0,5 %-ной концентрации, грибковых заболеваний от 0,05 до 0,1 %-ной концентрации препарата [3].
Для внедрения препарата в лечебную практику необходимо было разработать научно-техническую документацию и рабочий стандартный образец с постоянным химическим составом и содержанием основного вещества не менее 99,5 %, что и являлось нашей основной целью.
Для решения указанной цели были поставлены следующие задачи:
1. Постадийное исследование синтеза 5,7-дихлор-4,6-динитробензофурок-сана. Выявление возможных побочных продуктов и примесей на каждой стадии синтеза.
2. Контроль качества сырья, промежуточных продуктов синтеза и конечного продукта — ДХДНБФО с применением высокочувствительных физико-химических методов: хроматография, инфракрасная спектроскопия (ИК-спектр), методы дифференциально-сканирующего (ДСК) и термогравиметрического (ТГА) анализов.
3. Разработка рабочего стандартного образца 5,7-дихлор-4,6-динитробен-зофуроксана.
Были проведены ряд параллельных опытов с использованием очищенных от примесей, методом кристаллизации, начальных и промежуточных продуктов реакции, а так же с непосредственно полученными в ходе реакций промежуточными продуктами синтеза. На каждом этапе контролировали выход и температуру плавления продукта реакции. Одновременно производили контроль возможных побочных продуктов и примесей методом ТСХ.
ИК-спектры проб снимались на спектрофотометре ИК-спектрометре UR-20 (Германия) в интервале 400—4000 см-1 при комнатной температуре. Крис-таллические образцы исследовались в виде таблетки с порошком КBr.
Жидкостную хроматографию проводили на хроматографе с насосом высокого давления High pressure pump 5001 (HPP 5001) (Чехия). Рабочее давление насоса составило 8,5 МПа, температура термостата +20 0С, ультрафиолетовый детектор в 254 нм длины волны, сорбент в колонке — сепарон GXC, 7 мкм., подвижная фаза — ИПС.
Для элементного анализа применялся прибор элементный анализатор EuroVector EA3000 (Италия). Температура сжигания 1100 0С, газ-носитель — гелий.
Анализ ДСК (ТГА-ДТА) проводили на системе термического анализа
METTLER TOLEDO (Швейцария) в интервале температур от 25 до 150 0С в атмосфере воздуха, скорость протекавшего воздуха через прибор составил 15 см3/мин. Скорость нагрева — 10 0/мин.
Температуру плавления продуктов реакций отмеряли на сернокислотном блоке.
Полноту протекания реакций контролировали методом ТСХ на пластинках Sorbfil (Россия) в среде гексан-хлороформ (8:2).
С целью получения рабочего стандартного образца первоначально необходимо было воспроизвести синтез ДХДНБФО с постадийным контролем выхода и температуры плавления, по схеме:
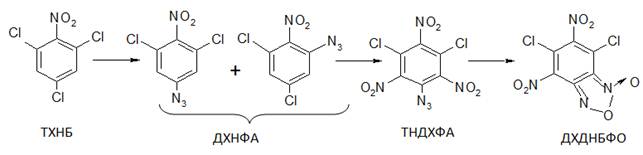
Схема 1. Синтез ДХДНБФО
Ранее синтез 5,7-дихлор-4,6-динитробензофуроксана осуществлялся из 2,4,6-трихрлоранилина (ТХА):
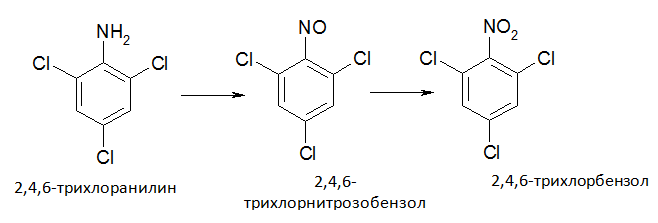
Схема 2. Получение исходного сырья ТХНБ из ТХА, используемого для синтеза ДХДНБФО
Но как показывают результаты данного эксперимента, конечный продукт получается загрязненным различными примесями и побочными продуктами, что крайне недопустимо в синтезе лекарственных препаратов. В связи с этим явлением, впервые нами в качестве исходного сырья для синтеза ДХДНБФО был взят 1,3,5-трихлорбензол (ТХБ):
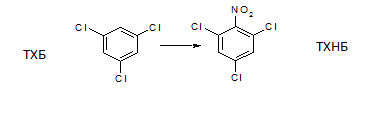
Схема 3. Получение исходного сырья ТХНБ из ТХБ, используемого для синтеза ДХДНБФО
Контроль качества исходного вещества ТХБ осуществлялся методами хроматографии, ИК-спектроскопия, методы ДСК-ТГА и определением температуры плавления: Тпл.=59—64 0С; ИК-спектр, см-1(рис.1): 1625(бензольное кольцо), 717,17(С-Сl), 664,85(Сарен-Н). Анализ ДСК-ТГА показал Тпл=58,66—64,03 0С при «размытой» вершине пика, убыль массы на 94,05 % при 95,88 0С-ном нагревании. Предположили, что большая убыль массы происходит из-за термической нестабильности ТХБ.
Рисунок 1. ИК-спектр ТХБ-сырца
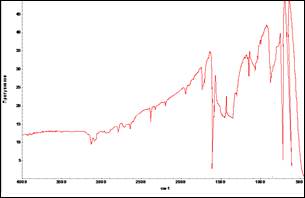
Рисунок 2. ИК-спектр ТХБ-чистого
ТХБ (кристаллизация из этилового спирта).: Тпл.=63,5—64,5 0С; ИК-спектр, см-1(рис.2): 1640(бензольное кольцо), 749,86(С-Сl), 661,58(Сарен-Н); на хроматограмме 1 пик. Тпл=64,05—64,15 0С по ДСК с острой вершиной пика, убыль массы при 92,17 0С на 91,92 % по ТГА.
Исследование нитрования ТХБ до 2,4,6-трихлорнитробензола (ТХНБ) показало, что образование побочных продуктов не наблюдается, в качестве примеси методом ТСХ был идентифицирован недонитрованный исходный ТНБ. Выход 56 %. ТХНБ-сырец очищали кристаллизацией из изопропилового спирта. После однократной перекристаллизации достигали Тпл.=69,5—70,5 0С; ИК-спектр, см-1(рис. 3): 1640(бензольное кольцо), 723,71(С-Сl), 680(Сарен-Н), 1541,14(NO2); на хроматограмме 1 пик. ДСК определил Тпл=68,73—68,95 0С с острой вершиной пика, по ТГА убыль массы на 49,25 % при 128,85 0С.
После оптимизации реакции нитрования ТХБ присутствие в целевом продукте исходного продукта не обнаружили. ТХНБ: Тпл.= 69,5—70,5 0С; ИК-спектр, см-1(рис. 4): 1670 (бензольное кольцо), 723,71(С-Сl), 640(Сарен-Н), 1530(NO2); на хроматограмме 1 пик. Анализ ДСК-ТГА выявил Тпл=69,81—69,96 0С, острая вершина пика, убыль массы на 48,17 % при 128,53 0С-ном нагревании. Выход 90 %.
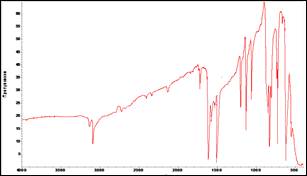
Рисунок 3. ИК-спектр ТХНБ-сырца
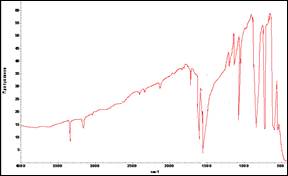
Рисунок 4. ИК-спектр ТХНБ-чистого
Стадия азидирование ТХНБ — взаимодействие 2,4,6-трихлорнитробензола с азидом натрия в присутствии растворителя ДМФА — является одной из важной стадии в синтезе ДХДНБФО. Выход азидодихлоронитробензолов — 2-азидо-4,6-дихлоро- и 4-азидо-2,6-дихлоронитробензолов и появление возможных примесей зависит от количества взятой для реакции азида натрия: возможно присутствие в продукте реакции исходного ТХНБ при недостатке азида, а при 10%-ом избытке азида натрия образуется побочный продукт – диазидодихлорнитробензол. При 5 %-ом избытке азида побочные продукты не образуются. ДХНФА: Тпл.=68—69 0С; ИК-спектр, см-1(рис. 5): 1640(бензольное кольцо), 717,17(С-Сl), 680(Сарен-Н), 1565(NO2) 2126,43(N3); на хроматограмме было обнаружено 3 пика — один пик был идентифицирован как исходный ТХНБ, а остальные как два изомера: 2-азидо-4,6-дихлоро- и 4-азидо-2,6-дихлоронитробензол. Анализ ДСК-ТГА выявил Тпл=65,3—68,06 0С, при котором наблюдается «размытость» пика; убыль массы при нагревании в 130,74 0С на 21,8 %. Выход 74 %. После однократной перекристаллизации ДХНФА из этилового спирта.: Тпл.=69—70 0С; ИК-спектр, см-1(рис. 6): 1600 (бензольное кольцо), 2126,43(N3); 723,71(С-Сl), 675(Сарен-Н), 1534(NO2) на хроматограмме 1 пик. Анализ ДТА показал Тпл=69,06—69,92 0С с выраженной остротой пика. По ТГА выявили убыль массы при Т=129,79 0С на 30,48 %. Скорее всего, убыль массы происходит вследствие разложения или циклизации одного из изомеров, а именно 2-азидо-4,6-дихлоронитробензола. Выход 60 %.
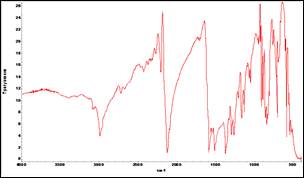
Рисунок 5. ИК-спектр ДХНФА-сырца
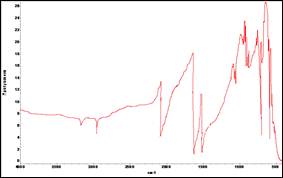
Рисунок 6. ИК-спектр ДХНФА-чистого
В ходе экпериментов убедились, что методом многократной кристаллизации возможно регулировать соотношение изомеров в смеси (содержание изомеров 4-азидо-2,6-дихлоро- и 2-азидо-4,6-дихлоронитробензолов в полученной смеси из ТХНБ составило 22,64 % и 77,36 % соответственно, при однократной кристаллизации ДХНФА содержание 4-азидо-2,6-дихлоро- и 2-азидо-4,6-дихлоронитробензолов составил 30,48 % и 69,52 % соответственно, а при двукратной кристаллизации — 40,75 % и 59,25 % соответственно). Таким образом, предоставляется возможность полного разделения данных соединений.
Результирующей стадией является стадия нитрования ДХНФА до 4,6-дихлоро-1,3,5-тринитрофенилазида (ТНДХФА). Изучение стадии нитрования в ранних работах [2] дихлоронитрофенилазида концентрированной кислотной смесью (H2SO4+HNO3) показало, что совместно с целевым продуктом 4,6-дихлоро-1,3,5-тринитрофенилазидом возможно образование 4,6-дихлоро-1,3-динитрофенилазид, что так же нежелательно в нашем синтезе.
ТНДХФА-сырец имеет Тпл.=92—93 0С; ИК-спектр, см-1(рис. 7): 1650 (бензольное кольцо), 726,98(С-Сl), 1544,41(NO2), 2152,59(N3); на хроматограмме 2 пика, один из которых идентифицирован как недонитрованный исходный ДХНФА. Элементный состав вычислено: С=24,74 %, N=19,24 %; найдено: С=24,77 %, N=19,3 %, а так же указывает на наличие атомов водорода (Н=0,78%) в полученном соединении, что говорит о наличии примеси в конечном продукте реакции. Характерным для ИК-спектрограммы ТНДХФА должно являться полное отсутствие пиков атомов водорода, чего мы не наблюдаем. Выход составил количественно 89 %. Анализы ДСК-ТГА- Тпл=90,08—94,95 0С, пик «размытый»; убыль массы составила 6,64% при нагревании в 133,75 0С. Выход 89 %.
После однократной перекристаллизации ТНДХФА (кристаллизация из изопропилового спирта).: Тпл.=103—104 0С; ИК-спектр, см-1(рис. 8): 1630(бензольное кольцо), 730(С-Сl), 1544,41(NO2), 2155,86(N3), на хроматограмме 2 пика. Двухкратная перекристаллизация позволила получить более чистый ТНДХФА: Тпл.=105—106 0С; ИК-спектр, см-1(): 1620(бензольное кольцо), 730,25(С-Сl), 1530(NO2), 2142,78(N3); на хроматограмме 1 пик. Тпл=104,97—105,84 0С с острым пиком (ДСК), по анализу ТГА наблюдается убыль массы на 5,95 % при 132,36 0С-ном нагревании. Это объясняется потерей азота при нагревании за счет циклизации ТНДХФА и образования ДХДНБФО, который при дальнейшем нагревании плавится. С этим и связан эндоэффект при данной температуре.
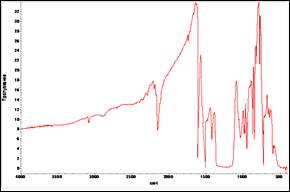
Рисунок 7. ИК-спектр ТНДХФА-сырца
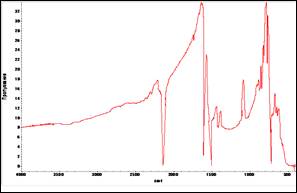
Рисунок 8. ИК-спектр ТНДХФА-чистого
Циклизация ТНДХФА до ДХДНБФО протекает количественно с выходом 95 %. ДХДНБФО-сырец имеет: Тпл.=125—127 0С; ИК-спектр, см-1(рис. 9): 1630 (С=N→O), 730,25(С-Сl), 1550,95(NO2), 1132,43(N→O); на хроматограмме 1 пика. После двухкратной перекристаллизации ДХДНБФО (кристаллизация из гексана и хлороформа в соотношении 1:6 соответственно): Тпл.=130—131,5 0С; ИК-спектр, см-1: 1630(С=N→O), 740(С-Сl), 1556(NO2), 1201,09(N→O), на хроматограмме 1 пик. Анализ ДСК (ТГА, ДТА) определил Тпл=127—127,85 0С, пик острый; увеличение массы на 3,18 % при нагревании в 53,66 0С, а при достижении 134,02 0С наблюдается убыль массы на 2,087 %.
Перекристаллизацию ДХДНБФО осуществили в смеси двух растворителей: хлороформа и гексана, в соотношении 1:6 соответственно. Тпл.=130—131,50С; ИК-спектр, см-1(рис. 10): 1630(С=N→O), 740(С-Сl), 1556(NO2), 1201,09(N→O), на хроматограмме 1 пик. Вычисленный элементный анализ полностью соответствует найденному. Анализ ДСК-ТГА- Тпл=130,08—130,96 0С (пик острый); при 59,3 0С — увеличение массы на 3,8 %, при достижении температуры в 134,84 0С — убыль массы на 0,69 % в следствие улетучивания растворителя.
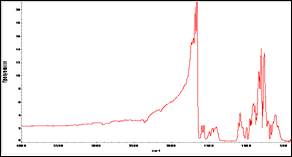
Рисунок 9. ИК-спектр ДХДНБФО-сырца
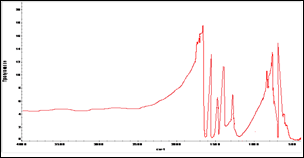
Рисунок 10. ИК-спектр ДХДНБФО-чистого
Таким образом, мы получили аналитический образец целевого продукта — ДХДНБФО с содержанием основного вещества не менее 99,5 % согласно элементному анализу, а так же пришли к выводу, что очистка начального сырца и промежуточных продуктов, а так же соблюдение оптимальных условий синтеза обеспечивает получение ДХДНБФО — одного из компонентов «Димиксан»а высокой степени чистоты, что является крайне необходимым требованием для разработки проекта фармстатьи на одну из субстанцию данного высокоэффективного ветеринарного препарата «Димиксан».
Список литературы:
1.Горелова Е.Г. Нитропроизводные дихлорбензофуроксанов и их акари-цидные составы в водных средах: Автореф. дис. на соиск. уч. степ. канд. хим. наук. Казань, 2009 г. — 2 с.
2.Спатлова Л.В. Синтез и свойства 5,7-дизамещенных-4,6-динитробензо-фуроксана: Автореф. дис. на соиск. уч. степ. канд. хим. наук. Казань, 2003 г. — с. 7—100.
3.Юсупова Л.М., Гармонов С.Ю., Захаров И.М. Средства биологической защиты многоцелевого назначения на основе хлорпроизводных нитробензофуроксана // Вестник Казанского технологического университета. — 2005. — № 1. — С. 103—111.
отправлен участнику

