Статья опубликована в рамках: X Международной научно-практической конференции «Научное сообщество студентов XXI столетия. ЕСТЕСТВЕННЫЕ НАУКИ» (Россия, г. Новосибирск, 06 мая 2013 г.)
Наука: Химия
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
ИЗУЧЕНИЕ СОРБЦИИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ ГЕТЕРОПОЛИКИСЛОТАМИ СТРУКТУРЫ КЕГГИНА
Тюлюш Шончалай Алексеевна
студент 4 курса, кафедра химии ХГУ им. Н.Ф. Катанова, г. Абакан
E-mail: tyulyush_88@mail.ru
Сердюков Данил Сергеевич
студент 4 курса, кафедра химии ХГУ им. Н.Ф. Катанова, г. Абакан
E-mail: Aszx12311@rambler.ru
Фисун Любовь Александровна
научный руководитель, канд. хим.х наук, доцент кафедры химии ХГУ им. Н.Ф. Катанова, г. Абакан
Гетерополисоединения (ГПС) — особая группа комплексных соединений, химия которых представляет собой одну из фундаментальных отраслей в теоретическом плане. Среди различных типов структур ГПС наиболее изученными являются гетерополикислоты (ГПК) и их соли 12-го насыщенного ряда структуры Кеггина, соответствующие общей формуле Аn[XM12O40], где А — катион (Н+, К+, Сs+, Ва2+ и др.); Х — Si, Р; М — Мо,W; n — число катионов, компенсирующих заряд гетерополианиона (ГПА) [3, с. 125].
Интерес к изучению гетерополикислот вызван их широким кругом применения в различных областях науки, техники, медицины, что, несомненно, обусловлено уникальными особенностями строения и многообразия свойств гетерополисоединений [4, с. 73].
ГПК являются сильными многоосновными бренстедовскими кислотами. Они значительно превосходят по силе таких минеральные кислоты, как Н2SO4, HBr, HCl, HNO3, что позволяет создавать на их основе эффективные кислотные катализаторы.
Многие ГПК — довольно сильные окислители, характеризуются высокой активностью и селективностью в качестве катализаторов ряда процессов органического синтеза. При изменении состава ГПК можно в широких пределах варьировать их свойства.
Использование ГПК в гетерогенном катализе органических реакций определяется спецификой их взаимодействия с органическими соединениями.
В данной работе исследована сорбция органических соединений молибденовыми и вольфрамовыми гетерополикислотами с центральным атомом кремния, которые занимают среднее положение в ряду ГПК как по окислительной активности, так и по заряду и радиусу центрального атома, относятся к наиболее типичным и устойчивым кислотам структуры Кеггина [2, с. 1420].
В ходе работы решались следующие задачи:
·исследование характера абсорбции паров органических соединений массивными ГПК;
·установление корреляций между свойствами ГПК и природой органического соединения.
Гетерополикислоты — кремнемолибденовая H4SiMo12О40, кремневольфрамовая H4SiW12O40 марки ч.д.а. перекристаллизовывали из водного раствора. Содержание воды в гидратах гетерополикислот определяли прокаливанием образцов до постоянной массы. Для удаления воды кристаллогидраты ГПК нагревали при температуре 50—1000С в течение 2 часов.
Для изучения сорбционных свойств гетерополикислот использовали органические растворители, которые отличались по полярности, основности и давлению паров:
1 группа: ацетон (СН3)2СО, изопропиловый спирт (СН3)2СНОН, 1-пентанол С5Н11ОН, изоамиловый спирт (СН3)2СНСН2СН2ОН;
2 группа: этилацетат СН3СООС2Н5, бутилацетат СН3СООС4Н9, диоксан;
3 группа — некислородсодержащие: толуол С6Н5СН3.
Органические растворители марки «ч.д.а» дополнительной очистки не подвергали.
Таблица 1.
Некоторые характеристики органических соединений
|
Органические соединения |
Дипольный момент, Д |
Давление паров, мм.рт.ст. |
|
Толуол |
0,36 |
22 |
|
Диоксан |
1,20 |
15
|
|
Этилацетат |
1,65 |
15 |
|
Бутилацетат |
1,66 |
10
|
|
1-Пентанол |
1,65 |
2 |
|
Изоамиловый спирт |
1,65 |
65 |
|
Изопропиловый спирт |
1,65 |
74 |
|
Ацетон |
2,71 |
185 |
Для оценки сорбционных свойств гетерополикислот бюксы с образцами помещали в эксикаторы с органическими растворителями. Сорбционные измерения проводили при температуре 20оС.
Установление равновесия сорбции определяли по прекращению изменения массы образцов. Тип сорбции твердое тело — газ. Определение состава сольватов проводили гравиметрическим методом.
Спектры поглощения водных и неводных растворов ГПК регистрировали с помощью спектрофотометра UNICO 2800 в области 190—550 нм, рабочая длина кюветы 10 мм.
В ходе работы изучен процесс сорбции органических соединений безводными гетерополикислотами в широком интервале относительных давлений при комнатной температуре. Некоторые кинетические кривые сорбции органических соединений представлены на рисунках 1,2.
Время установления сорбционного равновесия зависит от полярности органического соединения. Так, в случае полярных соединений равновесие устанавливается в течение 3—5 суток, в случае менее полярного соединения — толуола время установления сокращается до 2 суток.
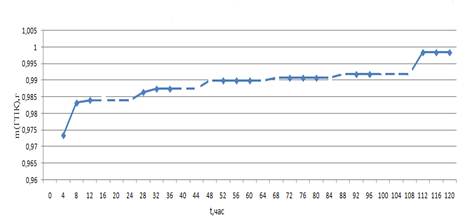
Рисунок 1. Кинетическая кривая сорбции толуола
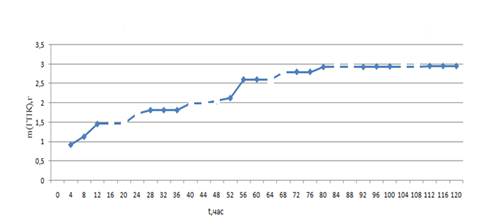
Рисунок 2. Кинетическая кривая сорбции этилацетата
Максимальные значения сорбции паров органических соединений на кремнемолибденовой гетерополикислоте приведены в таблице 2.
Таблица 2.
Максимальные значения сорбции органических соединений (кремнемолибденовая гетерополикислота)
|
Органические соединения |
аmax*103, моль/г |
|
Толуол |
0,3 |
|
Диоксан |
73,0 |
|
Этилацетат |
25,0 |
|
Бутилацетат |
4,3 |
|
Пентанол - 1 |
17,4 |
|
Изоамиловый спирт |
42,0 |
|
Изопропиловый спирт |
150,0 |
|
Ацетон |
60,0 |
Согласно [6, с. 2620] вероятной причиной активного «встраивания» полярных молекул органических соединений в кристаллическую решетку ГПК является их сродство к протонам ГПК, а именно взаимодействие протонов ГПК с О-центрами молекул спиртов, сложных и простых эфиров, кетонов.
Низкое значение величины сорбции толуола обусловлено, по-видимому, отсутствием такого центра в составе его молекулы.
Сорбция полярных соединений, в отличие от толуола, сопровождается явлением ожижения, возможно, взаимодействие протонов ГПК с органическими соединениями происходит как на поверхности, так и в объеме твердой ГПК [1, с. 2229].
Последовательность сорбатов в ряду абсорбционной активности по отношению к кремнемолибденовой гетерополикислоте можно представить следующим образом: вторичные спирты > простые эфиры > кетоны > первичные спирты > сложные эфиры > ароматические углеводороды.
Величина сорбции органических соединений незначительно зависит от состава ГПК; так, замена атомов лиганда молибдена на атомы вольфрама в гетерополианионе сопровождается увеличением величины сорбции (например, бутилацетата), что согласуется с большей кислотностью кремневольфрамовой кислоты [2, с. 1421].
Согласно полученным результатам сорбционные свойства ГПК зависят от от полярности, основности и давления паров органических соединений, однако четкой зависимости сорбции от указанных характеристик не выявлено.
О возможном взаимодействии ГПК с органическими соединениями судили по результатам спектрофотометрических исследований [5, с. 72]. В спектре поглощения кремнемолибденовой гетерополикислоты присутствует интенсивная полоса в области 320 нм. По положению и интенсивности этой полосы поглощения в спектрах судили о взаимодействии ГПК с органическими растворителями.
Результаты исследования представлены в таблице 3, спектр поглощения ГПК в воде и изоамиловом спирте представлен на рисунке 3.
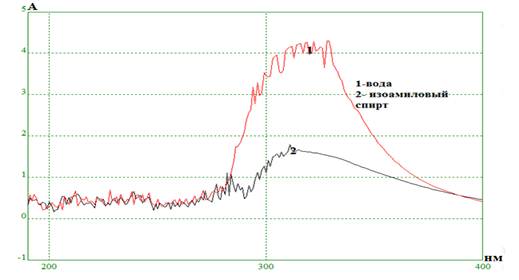
Рисунок 3. Спектр поглощения кремнемолибденовой кислоты в воде (1) и изоамиловом спирте (2)
Таблица 3.
Положение полосы поглощения ГПК в органических соединениях
|
Органические соединения |
λmax, нм |
Интенсивность п.п.,I |
|
Изоамиловый спирт |
312 |
1,8 |
|
Изопропиловый спирт |
313 |
3,8 |
|
Бутилацетат |
318 |
4 |
|
Вода |
320 |
4,1 |
Взаимодействие протонов ГПК с О-центрами молекул спиртов, сложных эфиров приводит к сдвигу полосы поглощения в более коротковолновую область спектра (гипсохромный сдвиг), при этом величина смещения коррелирует с последовательностью сорбатов в ряду абсорбционной активности по отношению к кремнемолибденовой гетерополикислоте.
Отсутствие в спектрах новых полос поглощения и незначительные изменения интенсивности основной полосы указывают на сохранение кеггиновской структуры ГПК в процессах сорбции органических соединений.
На основании полученных результатов можно сделать следующие выводы:
·сорбция органических соединений гетерополикислотами зависит от их полярности и основности;
·последовательность сорбатов в ряду сорбционной активности определятся их сродством к протонам гетерополикислоты.
Список литературы:
1.Дмитриенко С.Г., Гончарова Л.В., Рунов В.К. // Сорбция гетерополикомплексов пенополиурентами. / Журн. физической химии. — 1997. — Т. 71. — № 12. — С. 2227—2231.
2.Кожевников И.В. Успехи в области катализа гетерополикислотами.// Успехи химии. — 1987. — Т. 56. — № 9. — С. 1417—1443.
3.Поп М.С. // Гетерополи- и изополиоксометаллаты. М.: Наука, 1990. — 484 с.
4.Семеновская Е.Н. Применение гетерополикислот в биологии и медицине // Физико-химические основы практического использования изо- и гетерополисоединений. — Днепропетровск. — 1983. — С. 71—75.
5.Спицын В.И., Торченкова Е.А., Казанский Л.П. // Исследоване гетерополисоединений различных типов структур / Итоги науки и техники. Неорганическая химия. — 1984. — Т. 10. — С. 65—140.
6.Чуваев В.Ф., Пинчук И.Н., Плотникова З.М., Спицын В.И. // Поглощение паров кислородсодержащих органических соединений безводными гетрополикислотами молибдена и вольфрама. / Изд. АН СССР. Сер. хим. — 1982. — Т. 6. — № 2. — С. 2620—2622.
дипломов

