Статья опубликована в рамках: IX Международной научно-практической конференции «Научное сообщество студентов XXI столетия. ЕСТЕСТВЕННЫЕ НАУКИ» (Россия, г. Новосибирск, 04 апреля 2013 г.)
Наука: Медицина
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
МОЛЕКУЛЯРНО-ГЕНЕТИЧЕСКИЕ АСПЕКТЫ ВРОЖДЕННЫХ ПОРОКОВ СЕРДЦА
Швецов Ярослав Дмитриевич
аспирант кафедры биологии, медицинской генетики и экологии Курский Государственный Медицинский Университет г. Курск
Email: shvecov.miogu@rambler.ru
Полоников Алексей Валерьевич
научный руководитель, д-р мед. наук, профессор кафедры биологии, медицинской генетики и экологии г. Курск
Врожденные пороки сердца (ВПС) — наиболее распространенный тип врожденных дефектов, затрагивающий 1 % всех новорожденных, и ведущая неинфекционная причина смертности в первый год жизни. Это комплексная мультифакториальная патология, в которой главную роль играют генетические факторы и факторы окружающей среды. Считается, что факторы окружающей среды, воздействующие во время внутриутробного развития, повышают риск развития ВПС: вирусные инфекции, такие как краснуха; воздействие химических тератогенов — ретиноевая кислота, литий, дилантий и галогенизированные углеводороды; заболевания матери, такие как сахарный диабет, системная красная волчанка [1]. Эпидемиологические исследования ВПС продемонстрировали повышенный риск повторных сердечных пороков развития в последующих беременностях, подтверждающие наличие генов предрасположенности. Признавалось, что запутанный процесс сердечного морфогенеза контролируется сетью высоко специфичных генетических и молекулярных путей. Происхождение ВПС разнообразно, причиной могут являться аномальная структура хромосомы (дублирование или удаление), мутации гена, единичные нуклеотидные полиморфизмы, аномальные РНК, эпигенетика и так далее. Ведущие причины развития врожденных пороков сердца представлены на рисунке 1.
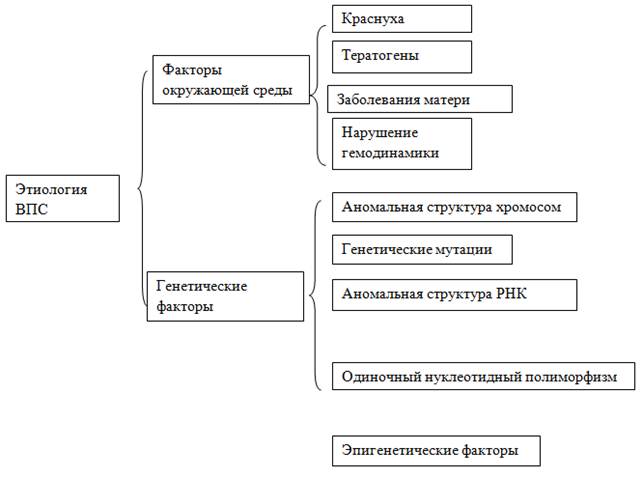
Рисунок 1. Этиология ВПС
В настоящее время выявлены этиологические факторы многих генетических синдромов и семейных ВПС, но генетические основы большинства из «спорадических» врожденных пороков сердца до сих пор остаются неизвестными. С эволюционированием молекулярной генетики и биологии были определены многие гены, связанные с развитием сердца. Установлено, что ряд отдельных врожденных пороков сердца и генетических синдромов, ассоциируется с мутациями в различных единичных генах [2]. Например, NKX2,5 homeobox — содержащие гены играют важную роль в регулировании тканеспецифической экспрессии генов, необходимых для дифференцировки тканей, а также определение временных и пространственных моделей развития. Исследования показали, что в последнее время несиндромные врожденные пороки сердца могут быть результатом дефекта одного гена (Рис. 2).
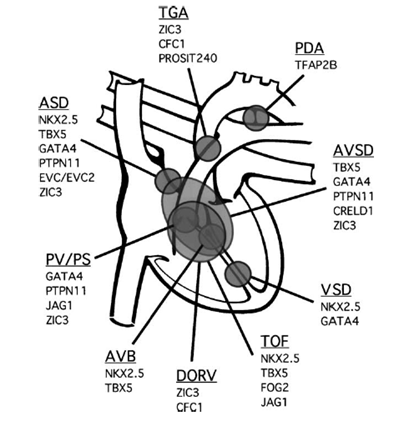
Рисунок 2. Причинные гены, ассоциированные с различными типами врожденных пороков сердца (ASD, дефект межпредсердной перегородки, AVB, атриовентрикулярный блок; AVSD, атриовентрикулярный септальный дефект; DORV, двойной выход сосудов из правого желудочка; PDA, открытый артериальный проток; PV/PS, Дисплазия пульмонального клапана или пульмональный стеноз; TGA, транспозиция магистральных сосудов; TOF, тетрада Фалло; VSD, дефект межжелудочковой перегородки)
Многие причинные гены, ответственные за развитие порока, в настоящее время ассоциированы с ВПС у человека, кодируемые посредством транскрипционных факторов или сигнальных молекул. Транскрипционные факторы являются белками, которые содержат ДНК-связывающие домены и играют фундаментальную регулирующую роль, контролируя экспрессию генов. Сигнальными молекулами являются белки, которые позволяют клеткам реагировать на их окружение и таким образом участвуют в регуляции многих важных биологических функций [3].
У человека, развитие сердца начинается на 15—16 день гестации с миграцией клеток прекардиального стебля, в пять этапов:
1. миграция прекардиальных клеток из первичной полоски и соединение сердечных полумесяцев в миокардиальной пластине;
2. слияние сердечных полумесяцев с целью формирования первичной трубки сердца и создания конечной структуры сердца;
3. сердечное перекручивание и обеспечение надлежащего выравнивания будущих сердечных камер;
4. образование перегородок и формирование камер сердца;
5. развитие проводящей системы сердца и коронарных артерий.
Фенотипы врожденных пороков сердца варьируются от небольших септальных дефектов, которые могут остаться незамеченными на протяжении всей жизни, до больших, которые проявляются значительной симптоматикой. Клинически значимые аномалии в диапазоне от персистенции фетального кровообращение (например, открытый артериальный проток) до сложных дефектов, таких как транспозиция магистральных сосудов, общий желудочек, синдром гипоплазии левых отделов сердца, и сложные варианты гетеротаксии. Существует шесть причинных механизмов в соответствии с патогенетической классификацией врожденных пороков сердечно-сосудистой системы: аномалии миграции эктомезенхимальной ткани (аномалии дуги аорты); дефекты внутрисердечного кровотока (септальные дефекты и левые или правые обструктивные пороки сердца); аномалии, связанные с гибелью клеток (септальные дефекты и аномалии клапанов); аномалии экстрацеллюлярного матрикса (дефекты атриовентрикулярного канала); аномальный рост (частичная или полная мальформация легочного венозного возврата и cor triatriatum) и неправильная позиция и перекручивание, что включает нарушение лево-правой асимметрии [3].
Исходя из вышесказанного, можно сделать вывод, что предрасположенность к ВПС является результатом одиночных нуклеотидных полиморфизмов или ключевых генов, которые при взаимодействии с факторами окружающей среды, нарушают нормальный морфогенез сердца, что приводит к развитию врожденных сердечных аномалий (таблица 1).
Таблица 1.
Генетические причины врожденных пороков сердца (AD, аутосомно-доминантный; ASD, Дефект межпредсердной перегородки; AVB, атриовентрикулярный блок; AVSD, дефект атриовентрикулярной перегородки; DORV, двойной выход сосудов из правого желудочка; HCM, гипертрофическая кардиомиопатия; HOS, Holt –Oram синдром; PDA, открытый артериальный проток; PPS, периферический легочный стеноз; PS, стеноз легочной артерии; PV, дисплазия легочного клапана; TA, атрезия ствола; TAPVR,тотальная аномалия венозного возврата; TGA, транспозиция магистральных сосудов; TOF, Тетрада Фалло; TV, Аномалия трикуспидального клапана; VSD, дефект межжелудочковой перегородки)
|
Ген |
Наследование |
Протеин |
Механизм |
Фенотип человека |
Модель фенотипа |
|
|
NKX2.5 |
AD, спорадическое |
Транскрип ционный фактор |
Гаплонедо статочность, доминирующее негативное |
ASD, AVB, VSD, TOF, HCM, TV abnormality |
Аневризма п редсердной перегородки, AVB |
|
|
TBX5 |
AD, спорадическое |
Транскрип ционный фактор |
Гаплонедо статочность, доминирующее негативное |
HOS, ASD, AVSD, AVB, TOF, T/PAPVR, TA, PS |
ASD, VSD, AVB |
|
|
GATA4 |
AD, спорадическое |
Транскрип ционный фактор |
Гаплонедо статочность |
ASD, VSD, AVSD, PV dysplasia |
ASD, VSD, AVSD, миокардиальные аномалии |
|
|
FOG2 |
Спорадическое |
Транскрип ционный фактор |
Потеря функции |
TOF |
AVSD, м иокардиальные аномалии, отсутствие к оронарных артерий, T OF |
|
|
TFAP2B |
AD, спорадическое |
Транскрип ционный фактор |
доминирующее негативное |
Char syndrome, PDA |
Поликистозная бо лезнь почек |
|
|
PTPN11 |
AD, спорадическое |
Сигнальная молекула
|
Приобретение функции |
Noonan syndrome, PS, PV dysplasia, ASD, AVSD, HCM |
ASD, VSD, AVSD, DO RV, миокардиальные аномалии |
|
|
JAG1 |
AD, спорадическое |
Сигнальная молекула
|
Гаплонедо статочность |
Alagille syndrome, TOF, PS/PPS |
RV and PA г ипоплазия, VSD аортальная декстрапозиция, ASD |
|
|
EVC/EVC2 |
AR |
Сигнальная молекула
|
Неизвестно |
Ellis– van Creveld syndrome, Common atrium, ASD |
Нет модели |
|
|
CRELD1 |
Спорадическое |
Сигнальная молекула |
Потеря функции |
AVSD |
Нет модели |
|
|
ZIC3 |
Х-сцепленное |
Транскрип ционный фактор |
Потеря функции |
Heterotaxy, ASD, AVSD, TGA, PS, DORV, TAPVR |
TGA, ASD, VSD, аномалия системного ве нозного возврата |
|
|
CFC1 |
Неизвестно |
Сигнальная молекула
|
Потеря функции |
Heterotaxy, TGA, DORV |
Правый изомеризм, TGA, септальные дефекты, ано малия системного венозного возврата |
|
|
PROSIT240 |
Неизвестно |
Сигнальная молекула
|
Неизвестно |
TGA |
Нет модели |
|
Молекулярные основы врожденных пороков сердца являются интересной и быстро развивающейся областью. Актуальность данной проблемы объясняется тем, что на данном этапе этиология, патогенетические механизмы и клиническое течение ВПС является одним из главных приоритетов пренатальной диагностики и неонатальной тактики ведения новорожденных. Врожденный порок сердца рассматривается как спорадический случай и редко рассматривают как генетический сбой. Риск рождения ребенка с врожденным пороком сердца увеличивается, если сами родители имеют врожденное заболевание сердца или при наличии в семье ребенка с врожденными дефектами сердечно-сосудистой системы.
Несмотря на значительные успехи в понимании механизмов, контролирующих развитие сердца, причины ВПС в организме человека остаются неопределенными в подавляющем большинстве случаев. Методы и инструменты, предназначенные специально для решения генетически сложных задач, дают возможность в полной мере изучить роль молекулярно-генетических механизмов врожденных пороков сердца и разгадать эту клинически важную тайну.
Список литературы:
1.Ashleigh A. Richards, Vidu Garg Genetics of Congenital Heart Disease// Current Cardiology Reviews, 2010, 6, 91—97.
2.Fahed AC, Gelb BD, Seidman JG, Seidman CE Genetics of congenital heart disease Genetics of Congenital Heart Disease: The Glass Half Empty//Circulation Research.2013;112:707—720.
3.Huang Jing-bina, Liu Ying-longa, Sun Pei-wub, Lv Xiao-donga, Du Minga, Fan Xiang-minga Molecular mechanisms of congenital heart disease // Cardiovascular Pathology 19 (2010) e 183 — e 193.
дипломов

