Статья опубликована в рамках: XXXIX Международной научно-практической конференции «Технические науки - от теории к практике» (Россия, г. Новосибирск, 22 октября 2014 г.)
Наука: Технические науки
Секция: Химическая техника и технология
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
Статья опубликована в рамках:
Выходные данные сборника:
ПРАКТИЧЕСКИЕ ОСНОВЫ ПОЛУЧЕНИЯ ГЕКСАМЕТИЛЕНТЕТРАМИНА ИЗ АММОНИЙНЫХ СОЛЕЙ МИНЕРАЛЬНЫХ КИСЛОТ
Жуманиязов Максуд Жаббиевич
д-р техн. наук, профессор, Ургенчский государственный университет, Республика Узбекистан, г. Ургенч
E-mail:
Курамбаев Шерзод Раимберганович
канд. техн. наук, доцент, Ургенчский государственный университет, Республика Узбекистан, г. Ургенч
E-mail:
Жуманиязова Дилноза Максудовна
ассистент кафедры общей химии, Ургенчский государственный университет, Республика Узбекистан, г. Ургенч
E-mail:
PRACTICAL BASES OF THE RECEIPT OF HEXAMETHYLENETETRAMINE FROM AMMONIUM SALTS OF MINERAL ACIDS
Jumaniyazov Maksud
doctor of technical sciences, prof., Urgench State University, Republic of Uzbekistan, Urgench
Kurambaev Sherzod
candidate of technical sciences, docent, Urgench State University, Republic of Uzbekistan, Urgench
Jumaniyazova Dilnoza
assistant, Urgench State University, Republic of Uzbekistan, Urgench
АННОТАЦИЯ
Данная статья посвящена исследованию возможности практического получения гексаметилентетрамина различными способами. В статье приводится результаты экспериментальных исследований реакций аммонийных солей ряда минеральных кислот с формальдегидом, а также оптимальные параметры получения гексаметилентетрамина из аммонийных солей.
ABSTRACT
This article is devoted to the investigations of possibility of practical receipt of hexamethylenetetramine of different ways. The results of experimental researches of reactions of ammonium salts of number of the mineral acids with formaldehyde, and also optimal parameters of receipt of hexamethylenetetramine from ammonium salts are given in the article.
Ключевые слова: гексаметилентетрамин; обратимая реакция; формальдегид; индикатор; технический формалин; степень превращения; минеральные кислоты; сульфат аммония
Keywords: hexamethylenetetramine; reversible reaction; formaldehyde; indicator; technical formalin; extent of transformation; mineral acids; ammonium sulfate
Обратимые реакции конденсации аммонийных солей минеральных кислот в гексаметилентетрамин (ГМТА) с помощью формальдегида мы изучали в зависимости от стехиометрической нормы расхода формальдегида в термостатированном сосуде, снабженном мешалкой в интервале температур от 20 до 80 °С путем титрования выделяющейся кислоты 0,1N раствором NaOH в присутствии индикатора метилового красного. В работе использовали технический формалин по ГОСТ 1625-75 и аммонийные соли квалификации "ч.д.а.". Концентрация формалинa составляла 37 %. Соли применяли в твердом виде и в виде растворов соответствующих концентраций [1].
Экспериментальные данные по степени превращения аммонийных солей в ГМТА (его выход) в зависимости от температуры, соотношений формальдегида и аммонийных солей представлены на рисунке 3.1 и в таблицах 3.2 и 3.3. Проведенные исследования показали, что реакции конденсации протекают с большой скоростью и равновесие достигается практически мгновенно, что является следствием больших значений рассчитанных нами констант равновесий Кр и подтверждается данными по скорости прохождения ультразвука через растворы, измеренные с помощью прибора УЗАС-7 и совпадением ее графика с кривой потенциометрического титрования аналогичных растворов щелочью.
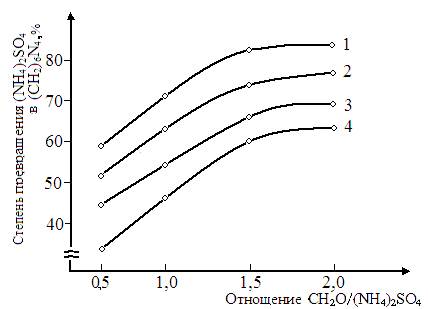
Рисунок 1. Выход гексаметилентетрамина в зависимости от соотношений формальдегида и сульфата аммония при различных температурах. Температура, 0С: 1- 20; 2- 40; 3- 60; 4- 80
Исключение составляли опыты с применением твердых солей, в которых визуально наблюдалась корреляция количества выделяющейся кислоты и скорости растворения кристаллов солей.
Как видно из приведенных данных, степень превращения аммонийных солей в ГМТА в значительной мере зависит от анионного остатка минеральной кислоты и соотношения формальдегида к соли, а также — от температуры.
![]() В зависимости от вида кислотного остатка степень превращения аммиака в ГМТА достигает наибольшего значения для моноаммонийфосфата, а наименьшего — для хлорида аммония, которые составляют соответственно 82 и 34 %. Изученные соли по способности к конденсации могут быть выстроены в следующий убывающий ряд:
В зависимости от вида кислотного остатка степень превращения аммиака в ГМТА достигает наибольшего значения для моноаммонийфосфата, а наименьшего — для хлорида аммония, которые составляют соответственно 82 и 34 %. Изученные соли по способности к конденсации могут быть выстроены в следующий убывающий ряд:
NH4H2PO4> (NH4)2SO4>(NH4)2HPO4>NH4NO3> NH4Cl
Порядок расположения солей зависит и согласуется со степенью их диссоциации с учетом ее подавления в присутствии соответствующих кислот. При этом, чем сильнее кислота, тем меньший требуется избыток формальдегида по отношению к соли для достижения равновесного выхода ГМТА.
Учитывая, что степень диссоциации солей находится в прямой зависимости от степени или константы диссоциации кислот, можно заключить, что значение степени превращения аммонийной соли в ГМТА является следствием степени диссоциации кислот, образующих эти соли [2].
Степень превращения аммонийных солей в ГМТА в зависимости от температуры изучена на примере сульфата аммония (табл. 3.3). При этом опыты проводили при постоянных температурах в пределах от 20 до 80 0С с интервалом 10 0С. Данные, приведенные на рисунках, показывают, что с увеличением температуры степень превращения повышается. В изученном интервале повышение температуры на 1 0С приводит к увеличению степени превращения в среднем на 0,16 %.
Таблица 1.
Степень превращения аммонийных солей в гексаметилентетрамин при рН=7, t =25 0C
|
Мол ьное отноше-ние СН2О: соль |
Теори-тичес кий выход (CH 2)6N4, Моль |
Степень пре-вра щения (NH 4)2HPO4 % |
Экспе римен-тальный выход (CH 2)6N4, моль |
Степень пре-вра щения NH 4NO3, % |
Экспе римен-тальный выход (CH 2)6N4, моль |
Степень пре- вра щения NH 4CI, % |
Экспе римен-тальный выход (CH 2)6N4, моль |
Степень пре-вра щения NH 4H2PO4, % |
Экспе римен-тальный выход (CH 2)6N4, моль |
|
1 1,2 !,4 1,6 1,8 2,0 2,2 2,4 2,6 3,0 5,0 |
1 1 1 1 1 1 1 1 1 1 1 |
35,0 41,0 44,5 48,0 50,0 52,0 53,7 55,3 57,2 59,2 62,0 |
0,35 0,41 0,445 0,48 0,50 0,52 0,537 0,553 0,572 0,592 0,62 |
35,1 39,7 43,7 47,0 49,5 50,5 50,8 51,1 |
0,351 0,397 0,437 0,470 0,495 0,505 0,508 0,511 |
23,5 27,5 30,8 33,5 34,2 34,4 |
0,235 0,275 0,308 0,335 0,342 0,344 |
61,5 67,3 72,3 76,5 79,0 80,0 80,4 80,8 |
0,615 0,673 0,723 0,765 0,790 0,80 0,804 0,808 |
Таблица 2.
Степень превращения сульфата аммония в гексаметилентетрамин при различных температурах
|
Моль- ное отно-шение СН2О : (NH4)2SO4 |
t= 20 0C |
t= 40 0C |
t= 60 0C |
t = 80 0C |
||||||||
|
Теорети-ческий выход (СН2)6 N 4, моль |
Степень превра-щения, % |
Экспе-римен-тальный выход (СН2)6 N 4, моль |
Степень превра-щения, % |
Экспе-римен-тальный выход (СН2)6 N 4, моль |
Степень превра-щения, % |
Экспе-римен-тальный выход (СН2)6 N 4, моль |
Степень превра-щения, % |
Эксперимен-тальный выход (СН2)6 N 4, моль |
||||
|
0,8 |
0,8 |
49,1 |
0,491 |
55,2 |
0,552 |
59,2 |
0,592 |
64,0 |
0,64 |
|||
|
1,0 |
I |
56,0 |
0,56 |
59,6 |
0,5% ? |
63,2 |
0,632 |
68,0 |
0,68 |
|||
|
1,25 |
I |
62,0 |
0,62 |
64,3 |
0,643 |
66,9 |
0,669 |
72,2 |
0,722 |
|||
|
1,5 |
I |
66,0 |
0,66 |
67,9 |
0,679 |
69,7 |
0,697 |
75,0 |
0,75 |
|||
|
1,75 |
I |
67,0 |
0,67 |
69,6 |
0,6% ? |
71,5 |
0,715 |
76,1 |
9,761 ??? |
|||
|
2,0 |
I |
67,3 |
0,673 |
70,0 |
0,700 |
72,0 |
0,72 |
76,5 |
0,765 |
|||
Таким образом, в результате экспериментально-теоретических исследований термодинамики равновесного состояния реакций конденсации аммонийных солей ряда минеральных кислот с формальдегидом, установлены оптимальные параметры получения ГМТА из аммонийных солей. Эти данные свидетельствуют о возможности получения ГМТА различными способами.
Список литературы:
1.Жуманиязов М.Ж. Удобрения пролонгированного действия, содержащие гексаметилентетрамин.: Автореф. дис.…канд. тех. наук. Ташкент: 1987. — 22 с.
2.Gaillard V., Bussien V., Paciorek W., Schenk K, Chapuis G. Hexamethylenetetramine Suberate, a strongly anharmonic modulated structure // Acta Crystallogr., Sect. B: Struct. Sci. — 1996. — B52(6). — P. 1036—1047.
дипломов

