Статья опубликована в рамках: XLIII Международной научно-практической конференции «Технические науки - от теории к практике» (Россия, г. Новосибирск, 24 февраля 2015 г.)
Наука: Технические науки
Секция: Технология продовольственных продуктов
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
Статья опубликована в рамках:
Выходные данные сборника:
ВЛИЯНИЕ МЕТОДА ОБРАБОТКИ И ТЕМПЕРАТУРЫ ХРАНЕНИЯ ГРАНАТОВОГО СОКА НА СОХРАННОСТЬ АНТОЦИАНОВ
Гафизов Гариб Керим оглы
канд. техн. наук, заведующий лаборатории биохимии и переработки плодов Азербайджанского научно-исследовательского института садоводства и субтропических культур, Республика Азербайджан, г. Губа
Е-mail : hafizov-54@mail.ru
Гафизов Самир Гариб оглы
специалист по процессам и аппаратам пищевых производств лаборатории биохимии и переработки плодов Азербайджанского научно-исследователь-c кого института садоводства и субтропических культур, Республика Азербайджан, г. Губа
EFFECT OF THE PROCESSING METOD AND STORAGE TEMPERATURE OF POMEGRANATE JUİCE ON THE SAFETY OF ANTHOCYANİNS
Qarib Hafizov
candidate of technical sciences, head of the laboratory of biochemistry and processing of fruit of Azerbaijan Science Research Institute of Horticultural and Subtropical Crops, Republic of Azerbaijan, Quba
Samir Hafizov
Specialty in processes and equipment for food production in the laboratory of biochemistry and processing of fruit of Azerbaijan Science Research Institute of Horticultural and Subtropical Crops, Republic of Azerbaijan, Quba
АННОТАЦИЯ
Показано как изменяется содержание антоцианов, а значит и антиоксидантная активность гранатового сока в начальной стадии его получения и при хранении в качестве готового продукта. Установлено, что обычными технологическими приёмами не удаётся достичь значительного эффекта в стабилизации природных антоцианов, потери их продолжаются непрерывно до полного исчезновения. При хранении соков неравнозначность действия температур +18…+22о и 0…+3 оС больше сказывается на антоцианах и катехинах по сравнению с аскорбиновой кислотой.
ABSTRACT
It is demonstrated how the anthocyanins content, and thus the antioxidant, activity of pomegranate juice, changes in the early stages of its production and storage as finished product. It is found that conventional techniques can not achieve a significant effect in stabilizing of the natural anthocyanins, losing their last no continuously until the complete disappearance. When storing juices none quivalance action temperature +18 ... +220 С and 0…+ 30 С more effect on anthocyanins and catechins compared with ascorbic acid.
Ключевые слова: гранатовый сок; технологическая обработка; хранение; аскорбиновая кислота; катехины; деградация антоцианов.
Keywords : pomegranate juice; technological processing; storage; ascorbic acid; catechins; degradation of anthocyanins.
Гранатовый сок относят к фруктовым сокам с высокой антиоксидантной активностью. Проведенные исследования на мышах и человеке показали, что гранатовый сок способен оказывать антиоксидантное, антиатерогенное, противораковое, гипотензивное и противовоспалительное действие. Кардиопротективный потенциал гранатового сока заслуживает дальнейшего исследования, но уже имеющиеся на сегодняшний день результаты могут послужить основанием для включения его в оздоровительный сердечный рацион [19, с. 5] .
Отмечается, что антиоксидантный потенциал гранатового сока выше, чем красного вина и зелённого чая, и индуцируется через эллаготанины и гидролизованные танины [24, с. 100], а также посредством того, что активные аномерные эллаготанины отвечают за более чем 50 % антиоксидантного потенциала сока [25, с. 2730].
Самые важные факторы, от которых зависит стабильность антоцианов ферменты, температура, кислород, рН, ионы металлов, аскорбиновая кислота, свет и т. д. [18, с. 15].
Ранее мы показали предпочтительность температуры 750 С для кратковременной обработки гранатового сока в начальной стадии процесса его получения [15, с. 138].
Нами были также поставлены опыты, в которых из гранатового сока с интенсивным цветом с помощью буферов готовили растворы с разными значениями рН от 1,8 до 8,0. Сразу после приготовления и через 24 часа хранения (при 0…+3 0С) самой высокой была интенсивность цвета в растворе с рН 5,0. Через 15 суток наиболее интенсивным стал цвет у раствора с рН 4,0, а через 30 суток — у раствора с рН 2,0. Превращения антоцианов в буферных растворах по своему характеру были следующие:
· предельно высокое значение рН, при котором достигается максимум интенсивности цвета за счёт взаимопревращений антоцианов равно 5,0, при этом же значении рН с максимально высокой скоростью идёт снижение интенсивности цвета при хранении растворов;
· в процессе хранения растворов усиление цвета, после которого непременно происходит необратимое снижение его интенсивности, проявляется тем позже, чем ниже значение рН, но при этом оно тем сильнее, чем выше значение рН в пределах их значений от 1,8 до 5,0.
В буферном растворе с самым низким значением рН, равным 1,8, через месяц сохранилось всего 53 % антоцианов к их начальному содержанию. Это позволило прийти к выводу, что низкое рН не может обеспечить в полной мере повышение стабильности антоцианов [14, с. 138].
В опытах, где хранились не буферные растворы, а плоды граната, также происходило увеличение интенсивности цвета их сока уже в первый месяц их хранения при температуре 50С, а вслед за этим интенсивность цвета сока, т. е. содержание антоцианов также снижалась, причем очень быстрыми темпами [20, с. 1805].
В процессах, сопровождающихся появлением продуктов окисления антоцианов, нарушением стабильности гранатового сока и выпадением осадка, существенная роль отводится аскорбиновой кислоте, катехинам и коллоидам белковой природы [3, с. 62]. Было показано [11, с. 95], что флавоноиды, в том числе и антоцианы, предохраняют аскорбиновую кислоту от окисления металлами, связывая их в стабильные комплексы.
Содержание лейкоантоцианов и образование осадка в гранатовом соке — явления взаимосвязанные, но при повышенном содержании лимонной кислоты в соке выпадение осадка обычно не происходит [12, c. 112]. В то же время, по результатам анализа сока 16 сортов граната из трёх районов произрастания (Крыма и др.) не обнаружено присутствие в нём лейкоантоцианов [16, с. 37].
В свежих соках азербайджанских сортов гранатов лейкоантоцианы также найдены не были. Однако, после хранения свежесобранных плодов в течение двух недель в обычных условиях, анализы показали появление в соках некоторого количества лейкоантоцианов, мг/л: Гюлейша розовая — 8,4, Гюлейша красная — 11,3, Ириданалы — 5,4, Весна — 2,0 и дикий гранат — 15,2. В соках интенсивно окрашенных сортов (Г. красная, Г. розовая) и интенсивно окрашенном соке дикого граната лейкоантоцианов содержалось больше, чем в слабоокрашенных соках других вышеуказанных сортов [13, c. 70].
Несмотря на эти и другие данные, в технологию производства гранатового сока до сих пор не удалось ввести основной по влиянию на качество этого продукта элемент, роль которого заключалась бы в обеспечении хорошей сохранности антоцианов. Предлагается придерживаться холодной обработки при отжиме сока и фильтровании и хранить готовый продукт при относительно низкой (5 0С) температуре [23, с. 905], а также добавлять на одну часть гранатового сока 0,020 части глюкозы и 0,03 части лимонной кислоты [4, c. 2]. Однако эффективность таких обработок не является достаточно высокой. Между тем, введение в технологию новшества такого характера, наряду с обеспечением выпуска сока с особенно привлекательным цветом, способствовало бы повышению биологической ценности продукта в результате лучшего сохранения в его составе антоцианов. Учитывая это, в качестве первоначальной, была поставлена задача — установить характер превращений антоцианов в вариантах технологии, не предусматривающих использование стабилизатора цвета, и тем самым, подчеркнуть всю важность происходящих в гранатовом соке изменений при хранении его в качестве готового продукта.
Экспериментальные исследовательские работы (описание их результатов дано в таблицах 1—3) проводились в лаборатории биохимии и переработки плодов Азербайджанского научно-исследовательского института садоводства и субтропических культур. Число технологических экспериментов по каждому варианту не менее пяти.
Отбор проб для химических анализов проводили по ГОСТ 26313-84 [5, c. 1]. Пробы подготавливали к анализу по ГОСТ 26671-85 [6, c. 2].
Концентрацию сухих растворимых веществ устанавливали рефрактометром по ГОСТ 28562-90 [7, c. 2], аскорбиновой кислоты — по ГОСТ 24556-89 [8, c. 2], титруемую кислотность — по ГОСТ 25555.0-82 [9, c. 2] Массовую долю общего сахара определяли по методу Бертрана ГОСТ 8756.13-87 [10, c. 3].
При расчетах зависимости между концентрацией антоцианов и лейкоантоцианов и оптическими плотностями при проведении определений по методике Свайна и Хиллиса [20, с. 63], исходили из градуировочной кривой, построенной для цианидин-моногликозида, полученному из плодов ежевики и очищенному по методике Ю.Г. Скориковой и Э.А. Шафтан [17, с. 455].
Исходные растворы готовили по методике Ю.Г. Скориковой и Э.А. Шафтан [17, с. 453], которая сводится к фиксации около 10 г сока (точная навеска) в мерной колбе кипящим метанолом, охлаждении ее под краном и доведении метанолом до 100 мл.
Приготовление испытуемых растворов сводилось к следующему. К 1 мл исходного раствора добавляли 9 мл 0,5 н HCL в 80—85 % метаноле, отсюда брали по 4,5 мл в две пробирки, в одну из них добавляли 1,5 мл 3 н HCL в метаноле, в другую — 1,5 мл реактива, состоящего из 9 мл 3 н HCL и 1 мл 30 % перекиси водорода.
Антоцианы гранатового сока являются нестойкими соединениями, которые под действием кислорода, температуры, света легко окисляются до соответствующих хинонов, не способных проявлять антиоксидантную активность [1, с. 34]. Поэтому, оптическая плотность испытуемых кислых растворов определялась до и после обработки их слабой перекисью водорода. После обработки слабой перекисью водорода антоцианы обесцвечиваются, что позволяет из оптической плотности испытуемого раствора против фона чистого метилового спирта до его обработки слабой перекисью водорода, вычесть оптическую плотность этого же испытуемого раствора после его обработки слабой перекисью водорода и по полученной разнице определить содержание собственно антоцианов. В список характеристик гранатовых соков нами также был введен показатель «сумма окрашенных пигментов», который определялся по оптической плотности испытуемого раствора до его обработки слабой перекисью водорода.
При определении суммы лейкоантоцианов брали 1 мл из приготовленного в количестве 100 мл общего с антоцианами исходного раствора, добавляли к нему 1 мл дистиллированной воды для снижения концентрации метилового спирта и разделяли на две равные части. К одной из них добавляли 10 мл кислого бутанола (бутиловый спирт/ концентрированная HCL=20: 1), тщательно перемешивали в закрытом стеклянном сосуде, нагревали при 970 С точно 40 минут, затем охлаждали и измеряли оптическую плотность при длине волны 500 нм в кюветах с толщиной рабочего слоя 10 мм (при этой же длине волны и в таких же кюветах определялись собственно антоцианы и сумма окрашенных пигментов) против фона (вторая часть от разбавленного наполовину водой исходного экстракта 1 мл + кислый бутиловый спирт, без нагревания).
Сумму катехинов определяли фотометрическим методом с использованием ванилинового реактива [2, с. 455]. Расчёты вели по градуировочной кривой, построенной по чистому препарату эпикатехина.
Все аналитические определения выполнены в 3-кратной повторности. Данные статистически обработаны с использованием программы Excel. При этом средняя квадратическая ошибка среднего не превышала 1,5—2,0 %.
Как нами уже было отмечено, снижение концентрации собственно антоцианов и появление в них лейкоантоцианов — это нежелательный процесс с точки зрения сохранения стабильности и натуральности гранатовых соков на исходном уровне.
Из табл. 1 видно, что осветление свежеотжатого гранатового сока путём быстрого его подогрева до 750 С, выдерживания 1—3 мин и охлаждения до 35—400 С не приводит появлению в соке лейкоантоцианов, чего нельзя сказать о трёх других испытанных способах осветления. При этом остаётся неясным, как испытанные способы обработки отразятся на сохранении антоцианов после фильтрования, розлива, пастеризации и хранения в качестве готовой продукции.
В табл. 2 дано содержание антоцианов в хранившихся 6 месяцев при температуре +18…+22 0С гранатовых соках, обработанных перед фильтрованием, розливом и пастеризацией по вариантам за номерами: 1 — отжим, процеживание, отстаивание 2 ч., сепарация; 2 — горячий розлив в стеклянные сосуды, выдержка 3 мес., сцеживание с осадка; 3 — осветление желатином 6 ч. при температуре 6…80 С, декантация; 4 — осветление мгновенным подогревом до 750 С и охлаждением до 350 С, 5 — осветление желатином в сочетании с мгновенным подогревом до 75 0С и охлаждением до 35 0С; 6 — процеживание, осветление 6 ч. желатином [перед отжимом зёрна обработаны острым (800С) паром]. Из нее видно, что в соках из предыдущего
Таблица 1.
Химические показатели свежеотжатого гранатового сока различных способов осветления (сорт Гюлейша красная)
|
Способ осветления
Показатели |
6-часовая обработка 1 % р-ом желатинапри темпера- туре +7 …+80 С |
«Мгновен- ный» подогрев до 750 С за 1—3 мин и охлаждение до 35—40 0С |
Обработка желатином в сочетании с «мгновенным» подогревом до 75 0С и охлаждением до 35-400С |
Обработка желатином [перед отжимом зёрна в течение 2 мин обработаны острым (800 С) паром] |
|
Р-мые сухие вещества, % |
16,1 |
17,2 |
15,2 |
15,6 |
|
Кислотность,% |
1,08 |
1,08 |
0,70 |
0,90 |
|
Лейкоантоцианы, мг/л |
12,9 |
0 |
5,3 |
4,3 |
|
Собственно антоцианы, мг /л |
230,7 |
248,8 |
211,3 |
207,3 |
|
Сохранность собственно антоцианов, % к начальному содержанию их в свежеотжатом соке (386 мг /л) |
59,8 |
64,5 |
54,7 |
53,7 |
Таблица 2.
Содержание антоцианов в хранившихся 6 мес. при температуре +18…+22 0С пастеризованных гранатовых соках (сорт Гюлейша красная)
|
П о к а з а т е л и |
Номера испытанных вариантов технологии |
||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
||
|
Сухие вещества, % |
16,0 |
16,0 |
16,0 |
17,0 |
15,0 |
15,4 |
|
|
Сумма сахаров, % |
13,28 |
13,23 |
13,25 |
14,12 |
12,76 |
12,68 |
|
|
Общая кислотность, % |
1,08 |
1,07 |
1,07 |
1,09 |
0,69 |
0,88 |
|
|
Аскорбиновая кислота, мг% |
3,17 |
2,64 |
3,17 |
2,99 |
2,46 |
2,64 |
|
|
Сумма окрашенных пигментов , мг /л |
255,94 |
199,64 |
195,59 |
172,9 |
160,31 |
168,09 |
|
|
Лейкоантоцианы, мг /л |
7,4 |
7,0 |
10,2 |
12,6 |
10,7 |
3,8 |
|
|
Собственно антоцианы, мг/л |
133,3 |
166,7 |
190,7 |
137,3 |
144,8 |
138,0 |
|
|
Сохранность собственно антоцианов, % к начальному содержанию их в свежеотжатом соке (386 мг /л) |
34,5 |
43,2 |
49,4 |
35,6 |
37,5 |
35,8 |
|
Из табл. 2 видно, что в соках из предыдущего опыта (варианты за номерами 3—6) через 6 мес. xранения в пастеризованном виде при температуре +18…+220 С содержание собственно антоцианов изменяется в пределах 133,3…190,7 мг/л. Сохранность собственно антоцианов в процентах к их исходному содержанию в свежеотжатом соке в лучшем варианте (осветление желатином) составила 49,4 %, в худшем (осветление «мгновенным» подогревом) — 35,6 %. Значит, холодная обработка свежеотжатого сока желатином в этих условиях обеспечивает более высокий процент сохранности, чем обработка свежеотжатого сока «мгновенным» подогревом и охлаждением. Однако, как было установлено нами позже, для длительного хранения соков в охлаждаемых условиях больше подходит обработка свежеотжатого сока «мгновенным» подогревом. Это связано с тем, что процессы деградации антоцианов, катализатором для которых может служить термическая обработка, резко замедляются в условиях низких температур, что создаёт условия для лучшего сохранения первоначально достигнутого эффекта в сохранении антоцианов от кратковременной обработки свежеотжатого сока при температуре 750 С. Об этом говорят данные таблицы 3 по хранившимся 6 мес. при температуре 0…+3 0С гранатовым сокам, которые перед фильтрованием, розливом и пастеризацией подверглись обработке по вариантам: 1 — отжим; процеживание; отстаивание 2 ч., сепарация; 2 — подогрев свежеотжатого процеженного сока до 62 0С, отстаивание 24 ч., декантация; 3 — осветление желатином в течение 6 ч., декантация; 4 — осветление мгновенным подогревом до 750 С и охлаждением до 350 С, 5 — осветление танин — желатином в сочетании с мгновенным подогревом до 750 С и охлаждением до 250 С; 6 — осветление танин- желатином в течение 6 ч., декантация и фильтрование; 7 — осветление желатином в сочетании мгновенным подогревом до 750 С и охлаждением до 350 С; 8 — горячий розлив в стеклянные сосуды, выдержка 3 мес., сцеживание с осадка; 9 — осветление желатином и подкрашивание растительным (свекольным) красителем (0,03 % и массе сока); 10 — отжим сока из четвертушек плодов, горячий розлив в стеклянные сосуды, выдержка 3 мес., сцеживание с осадка. Из таблицы видно, что сохранность антоцианов в соке, осветленном «мгновенным» подогревом, выше (49,7 %), чем в соке, осветленном желатиной (42,7 %). Но в общем нет большой разницы по этому показателю между двумя вышеупомянутыми и другими испытанными вариантами, в зависимости от варианта он варьирует в пределах от 35,9 до
Таблица 3.
Содержание антоцианов в хранившихся 6 мес. при температуре 0…+30 С пастеризованных соках (сорт Гюлейша розовая)
|
П о к а з а т е л и |
Номера испытанных вариантов технологии |
||||
|
1 |
2 |
3 |
4 |
5 |
|
|
Р-мые сухие вещества,% |
12,0 |
12,0 |
12,0 |
12,8 |
13,7 |
|
Сумма сахаров,% |
10,31 |
10,13 |
9,81 |
10,76 |
11,04 |
|
Общая кислотность,% |
1,28 |
1,31 |
1,28 |
1,28 |
1,28 |
|
Аскорбиновая кислота, мг% |
3,52 |
3,34 |
3,40 |
3,60 |
3,17 |
|
Сумма окрашенных пигментов, мг/л |
147,9 |
139,2 |
133,7 |
149,3 |
126,1 |
|
Лейкоантоцианы,мг /л |
6,8 |
5,8 |
12,5 |
4,7 |
2,4 |
|
Собственно антоцианы,мг /л |
139,3 |
136,0 |
122,0 |
142,0 |
120,7 |
|
Сохранность собственно антоцианов, % к начальному содержанию их в свежеотжатом соке (286 мг /л) |
48,7 |
47,5 |
42,7 |
49,7 |
42,2 |
Продолжение таблицы 3.
|
П о к а з а т е л и |
Номера испытанных вариантов технологии |
||||
|
6 |
7 |
8 |
9 |
10 |
|
|
Р-мые сухие вещества, % |
12,0 |
13,6 |
14,0 |
12,2 |
16,7 |
|
Сумма сахаров, % |
9,88 |
11,08 |
11,18 |
10,26 |
13,92 |
|
Общая кислотность, % |
1,29 |
1,26 |
1,30 |
1,32 |
1,34 |
|
Аскорбиновая кислота, мг% |
3,27 |
2,29 |
2,10 |
2,64 |
2,29 |
|
Сумма окрашенных пигментов, мг/л |
126,3 |
139,7 |
193,9 |
142,6 |
160,9 |
|
Лейкоантоцианы, мг/л |
0 |
0 |
3,1 |
0 |
10,6 |
|
Собственно антоцианы, мг/л |
102,7 |
110,0 |
130,0 |
111,0 |
128,7 |
|
Сохранность собственно антоцианов, % к начальному содержанию их в свежеотжатом соке (286 мг/л ) |
35,9 34,2 |
38,5 36,7 |
45,5 43,3 |
38,8 37,0 |
45,0 42,9 |
47,3 %. По тому же показателю соки, хранившихся при температуре +18…+22 0С, мало отличаются от соков, хранившихся при температуре 0…+3 0С. Это объясняется тем, что на сохранность антоцианов влияют не только способ обработки и условия хранения, но и начальное содержание в свежеотжатом соке. Хранившиеся при температуре 0…+3 0С пастеризованные соки были изготовлены из свежеотжатого сока с более низким начальным содержанием антоцианов (286 мг/л), чем хранившиеся при температурах +18…+22 0С (386 мг /л), поэтому и получились результаты по сохранности антоцианов почти одинаковыми. Не только в наших, но и в других опытах, соки с высоким содержанием антоцианов показывали наибольшую стабильность пигмента [22, с. 340].
Вызываемое «мгновенным» подогревом усиление интенсивности цвета (из табл. 1 видно, что содержание собственно антоцианов в этом варианте обработки выше, чем в других вариантах) является, вероятно, следствием гидролиза самых нестойких гликозидов. Один из продуктов их гидролизов — агликоны. Они более яркого цвета и больше склоны к превращениям по сравнению с гликозидами антоцианов. Но если хранение соков осуществляется в охлаждаемых условиях, скорость окислительных превращений антоцианов становится замедленной и исходный цвет сока в этом варианте сохраняется лучше, чем во всех других испытанных вариантах.
В таблицах 4 и 5 представлены данные о количествах деградировавших антоцианов, появившихся окрашенных продуктов их окисления и выпавшего осадка в образцах гранатового сока из предыдущих опытов. Если ориентируясь на данные этих таблиц, поставить образцы соков, в том числе повторяющих друг друга по методу обработки в один ряд, начинающийся с образца с самым низким содержанием деградировавших антоцианов и заканчивающийся образцом, с самым высоким содержание деградировавших антоцианов, то станет ясно, что в 9 образцах сока (из 16-ти) с повышением количества деградировавших антоцианов повышается также содержание появившихся окрашенных продуктов их деградации.
Таблица 4.
Количества деградировавших антоцианов, появившихся окрашенных продуктов их деградации и выпавшего осадка в пастеризованных гранатовых соках после хранения их 6 месяцев при температуре +18…+22 0С, в мг/л (сорт Гюлейша красная)
|
Показатели |
Номера испытанных вариантов технологии |
|||||
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
Деградировавшие антоцианы |
252,7 |
219,3 |
195,3 |
248,7 |
241,2 |
248,0 |
|
Появившиеся продукты деградации антоцианов |
122,6 |
32,9 |
4,9 |
35,6 |
15,5 |
30,1 |
|
Осадок |
820 |
910 |
970 |
1010 |
1190 |
1460 |
|
Суммарное количество появившихся продуктов деградации антоцианов и выпавшего осадка |
204,6 |
123,9 |
101,9 |
136,6 |
134,5 |
176,1 |
Таблица 5.
Количества деградировавших антоцианов, появившихся окрашенных продуктов их деградации и выпавшего осадка в пастеризованных гранатовых соках после хранения их 6 месяцев при температуре 0…+30 С, в мг/ л (сорт Гюлейша розовая)
|
Показатели |
Номера испытанных вариантов технологии |
||||
|
1 |
2 |
3 |
4 |
5 |
|
|
Деградировавшие антоцианы |
146,7 |
150,0 |
164,0 |
144,0 |
165,3 |
|
Появившиеся продукты деградации антоцианов |
8,6 |
3,2 |
11,7 |
7,3 |
5,4 |
|
Осадок |
1000 |
1740 |
1510 |
870 |
1460 |
|
Суммарное количество появившихся продуктов деградации антоцианов и выпавшего осадка |
108,6 |
177,2 |
162,7 |
94,3 |
151,4 |
Продолжение таблицы 5.
|
Показатели |
Номера испытанных вариантов технологии |
||||
|
6 |
7 |
8 |
9 |
10 |
|
|
Деградировавшие антоцианы |
183,3 |
176,0 |
156,0 |
175,0 |
157,3 |
|
Появившиеся продукты деградации антоцианов |
23,6 |
29,7 |
63,9 |
31,6 |
32,2 |
|
Осадок |
130 |
112 |
120 |
127 |
176 |
|
Суммарное количество появившихся продуктов деградации антоцианов и выпавшего осадка |
153,6 |
141,7 |
183,9 |
158,6 |
205,2 |
В 8 образцах, с повышением количества деградировавших антоцианов повышается и количество выпавшего осадка. В 10 образцах, наряду с повышением количества деградировавших антоцианов повышается также суммарное количество появившихся окрашенных продуктов их деградации и выпавшего осадка. Это значит, что мы не смогли в данном случае выявить прямую зависимость между вышеуказанными показателями в рамках вероятности, удовлетворяющей достоверности P < 0,05. Но это вовсе не значит, что такая связь не могла бы быть установлена в условиях других опытов, с большим количеством испытуемых образцов.
Как видно из рисунка 1, в консервированных сорбиновой кислотой соках собственно антоцианы сохраняются лучше, чем в пастеризованных соках.
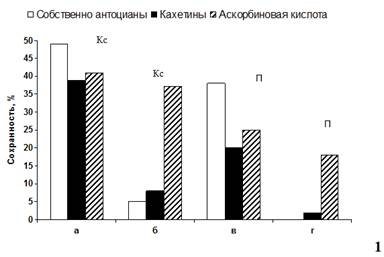
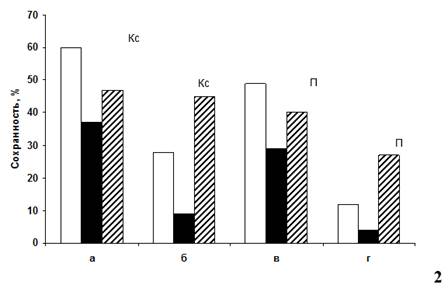
Рисунок 1. Сохранность собственно антоцианов, кахетинов и аскорбиновой кислоты в консервированном сорбиновой кислотой (Кс) и пастеризованном (П) осветленных натуральных гранатовых соках (сорт Гюлейша розовая), хранившихся 6 (а,в) и 12 (б,г) месяцев при температуре +18…+220С (1) и 0…+30С (2)
Однако после 6 и, особенно, 12 месяцев хранения биологическая ценность консервированных сорбиновой кислотой соков заметно ослабевает. Еще в большей мере это характерно для пастеризованных соков, в которых после 12 месяцев хранения антоцианы и катехины уже не обнаруживаются аналитически.
При хранении соков неравнозначность действия температур +18…+22 0С и 0…+30 С больше сказывается на собственно антоцианах и катехинах по сравнению с аскорбиновой кислотой.
Временная стабилизация цвета достигается за счет «мгновенного» подогрева свежеотжатого сока до температуры 750 C и столь же быстрого охлаждения до температуры 35—400 C, когда ферменты инактивированы, а термическая деградация антоцианов почти не происходит. Однако после фильтрации, пастеризации и при хранении качество гранатового сока постоянно снижается в связи с неустанным повышением количества продуктов деградации антоцианов, определяемых путем обесцвечивания испытуемого раствора слабой перекисью водорода.
Список литературы:
1.Белая Н.И. Антирадикальная активность фруктовых соков в реакции с дифенилпикрилгидразином/ Н.И. Белая, А.Н. Николаевский, Т.Н. Ивлева// Химико-фармацевтический журнал, — 2009. — т. 43. — № 6. — с. 32—34.
2.Вигоров Л.И. Определение различных форм катехинов в плодах и ягодах //Тр. II-го Всесоюз. семинара по биологич. активн. в-вам плодов и ягод. Свердловск, 1964. — с. 451—460.
3.Гафизов Г.К. Статистическое описание стабильности гранатового сока / Г.К. Гафизов, Д.Ш. Мамедов, Г.Ш. Абубекиров // Аграрная наука Азербайджана. Баку, — 2011. — № 2. — с. 61—63.
4.Гафизов Г.К., Сёмочкина Л.Г., Гахраманов М.С. Способ повыщения стабильности природной окраски пастеризованного натурального гранатового сока. // Патент СССР №1535517. 1990. Бюл. № 2.
5.ГОСТ 26313-84. Продукты переработки плодов и овощей. Правила приемки , методы отбора проб. введ. 01.07.1985. М:Стандартинформ, 2010. — 4 с.
6.ГОСТ 26671-85. Продукты переработки плодов и овощей, консервы мясные и мясорастительные. Подготовка проб для лабораторных анализов. введ. 01.08.86. М: Стандартинформ, 2010. — 2 с.
7.ГОСТ 28562-90. Продукты переработки плодов и овощей. Рефрактометрический метод определения растворимых сухих веществ. Введ. 01.07.91. М: Стандартинформ, 2010. — 11 с.
8.ГОСТ 24556-89. Продукты переработки плодов и овощей. Методы определения вмтамина C. введ. 01.01.90. М: Изд-во стандартов, 2003. —10 с.
9.ГОСТ 25555.0-82. Продукты переработки плодов и овощей. Методы определения титруемой кислотности. введ. 01.01.83. М: Стадартинформ, 2010. — 9 с.
10.ГОСТ 8756.13-87. Продукты переработки плодов и овощей. Методы определения сахаров. введ. 01.01.89. М: Стандартинформ, 2010. — 9 с.
11.Давидек И. Определение флавоноидных веществ после разделения методом хроматографии на бумаге // Биохимия, — 1961. — т. 26, — вып. 1. — с. 93—99.
12.Кривенцов В.И. Антоцианы плодов граната / В.И. Кривенцов, Н.К. Аренд //Тр. ГНБС Ялта, — 1981. — т. 33. — с. 110—116.
13.Мамедов Д.Ш. Полифенольный комплекс плодов граната / Д.Ш. Мамедов, Г.К. Гафизов // Аграрная наука Азербайджана. Баку, — 2009. — № 1—2. — с. 69—70.
14.Мамедов Д.Ш. Влияние рН на стабильность флавоноидов гранатового сока / Д.Ш. Мамедов, Г.К. Гафизов // Аграрная наука Азербайджана. Баку, — 2009. — № 3—4. — с. 137—138.
15.Мамедов Д.Ш. Влияние температуры обработки на стабильность флавоноидов гранатового сока / Д.Ш. Мамедов, Г.К. Гафизов // Аграрная наука Азербайджана. Баку, — 2009. — № 3—4, — с. 137—138.
16.Марх А.Т. Полифенолы гранатов /А.Т. Марх, Т.А. Лысогор // Известия взов СССР. Пищевая технология. — 1973. — № 2. — с. 36—38.
17.Скорикова Ю.Г. Методика определения антоцианов в плодах и ягодах /Ю.Г. Скорикова, Э.А. Шафтан// Труды III-го Всесоюз. Семинара по биолог. активн. в-вам плодов и ягод. Свердловск, 1968. — с. 451—460.
18.Танчев С.С. Антоцианы в плодах и овощах. М.: Пищ. пром-сть, 1981. — с. 304.
19Basu A. Pomeqranate juice: a heart-heaethy fruit juice. / A. Basu, K. Penuqonda //Nutr. Rev.— 2009. — vol. 67. issue 1. — p. 49—56.
20.Fisher U.A. Kammerer thermal stability of anthocyanins and colourless phenolics in pomegranate (Punica granatum L) juices and model solutions /U.A. Fisher, R. Carle and R. Dietmar // Food Chmistry. — 2013. — vol. 138. — issues 2—3. — p. 1800—1809.
21.Malik A. Pomeqranate fruit juice for chemoprevention and chemotherapy of prostate cancer. / Malik A., Afaq F., Sarfara S. [et al.] // Proc Natl Acad Sci USA, — 2005. — vol. 102. issue 41. — p. 108—113.
22.Miguel G. The contration of anthocyanins in fruits of «Assaria» hjmegranate a sweet Portuguese cultivar typically grown in Algarve (south Portugal), was monitored during storage under different conditions / G. Miguel, C. Fontes, Antunes D. [et. Al.] // Biomed Biotechnol. — 2004. — № 5. — р. 338—342.
23.Karnan M. Effects of processing method and srorage temperature on clear pomegranate juice turbidity and color hatice r ozyci /M. Karnan, N. Tetik and I. Turnan // Food Processing and Preservation. — 2013. — vol. 37. — issue 5. — p. 899—906.
24.Zarfeshany A. Potent health effects of pomeqranate /A. Zarfeshany, S. Asqary and S.H. Javanmard // Adv Biomed Res., 2014.-3:100. [Electronik resource] — URL: http//www.ncbi.nlm.nih.gov/pmc/articles/PMC4007340/ (date of treatment 2014.03.25).
25.Patel C. Safety assessment of pomeqranate fruit extrakt: acute and subchronic toxicity studies / Patel C., Asqary S., Javanmard S.H. [et al.] // Food Chem Toxicol. — 2008. — vol. 46. — issue 8. — p. 2728—2735.
26.Swain T. The phenolic constituents of Prunus Domestica L. The quantitative analysis of phenolic constituents/ T. Swain, W. Hillis// J. Sci. Food Agric. — 1959. — vol. 10. — № 1. — p. 63—68.
дипломов

