Статья опубликована в рамках: IV Международной научно-практической конференции «Технические науки - от теории к практике» (Россия, г. Новосибирск, 05 октября 2011 г.)
Наука: Технические науки
Секция: Технология продовольственных продуктов
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
ЗАМОРАЖИВАНИЕ ЯГОДЫ ДИОКСИДОМ УГЛЕРОДА
Иваненко Олег Васильевич
к. т. н., доцент КемТИПП, г. Кемерово
E-mail: ivanenkooleg@mail.ru
Диоксид углерода наиболее подходит для прямого контактного замораживания различных видов продуктов. Как контактный хладагент, он привлекателен дешевизной, химической пассивностью и термической стабильностью, не коррозирует металлических узлов, не горюч, не опасен для персонала. Жидкая углекислота при атмосферном давлении мгновенно превращается в смесь сухого снега и холодного углекислого газа, при этом газовая смесь внутри скороморозильного аппарата способна охладить продукт от +20°С до -78,5°С за несколько минут. Процесс замораживания протекает при высокой скорости без деформации в структуре продукта. Продукты, замораживаемые с помощью диоксида углерода, получают высокую органолептическую оценку, а потери массы из-за усушки составляют 0,3%.
При замораживании частицы в классической задаче Стефана [1, с. 424] процесс фазового перехода протекает при постоянной температуре на границе раздела фаз. В этом случае практически все теплофизические параметры (теплопроводность, теплоемкость, удельное сопротивление) изменяются скачкообразно.
В плодах ягоды благодаря ее пористой структуре процесс протекает иначе. Содержание жидкой фазы наблюдается при любой (практически до –100°С) температуре. По мере снижения температуры образца уменьшается доля жидкой фазы и увеличивается доля твердой, четкая граница раздела фаз отсутствует. В процессе замораживания выделяется теплота фазового перехода.
При моделировании процесса приняты следующие допущения:
· температура диоксида углерода остается постоянной;
· плотность замороженного продукта не зависит от температуры;
· температура в любой точке частицы зависит только от текущего радиуса и времени (симметричная задача).
Количество вымороженной воды характеризуется величиной ω,
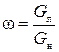 , (1)
, (1)
где Gл,, Gн – масса частицы льда и воды, соответственно, кг.
которая может изменяться от 0 до 1 по мере снижения температуры от tкр (tкр – криоскопическая температура). Для определения ω рекомендована следующая зависимость [2, с. 91],
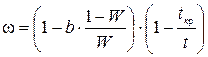 , (2)
, (2)
где b – содержание прочно связанной воды на единицу массы сухого вещества, кг/кг;
W – начальное содержание влаги в продукте;
tкр – криоскопическая температура, °С.
Дифференциальное уравнение теплопроводности для сферической частицы имеет вид
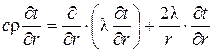 , (3)
, (3)
где c – теплоемкость, Дж/кг∙К;
ρ – плотность, кг/м³;
λ – теплопроводность, Вт/м∙К.
Теплоемкость до начала замораживания (t > tкр) определяется по формуле
![]() , (4)
, (4)
где сс, св – теплоемкости сухой массы и воды, соответственно, Дж/кг∙К.
При достижении кроископической температуры в частице появляется твердая фаза, доля которой растет по мере снижения температуры.
Теплота фазового перехода, выделяемая при замораживании влаги, учитывается как дополнительная теплоемкость, определяемая соотношением
![]() , (5)
, (5)
где r – теплота кристаллизации воды, кДж/кг.
Первые три слагаемых формулы (5) характеризуют вклад теплоемкостей сухого вещества, льда и воды, соответственно, последнее слагаемое – теплоту, выделяемую при кристаллизации воды.
Начальное условие: при ![]()
![]() .
.
Граничные условия:
при ![]()
![]() ;
;
при ![]()
![]()
где α – коэффициент теплоотдачи от частицы к хладагенту, Вт/м∙К;
tx – температура диоксида углерода, °С.
Ввиду нелинейного характера поставленной задачи, сложных зависимостей теплофизических характеристик от температуры ее аналитическое решение не представляется возможным. Поэтому процесс смоделирован на персональном компьютере с применением численных методов.
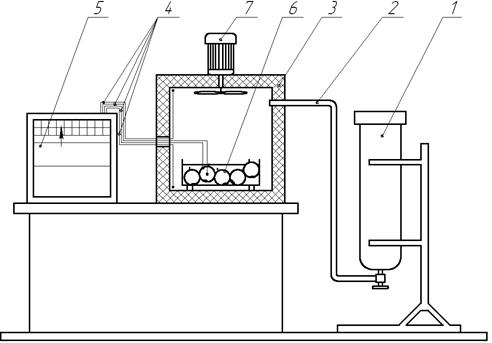
Для исследования процесса замораживания ягоды была использована экспериментальная установка [3], внешний вид которой представлен (рис. 1).
Рисунок 1. Схема экспериментальной установки
|
|
|
1 –баллон углекислотный; 2 – трубопровод медный; 3 – камера теплоизолированная; 4 – термопары хромель-копелевые; 5 – потенциометр КСП-4; 6 – ягода; 7 – вентилятор. |
Установка состоит из устройств и измерительного прибора, позволяющих проводить процесс замораживания ягоды с контролем параметров:
· изменения скорости движения газа в камере;
· изменение температурного поля ягоды в зависимости от времени.
Ягоду (6) помещают в изолированную камеру (3). После чего камера закрывается, и в нее из баллона (1) подается диоксид углерода по трубопроводу (2). Изменение температуры в слое ягоды и камере контролируется с помощью хромель-копелевых термопар (4) сигнал с которых подается на потенциометр КСП-4 (5). Циркуляция газа в камере обеспечивается вентилятором (7).
При проведении эксперимента в качестве модельной среды использовались плоды облепихи. В камеру периодично осуществлялась подача диоксида углерода. Отсчитывалось время процесса, и через определенные промежутки фиксировалась температура в камере, на поверхности и в объеме ягоды. Через 12 минут от начала замораживания она составила – 60°С.
Дискретный аналог уравнения Фурье (3) получен с использованием явной схемы с постоянным шагом по r и τ. Использование явной схемы для аппроксимации дифференциального уравнения накладывает определенные ограничения на выбор величин шагов по времени (Δτ) и координате (Δr). Устойчивость вычисления обеспечивается при условии:
![]() , (6)
, (6)
 , (7)
, (7)
где Fo – сеточное число Фурье.
В процессе исследования ягоды, замороженной диоксидом углерода, выявлен ряд принципиальных преимуществ по сравнению с традиционной технологией заморозки:
· время заморозки сокращается до 5-30 минут;
· быстро прекращается ферментативная активность в продукте;
· хорошо сохраняется структура тканей и клетки продукта, поскольку кристаллы льда формируются значительно меньших размеров и практически одновременно в клетках и в межклеточном пространстве тканей;
· при медленной заморозке в продукте появляются следы жизнедеятельности бактерий, в то время как при шоковой заморозке они просто не успевают развиться;
· потери массы продукта в результате усушки составляют всего 0,3% (против 3-6%).
По сравнению с замораживанием жидким азотом, при замораживании диоксидом углерода:
· не наблюдается растрескивание продукта из-за слишком большого перепада температуры между поверхностью и сердцевиной замораживаемого продукта
· в процессе замораживания диоксид углерода проникает в продукт и во время размораживания защищает его от окисления и развития микроорганизмов.
Плоды и овощи, подвергнутые быстрой заморозке и фасовке на месте, наиболее полно сохраняют вкусовые достоинства и питательную ценность, все витамины и биологически активные вещества, что дает возможность широко применять их для производства продуктов для детского и диетического питания.
Список литературы:
1.Лыков А.В. Теория теплопроводности. – М.: Высшая школа, 1967.–599 с.
2.Рогов И.А., Куцакова В.Е., Филиппов В.И., Фролов С.В. Консервирование пищевых продуктов холодом. – М.: Колос, 1999.–176 с.
3.Неверов Е.Н. Разработка технологии холодильной обработки тушек птицы диоксидом углерода в условиях транспортировки: дис. канд. техн. наук: 05.18.04 Кемерово, 2007. –145 с.
дипломов