Статья опубликована в рамках: XVI Международной научно-практической конференции «Естественные и математические науки в современном мире» (Россия, г. Новосибирск, 05 марта 2014 г.)
Наука: Химия
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
Статья опубликована в рамках:
Выходные данные сборника:
НОВЫЙ НИОБАТ ЛИТИЯ-МАРГАНЦА (II) СО СТРУКТУРОЙ ТИПА NACL
Ганноченко Алексей Анатольевич
канд. хим. наук, преподаватель, средняя школа № 6, РФ, г. Таганрог
NEW LITHIUM MANGANESE (II) NIOBATE WITH NACL STRUCTURE
Alexey Gannochenko
candidate of Science, lecturer, medium school № 6, Russia, Taganrog
АННОТАЦИЯ
Методом рентгенофазового анализа изучено фазообразование на сечении Li3NbO4-MnO в тройной системе Li2O-MnO-Nb2O5. Образцы получены методом твердофазного синтеза в атмосфере водорода. Получен новый частично упорядоченный ниобат лития-марганца (II) со структурой каменной соли, проведено полнопрофильное уточнение структуры. Тип упорядочения сопоставлен и обсужден с аналогичными фазами.
ABSTRACT
By the XRD, phase formation on the cut Li3NbO4-MnO in the ternary system Li2O-MnO-Nb2O5 was studied. The patterns were prepared by the solid state method in hydrogen atmosphere. A new partially ordered lithium manganese (II) niobate with rock salt structure was obtained, and full profile refinement was examined. The ordering type was discussed with compare in analogous phases.
Ключевые слова: упорядочение; ниобат; марганец; литий; твердофазный синтез; рентгенофазовый анализ; структура каменной соли.
Keywords: ordering; niobate; manganese; lithium; solid state synthesis; X-ray diffraction; rock salt structure.
В рамках исследования тройной системы Li2O-MnO-Nb2O5 изучено фазообразование в сечении Li3NbO4-MnO при температуре ~1000 °C. Для этого были приготовлены и сделан анализ ряда образцов (табл. 1,), находящихся на сечении и вблизи него.
Таблица 1.
Результаты РФА образцов сечения Li 3NbO4-MnO
|
Состав, изученных образцов, разреза Li 3NbO4–MnO, мол. % |
Фазовый состав образцов по данным РФА |
||
|
Li 2O |
MnO |
Nb 2O5 |
|
|
30 |
60 |
10 |
Li3Mn2NbO6 + MnO |
|
34 |
55 |
11 |
Li3Mn2NbO6 + следы MnO |
|
37,5 |
50 |
12,5 |
Li3Mn2NbO6 |
|
41 |
45 |
14 |
Li3NbO4×MnO + Li3Mn2NbO6 |
|
45 |
40 |
15 |
Li3NbO4×MnO + Li3Mn2NbO6 |
|
50 |
33,5 |
16,5 |
Li3NbO4×MnO |
|
56,5 |
25 |
18,5 |
Li3NbO4×MnO + следы LiNbO3 |
|
60 |
20 |
20 |
Li3NbO4×MnO + следы Li3NbO4 + следы LiNbO3 |
|
64 |
15 |
21 |
Li3NbO4×MnO + Li3NbO4 + следы LiNbO3 |
Оксид марганца MnO имеет структуру типа NaCl. Ортониобат лития Li3NbO4 имеет упорядоченную сверхструктуру от структуры типа NaCl [1]. В ней литий и ниобий упорядочены по октаэдрическим позициям. Ниобиевые октаэдры соединены по четыре таким образом, что 4 атома ниобия образуют тетраэдр, причем такие кластеры изолированы (рис. 1).
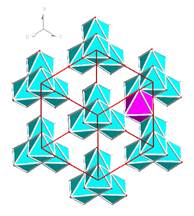
Рисунок 1. Полиэдрическая модель структуры Li 3NbO4
По данным РФА установлено, что образец состава Li3Mn2NbO6 является однофазным. По его дифракционной картине предположили, что соединение имеет структурный тип упорядоченного NaCl [2]. По рентгенограмме были определены параметры ячейки. Затем, по аналогии с изоструктурными фазами, в частности, с фазой Li3Mg2NbO6 [3, 4], методом профильного анализа уточнены структурные параметры. В качестве стартовой модели были использованы координаты атомов Li3Co2TaO6 [5] из порошковых данных, полученных методами рентгеновской и нейтронной дифракции.
Таблица 2.
Координаты атомов и заселенности позиций в структуре Li 3Mn2NbO6
|
Атом |
Позиции Вайкова |
Заселенность |
Координаты атомов |
||
|
x/a |
y/b |
z/c |
|||
|
Nb1 |
8a |
1 |
1/8 |
1/8 |
1/8 |
|
Li1 |
16g |
0,739 |
1/8 |
1/8 |
0,29485 |
|
Mn1 |
16g |
0,262 |
1/8 |
1/8 |
0,29485 |
|
Li2 |
16g |
0,340 |
1/8 |
5/8 |
0,28703 |
|
Mn2 |
16g |
0,660 |
1/8 |
5/8 |
0,28703 |
|
Li3 |
8b |
0,861 |
1/8 |
5/8 |
1/8 |
|
Mn3 |
8b |
0,139 |
1/8 |
5/8 |
1/8 |
|
O1 |
16f |
1 |
1/8 |
0,35410 |
1/8 |
|
O2 |
32h |
1 |
0,11287 |
0,38262 |
0,29781 |
Данный структурный тип достаточно распространен при такой стехиометрии, и реализуется в ряде других соединений [2] (табл. 1). Он представляет собой сверхструктуру каменной соли с изолированными октаэдрами ЭО6, разделяющими общие ребра с 12 соседними октаэдрами (Li/M)O6 (рис. 2).
Результаты уточнения структуры Li3Mn2NbO6 показывают, что достаточно близкие по размерам и зарядам катионы Li+ и Mn2+ частично упорядочены по трем позициям с разной заселенностью. Две из них больше заселены литием, третья — марганцем, причем таким образом, что общее соотношение Li : M = 3 : 2 (табл. 2). Более мелкие катионы Nb5+ сильно отличаются по заряду от остальных катионов. Вследствие этого, они имеют полностью собственные и обособленные позиции в структуре, поскольку максимальное удаление октаэдров с высокозарядными катионами ослабляет силы электростатического отталкивания между ними. Как видно из табл. 3, увеличение объема элементарной ячейки соединения Li3Mn2NbO6 соответствует увеличению радиуса металла М.
Таблица 3.
Параметры ячеек фаз Li 3M2ЭO6, ромбическая сингония, пр.гр. Fddd .
|
Фаза |
a , Å |
b , Å |
c , Å |
V, Å3 |
|
Li3Mg2NbO6 |
5,8952 |
8,5588 |
17,718 |
893,97 |
|
Li3Mg2TaO6 |
5,8020 |
8,8830 |
17,437 |
898,69 |
|
Li3Mg2SbO6 |
5,9080 |
8,6140 |
17,759 |
903,78 |
|
Li3Ni2NbO6 |
5,9069 |
8,4012 |
17,750 |
880,84 |
|
Li3Ni2TaO6 |
5,9073 |
8,4259 |
17,733 |
882,64 |
|
Li3Ni2SbO6 |
5,9071 |
8,3986 |
17,748 |
880,50 |
|
Li3Co2TaO6 |
5,9165 |
8,5715 |
17,778 |
901,56 |
|
Li 3Mn2NbO6 |
6,0016 |
8,8292 |
18,105 |
959,39 |
Судя по ранее приведенным в литературе сведениям, самым крупным катионом M2+ ,обнаруженным в этих структурах является Co2+ (0,885 Å (ВС)). Однако нами установлено, что эти позиции может занимать значительно более крупный катион Mn2+. Этот результат не противоречит, а только дополняет полученные ранее данные, так как в общем случае, возможность существования структурного типа определяется многими факторами, в частности, соотношением радиусов катионов и анионов, и схожими координационными предпочтениями этих ионов. В случае если в структуре имеется более одного вида катионов, всегда есть альтернатива: они могут быть упорядочены, либо разупорядочены.
Полученные нами результаты были сопоставлены с данными исследования аналогичных по составу соединений с другими двухвалентными металлами, приведенными в работе [2]. В этой работе описаны результаты уточнения структур четырех соединений (табл. 3). В каждом из них катионы М частично упорядочены с Li по трем позициям М1(16g), М2(16g) и М3(8b) таким образом, чтобы обеспечить наибольшую удаленность катионов М2+ и Э5+. Однако, степень упорядочения каждого М2+ с Li+ — разная. С одной стороны, чем сильнее отличаются размеры катионов и их эффективные заряды, тем больше вероятность упорядочения. Но эффективный заряд иона зависит от электроотрицательности (ЭО) элемента — чем меньше ЭО элемента М, тем более ионную связь он образует с кислородом, тем больше эффективный заряд иона, тем сильнее он отталкивается от Э5+, и тем выгоднее упорядочение. Учитывая эти две тенденции, можно объяснить разную степень упорядочения двухзарядных катионов внутри одного структурного типа.
Список литературы:
1.Химия твердого тела. Теория и приложения. / Вест А. // В 2-х ч. Ч. 2. Пер. с англ. М.: Мир. 1988. — 336 с.
2. Шукаев И.Л. Твердофазные равновесия, кристаллохимия и ионная проводимость фаз в некоторых тройных системах, содержащих оксиды натрия (лития) и титана (ниобия, тантала): Дис. канд. химич. наук. Ростов-н/Д. 1996. — 217 с.
3.Mather G., Smith R., Skakle J., Fletcher J., Castellanos M., Gutierrez M., West A./ Synthesis and Structures of the Partially Ordered Rock Salt Phases, Li3M2XO6: M = Mg, Co, Ni; X = Nb, Ta, Sb.// Journal of Materials Chemistry. — 1995. — V. 5 — № 8. — PP. 1177—1182.
4.Mather G.C., Smith R.I., Skakle J.M.S., Fletcher J.G., Castellanos M.A.R., Gutierrez M.P., West A.R./ Synthesis and structures of the partially ordered rock salt phases, Li3M2XO6: M=Mg, Co, Ni; X = Nb, Ta, Sb.// Journal of Material Chemistry. — 1995. — V. 5. — PP. 1177—1182.
5.Inorganic Crystal Structure Database. 2.01. 1997.
дипломов

