Статья опубликована в рамках: VI Международной научно-практической конференции «Научные достижения биологии, химии, физики» (Россия, г. Новосибирск, 04 апреля 2012 г.)
Наука: Химия
Секция: Органическая химия
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
СИНТЕЗ И ХРОМАТО-МАСС-СПЕКТРОМЕТРИЯ 1,6-ДИАЛКИЛ-3,4-ДИГИДРОКСИ-2,4-ГЕКСАДИЕН-1,6-ДИОНОВ
Карманова Ольга Геннадьевна
аспирант кафедры химии, ПГПУ, г . Пермь
E-mail:
Козьминых Владислав Олегович
д-р. хим. наук, зав. кафедрой химии, ПГПУ, г. Пермь
E-mail:
Муковоз Петр Петрович
канд. хим. наук, ст. науч. сотр. Института клеточного и внутриклеточного симбиоза ООО РАН, г. Оренбург
E-mail:
Практически значимые 1,6-дизамещенные 1,3,4,6-тетраоксогексаны (3,4-дигидрокси-2,4-гексадиен-1,6-дионы) характеризуются значительным своебразием строения (прототропные формы, кольчато-цепная таутомерия и кольчато-кольчатые интерконверсии), препаративной доступностью и выраженной реакционной способностью по отношению к нуклеофилам [5—7, 9].
В результате сложноэфирной конденсации Клайзена алкилметилкетонов с диэтилоксалатом в присутствии метилата натрия при соотношении реагентов 2:1:2 с последующим подкислением соляной кислотой нами получены целевые 1,6-диалкил-3,4-дигидрокси-2,4-гексадиен-1,6-дионы (1a-g: формы 1А, 1В, 1С) (схема 1) [2—4]. Характеристики и данные ИК и ЯМР 1Н спектроскопии полученных соединений (1a-d) представлены в статье [2].
По данным хромато-масс-спектрометрии в реакционной смеси нами впервые кроме тетракетонов (1) обнаружены побочные продукты: представитель ацилпируватов — метиловый эфир 2-гидрокси-4-оксо-2-пентеновой кислоты (2), а также производное 1,2-циклопентандиона — 3-бутаноил-4-метилциклопент-3-ен-1,2-дион (3). К сожалению, в свободном виде соединения (2) и (3) не получены. Однако при проведении оксалильной конденсации пропанона с 2-пентаноном нам удалось выделить смесь (3Z,5Z)-4,5-дигидроксиокта-3,5-диен-2,7-диона (1a), содержание 60 % и (5Z,7Z)-6,7-дигидроксидодека-5,7-диен-4,9-диона (1с), содержание 40 %. Относительное содержание компонентов по данным хромато-масс-спектрометрии иное, чем непосредственно в смесях, и это обусловлено особенностями метода (см. Экспериментальную часть).
Деструктивные методы исследования тетракетонов (1) для изучения их строения методом масс-спектрометрии, применялись ранее для установления структуры и исследования фрагментации 1,6-диарил-3,4-дигидрокси-2,4-гексадиен-1,6-дионов [8]. Характер и особенности масс-фрагментации 1,6-диалкил-3,4-дигидрокси-2,4-гексадиен-1,6-дионов (1) до наших исследований не изучались.
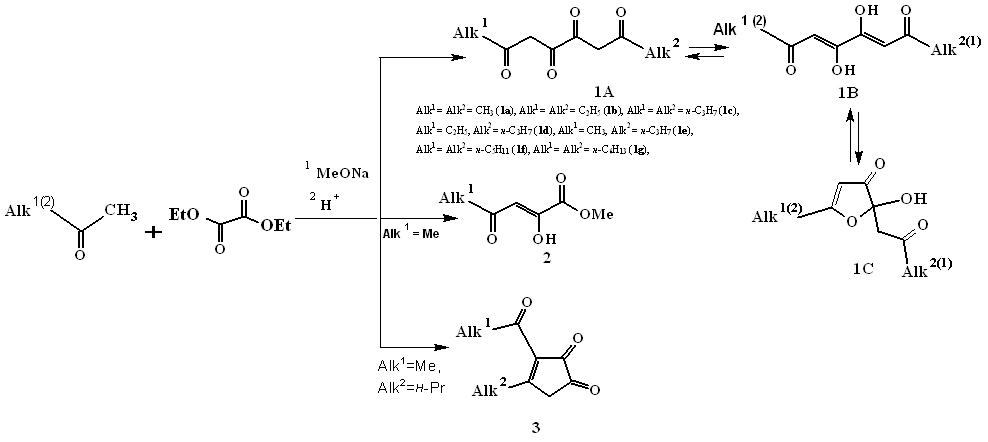
Схема 1
Нами исследованы процессы масс-распада тетракарбонильных соединений с алифатическими заместителями под действием электронного удара с использованием хромато-масс-спектрометрии (схема 2). Для 1,6-диалкил-3,4-дигидрокси-2,4-гексадиен-1,6-дионов (1a-g) преобладающими являются два основных направления фрагментации. Первое направление Ф1 связано с разрывом связи С(3)О — С(4)О с образованием двух равноценных алканоилацетильных звена. Вторым значимым направлением фрагментации является отщепление алканоильного иона с одновременным образованием иона Ф3 (М-Alk1(2)CO+). При этом наиболее интенсивными пиками являются RCOCH2CO+ и RCO+, образующиеся при α-разрыве связей в молекуле. Так, при таком разрыве появляются пики с массовыми числами m/z: 85 MeCOCH2CO+ (1a, 1g), 99 EtCOCH2CO+ (1b, 1d, 1f, 1g), 113 PrCOCH2CO+ (1c, 1d, 1e, 1f, 1g), а также 43 MeCO+ (1a-g), 57 EtCO+ (1b, 1d, 1f, 1g), 71 PrCO+ (1c, 1d, 1e, 1g) (таблица 1).

Схема 2
Сигналы ионов, образующихся при дегидратации молекулярного катион-радикала [М—18]+, со значениями массовых чисел m/z 170 (1b, 1e), 208 (1c), 194 (1d), 264 (1f) свидетельствует о направлении фрагментации с элиминированием молекулы воды из равновесной фрагментируемой структуры (1С). Фрагментный ион Ф7 с малой интенсивностью 0,04—0,56 % образуется в результате декарбонилирования исходного молекулярного иона по механизму скелетной перегруппировки с выбросом молекулы оксида углерода(II). В масс-спектре отмечен пик [М-42], образование которого обусловлено фрагментацией первичного осколка Ф1, сопровождающийся элиминированием кетенового иона (–CH2=C=O+), m/z 42.
Для каждого образующегося в результате фрагментации иона приведены значения формальной ненасыщенности (ФН) [1] и соответствующие им функциональные звенья (таблица). Рассчитанное нами значение ФН позволяет установить строение 1,6-диалкил-3,4-дигидрокси-2,4-гексадиен-1,6-дионов (1a-g). При значении ФН равном 4 возможно существование соединений (1a-g) в виде следующих возможных структур: 1) наличие в молекуле четырех карбонильных групп (форма 1А); 2) наличие в структуре двух карбонильных групп и двух двойных связей С=С (форма 1В); 3) присутствие одного ароматического кольца, двух карбонильных групп и одной двойной связи С=С (форма 1С). Нами выведены общие молекулярные формулы для молекулярного и фрагментных ионов, подходящих для любых алифатических 1,3,4,6-тетракетонов.
Таблица 1
Основные ионы, образующиеся при масс-фрагментации соединений (1), (2), (3) и их характеристики
|
Соединение |
R1 |
R2 |
m/z |
Iотн., |
М+ (Фn+) |
Брутто-формула |
ФН* |
ГИ** |
|
1а |
CH3 |
CH3 |
170 |
2,2 |
M+ |
C8H10O4 |
4 |
2 |
|
142 |
1,3 |
M — CO+ |
C7H10O3 |
3 |
2 |
|||
|
127 |
15,5 |
M — MeCO+ |
C5H5O3 |
4 |
1 |
|||
|
113 |
2,2 |
MeCOCH2COCO+ |
C5H5O3 |
4 |
1 |
|||
|
85 |
100 |
MeCOCH2CO+ |
C4H5O2 |
3 |
1 |
|||
|
69 |
6,6 |
O=C— CH=C=O+ |
C3HO2 |
4 |
13 |
|||
|
55 |
2,1 |
CH2CH=CO+ |
C3H3O |
3 |
13 |
|||
|
43 |
64,4 |
MeCO+ |
C2H3O |
3 |
1 |
|||
|
1b |
C2H5 |
C2H5 |
198 |
0,19 |
M+ |
C10H14O4 |
4 |
2 |
|
169 |
0,20 |
M — CO — H+ |
С9H13O3 |
4 |
1 |
|||
|
170 |
1,05 |
M — H2O+ |
C10H12O3 |
5 |
1 |
|||
|
155 |
0,08 |
M — CH2CO+ |
C8H12O3 |
3 |
1 |
|||
|
141 |
11,13 |
EtCOCH2COCO+ |
C7H9O3 |
4 |
1 |
|||
|
99 |
100 |
EtCOCH2CO+ |
C5H7O2 |
3 |
1 |
|||
|
98 |
0,34 |
½ M — H+ |
C5H6O2 |
3 |
0 |
|||
|
71 |
2,33 |
EtCOCH2+ |
C4H5O2 |
3 |
1 |
|||
|
57 |
27,21 |
EtCO+ |
C3H5O |
2 |
1 |
|||
|
43 |
13,0 |
MeCO+ |
C2H3O |
2 |
1 |
|||
|
1c |
C3H7 |
C3H7 |
226 |
0,04 |
M+ |
C12H18O4 |
4 |
1 |
|
208 |
0,04 |
M — H2O+ |
C12H16O3 |
5 |
12 |
|||
|
199 |
0,56 |
M — CO+ |
C11H18O3 |
3 |
3 |
|||
|
184 |
0,08 |
M — CH2CO+ |
C10H16O3 |
3 |
2 |
|||
|
155 |
7,83 |
M — PrCO+ |
C8H11O3 |
4 |
1 |
|||
|
113 |
100 |
PrCOCH2CO+ |
C6H9O2 |
3 |
1 |
|||
|
112 |
1,54 |
½ M — H+ |
C6H8O2 |
3 |
0 |
|||
|
85 |
0,50 |
PrCOCH2+ |
C5H9O |
2 |
1 |
|||
|
71 |
16,30 |
PrCO+ |
C4H7O |
2 |
1 |
|||
|
43 |
21,71 |
MeCO+ |
C2H3O |
2 |
1 |
|||
|
1d |
C2H5 |
C3H7 |
212 |
0,17 |
M+ |
C11H16O4 |
4 |
2 |
|
194 |
0,06 |
M — H2O+ |
C11H14O3 |
5 |
2 |
|||
|
184 |
1,33 |
M — CO+ |
C10H16O3 |
3 |
2 |
|||
|
183 |
0,18 |
M — СО —Н+ |
C10H15O3 |
4 |
1 |
|||
|
170 |
0,05 |
M — CH2CO+ |
C9H14O3 |
3 |
1 |
|||
|
169 |
0,21 |
M—CH2CO—Н+ |
C9H13O3 |
4 |
1 |
|||
|
155 |
8,59 |
EtCOCH2COCO+ |
C8H11O3 |
4 |
1 |
|||
|
141 |
7,83 |
PrCOCH2COCO+ |
C7H9O3 |
4 |
1 |
|||
|
113 |
100 |
PrCOCH2CO+ |
C6H9O2 |
3 |
1 |
|||
|
112 |
1,91 |
½ M — H+ |
C5H7O4 |
3 |
0 |
|||
|
99 |
82,20 |
EtCOCH2CO+ |
C5H7O2 |
3 |
1 |
|||
|
71 |
17,40 |
PrCO+ |
C4H7O |
2 |
1 |
|||
|
57 |
24,60 |
EtCO+ |
C3H5O |
2 |
1 |
|||
|
43 |
30,35 |
MeCO+ |
C2H3O |
2 |
1 |
|||
|
1e |
CH3 |
C3H7 |
198 |
0,31 |
M+ |
C10H14O4 |
4 |
2 |
|
170 |
1,41 |
M — H2O+ |
C10H12O3 |
5 |
1 |
|||
|
155 |
8,69 |
MeCOCH2COCO+ |
C8H11O3 |
4 |
1 |
|||
|
127 |
6,28 |
PrCOCH2COCO+ |
C6H7O3 |
4 |
1 |
|||
|
113 |
100 |
PrCOCH2CO+ |
C6H9O2 |
3 |
1 |
|||
|
112 |
1,14 |
½ M — H+ |
C5H6O2 |
3 |
0 |
|||
|
85 |
58,45 |
MeCOCH2CO+ |
C4H5O2 |
3 |
1 |
|||
|
71 |
13,91 |
PrCO+ |
C4H7O |
2 |
1 |
|||
|
43 |
54,23 |
MeCO+ |
C2H3O |
2 |
1 |
|||
|
1f |
C5H11 |
C5H11 |
282 |
2,32 |
M+ |
C16H26O4 |
4 |
2 |
|
264 |
1,32 |
M — H2O+ |
C16H24O3 |
5 |
12 |
|||
|
236 |
0,48 |
M — CO — H2O+ |
C15H24O2 |
4 |
1 |
|||
|
211 |
1,13 |
PrCOCH2COCO+ |
C12H19O3 |
4 |
1 |
|||
|
183 |
6,71 |
M - EtCOCH2CO+ |
C11H19O2 |
3 |
1 |
|||
|
141 |
100 |
C5H11COCH2CO+ |
C8H14O2 |
3 |
1 |
|||
|
113 |
1,84 |
PrCOCH2CO+ |
C6H9O2 |
3 |
1 |
|||
|
99 |
7,35 |
EtCOCH2CO+ |
C5H7O2 |
3 |
1 |
|||
|
71 |
9,45 |
EtCO+ |
C3H5O |
2 |
1 |
|||
|
43 |
11,87 |
MeCO+ |
C2H3O |
2 |
1 |
|||
|
1g |
C6H13 |
C6H13 |
310 |
1,92 |
M+ |
C18H30O4 |
4 |
2 |
|
282 |
0,83 |
M — CO+ |
C17H30O3 |
3 |
2 |
|||
|
264 |
0,64 |
M — CO — 2H+ |
C17H28O3 |
4 |
12 |
|||
|
212 |
0,32 |
M - EtCOCH2CO+ |
C13H23O2 |
3 |
2 |
|||
|
197 |
11,23 |
M - PrCOCH2CO+ |
C12H21O2 |
3 |
1 |
|||
|
155 |
100 |
C6H13COCH2CO+ |
C9H15O2 |
3 |
1 |
|||
|
113 |
8,56 |
PrCOCH2CO+ |
C6H9O2 |
3 |
1 |
|||
|
99 |
2,23 |
EtCOCH2CO+ |
C5H7O2 |
3 |
1 |
|||
|
85 |
3,42 |
MeCOCH2CO+ |
C4H5O2 |
3 |
1 |
|||
|
71 |
6,28 |
PrCO+ |
C4H7O |
2 |
1 |
|||
|
43 |
17,83 |
MeCO+ |
C2H3O |
2 |
1 |
* ФН — формальная ненасыщенность [1].
** ГИ — гомологический индекс [1].
Работа выполнена в рамках диссертационного исследования аспиранта кафедры химии Пермского государственного педагогического университета Кармановой О. Г.
Экспериментальная часть
Общая методика синтеза 1,6-диалкил-3,4-дигидрокси-2,4-гексадиен-1,6-дионов (1a-g). К 100 мл метанола, предварительно перегнанного над натрием, добавляют порциями 1,15 г (50 ммоль) натрия, метанол отгоняют, к сухому метилату натрия добавляют 150 мл абсолютного диэтилового эфира, при охлаждении и перемешивании прибавляют по каплям смесь 3,7 мл (50 ммоль) пропанона (для синтеза соединения 1а), 4,4 мл (50 ммоль) бутанона (для синтеза соединения 1b), 5,3 мл (50 ммоль) 2-пентанона (для синтеза соединения 1c), 2,2 мл (25 ммоль) бутанона и 2,7 мл (25 ммоль) 2-пентанона (для синтеза соединения 1d), 1,9 мл пропанона (25 ммоль) и 2,9 мл 2-пентанона (25 ммоль) (для синтеза соединения 1е), 5,2 мл 2-гептанона (для синтеза соединения 1f), 7,8 мл 2-октанона (50 ммоль) (для синтеза соединения 1g) и 3,4 мл (25 ммоль) диэтилоксалата и нагревают 1—2 часа. Осадок отфильтровывают, добавляют при перешивании и охлаждении 15 мл 15 % соляной кислоты, продукт кристаллизуют из этилацетата. Получают бесцветные кристаллы соединений (1a—g).
Хромато-масс-спектры записаны на приборе Agilent Technologies 6890 N/5975 В, колонка HP-5ms, 30 м х 0,25 мкм, газ-носитель — гелий (1 мл/мин), ионизация электронным ударом (70 эВ).
(3Z,5Z)-4,5-дигидроксиокта-3,5-диен-2,7-дион (1a), (5Z,7Z)-6,7-дигидроксидодека-5,7-диен-4,9-дион (1с) и 3-ацетил-4-пропил-3-циклопентен-1,2-дион (3).
Константы, выходы и спектральные характеристики индивидуальных соединений (1а) и (1с) описаны в статье [2]. По данным ЯМР 1Н смесь компонентов (1а) и (1с) выделена в соотношении 60 % и 40 %, соответственно. Хромато-масс-спектр, время удерживания, мин.: компонент (1а) 5,6 мин., компонент (1е) 6,5 мин., компонент (1с) 7,3 мин., компонент (3) 6,3 мин. Mасс-спектрометрические данные соединений (1а) и (1с) приведены в таблице.
Соединение (3), масс-спектр, m/z (I, %): 180 (10,16) М+, 165 (4,52) М — Ме+, 152 (15,43) M — Me+, 137 (37,16) M — Pr+, 123 (5,21) M — CO — H+, 109 (16,89) M — PrCO+, 95 (13,20) MeCOCH=C=O+, 82 (100) ![]() , 67 (14,12) C6H10 — Me+, 55 (12,23), С3Н3О+, 43 (9,2) Pr+, 41 (23,1) CH=C=O+.
, 67 (14,12) C6H10 — Me+, 55 (12,23), С3Н3О+, 43 (9,2) Pr+, 41 (23,1) CH=C=O+.
(4Z,6Z)-5,6-дигидроксидека-4,6-диен-3,8-дион (1b), (5Z,7Z)-6,7-дигидроксидодека-5,7-диен-4,9-дион (1с), (4Z,6Z)-5,6-дигидроксиундека-4,6-диен-3,8-дион (1d).
Константы, выходы и спектральные характеристики индивидуальных соединений (1b, 1c, 1d) представлены в статье [2].
Хромато-масс-спектр, время удерживания, мин.: компонент (1b) 6,5 мин., компонент (1d) 6,9 мин., компонент (1с) 7,3 мин. Mасс-спектрометрические результаты исследования идентифицированных соединений приведены в таблице.
Список литературы:
- Иоффе Б. В., Костиков Р. Р., Разин В. Ф. Физические методы определения строения органических соединений. М., Высшая школа, 1984, 336 с.
- Карманова О. Г., Козьминых В. О., Муковоз П. П., Козьминых Е. Н. Синтез и структурное разнообразие 1,6-диалкил-3,4-дигидрокси-2,4-гексадиен-1,6-дионов // Известия высших учебных заведений. Химия и химическая технология. Иваново: ИГХТУ, 2012 (в печати, рег. номер 4413).
- Карманова О. Г., Зыкова С. С., Муковоз П. П., Козьминых В. О. Новый модифицированный метод получения 1,6-диалкилзамещенных 3,4-дигидрокси-1,6-гексадиен-1,6-дионов // Современные фундаментальные и прикладные исследования. Кисловодск, 2011. С. 106—109.
- Карманова О. Г., Зыкова С. С., Козьминых В. О., Муковоз П. П. Синтез и особенности строения 1,6-диалкилзамещенных 1,3,4,6-тетраоксогексанов // Научное творчество XXI века. Том 3. Красноярск, 2012. С. 264—269.
- Кириллова Е. А., Козьминых В. О. Синтез, цепная таутомерия и кольчато-цепные интерконверсии замещённых 3,4-дигидрокси-2,4-алкадиен-1,6-дионов // Вестник Южно-Уральского гос. ун-та. Серия "Химия". Вып. 2. Челябинск, 2009. № 23 (156). С. 9—15.
- Кириллова Е. А., Муковоз П. П., Виноградов А. Н., Козьминых В. О., Дворская О. Н. Синтез, особенности строения и таутомерия 1,6-дизамещённых 3,4-дигидрокси-2,4-гексадиен-1,6-дионов // Известия высших учебных заведений. Химия и химическая технология. Иваново: ИГХТУ, 2011. Т. 54. № 4. С. 18—22.
- Козьминых В. О., Гончаров В. И., Козьминых Е.Н. Конденсация Клайзена метилкетонов с диалкилоксалатами в синтезе биологически активных карбонильных соединений (обзор, часть 3) // Вестник Оренбургского гос. ун-та. Оренбург, 2007. Вып. 5 (69). С. 138—148.
- Laćan М., Vukićević М., Džanić Н., Stefanović D. The mass spectra of some aromatic polyketones // Org. Mass Spectrom. — 1975. — N 10. — P. 899—904.
- Poje M., Balenović К. 3(2H)-Furanone derivatives. Ring-chain tautomerism in the 1,3,4,6-tetraketone // J. Heterocycl. Chem. — 1979. — Vol. 16. — N 3. — P. 417—420.
дипломов
