Статья опубликована в рамках: V Международной научно-практической конференции «Научные достижения биологии, химии, физики» (Россия, г. Новосибирск, 06 марта 2012 г.)
Наука: Биология
Секция: Биохимия
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
РОЛЬ АНТИОКСИДАНТНОЙ СИСТЕМЫ И ОКСИДА АЗОТА В ФОРМИРОВАНИИ СТРЕСС-ИНДУЦИРОВАНОЙ ЯЗВЫ ЖЕЛУДКА У КРЫС.
Остапченко Людмила Ивановна
д-р биол. наук, профессор, Киевский национальный университет им. Т. Шевченко, г. Киев
E-mail:
Сокур Олеся Вадимовна
канд. биол. наук, ст. науч. сотр., Киевский национальный университет им. Т. Шевченко, г. Киев
E-mail:
Максимович Ярослава Сергеевна
канд. биол. наук, мл. науч. сотр., Киевский национальный университет им. Т. Шевченко, г. Киев
Язвенная болезнь желудкапредставляет собой хроническое рецидивирующее заболевание, протекающее с чередованием периодов обострения и ремиссии, основным признаком которого является образование дефекта (язвы) в стенке желудка и двенадцатиперстной кишки. Согласно данным мировой статистики язвой желудка и двенадцатиперстной кишки страдает 6—10 % взрослого населения, приблизительно у половины из них в течение 5 лет возникает обострение. Патогенез этого заболевания можно представить в виде единого процесса, "пусковым моментом" которого является стрессорное воздействие на организм, а его последствия определяются степенью выраженности различных типов компенсаторных реакций, то есть индивидуальными особенностями адаптационного синдрома [1]. Универсальным механизмом адаптации и повреждения клеточных систем является окислительный стресс. Важную роль в ограничении повреждений при стрессе играют относящиеся к локальным стресс-лимитирующим системам антиоксидантная система в органах и тканях, включающая антиоксидантные ферменты (каталазу, супероксиддисмутазу). Они угнетают высвобождение катехоламинов из нервных окончаний и надпочечников, а также действие этих моноаминов на постсинаптическом уровне, уменьшая тем самым активацию свободнорадикального окисления (СРО) и ограничивая чрезмерную стресс-реакцию и ее повреждающее действие на органы и ткани [5]. В последнее время появились экспериментальные и теоретические данные, позволяющие причислить к стресс лимитирующим системам систему генерации оксида азота (NO), участвующую в широком спектре физиологических и патологических процессов. Установлено, что NO способен ограничивать повреждающее действие стресс реакции путем прямого уменьшения стрессорной активности свободнорадикального окисления за счет увеличения активности антиоксидантных ферментов. Оксид азота является локальным тканевым гормоном в париетальных клетках желудка, поддерживающим активную вазодилатацию, и одним из основных факторов, регулирующих кровоток [6]. Поэтому, изучение состояния стресс-лимитирующих систем в динамике развития стресс-индуцированных поражений желудка является актуальной проблемой современной биохимии.
Материалы и методы.Исследования проводили на самцах нелинейных белых крыс массой 250—270 г. Экспериментальную язву желудка у подопытных животных вызывали с помощью иммобилизационного водно-иммерсионного стресса [8]. Животных убивали методом дислокации шейных позвонков после 0,5, 1, 2, 3 часового действия стресса. Визуально исследовали состояние слизистой желудка крыс и рассчитывали степень и индекс язвенного повреждения используя систему балов. Определение активности NO-синтазы проводили согласно метода [3]. Содержание нитрит-ионов определяли методом Грисса с модификациями [2], пероксинитрита – методом регистрации пероксинитритзависимого окисления дигидрородамина 123 до родамина 123, который способен к флуоресценции [4]. Содержание ТБК-активных продуктов, активность супероксиддисмутазы и каталазы определяли общепринятыми методами.
Результаты и обсуждение.Проведенные нами исследования показали, что в динамике развития стресс-индуцированных поражений желудка возрастает уровень ТБК- активних продуктов (табл. 1). Так, уже через 0,5 ч действия стресса зафиксировано повышение содержания вторичных продуктов окисления липидов на 20 % в сравнении с контрольными величинами. Более длительное действие повреждающего фактора вызывало увеличение количества ТБК-активных продуктов на 94, 125 %, а через 3 часа достигал максимального значения (на 200 % больше контрольных значений).
Таблица 1.
Содержание ТБК-активных продуктов и активность антиоксидантных ферментов в динамике развития стресс-индуцированных поражений желудка крыс
|
Показатель |
Контроль |
Стресс, часы |
|||
|
0,5 |
1 |
2 |
3 |
||
|
ТБК-АП, нмоль/мг белка |
95,67± 8,07 |
114,98± 9,03 |
185,45± 15,45 |
215,57± 17,88 |
287,01± 22,45 |
|
СОД, у.е/мин∙мг белка |
0,185± 0,016 |
0,175± 0,015 |
0,15± 0,014* |
0,139± 0,012* |
0,123± 0,011* |
|
Каталаза, мкмоль Н2О2/мин∙мг белка |
4,92± 0,43 |
5,23± 0,48 |
6,02± 0,59* |
6,87± 0,61* |
7,38± 0,69* |
* - р£0,05 по сравнению с контролем
Поскольку структурным основанием клеточных мембран есть липидный бислой, избыточное образование продуктов перекисного окисления липидов (ПОЛ) оказывает повреждающее действие на уровне клеток. Перекисные радикалы взаимодействуют с молекулами жирных кислот, образуя высокотоксичные гидроперекиси и новый свободный радикал. Такой лавинообразный процесс формирует новые цепи окисления продуктов ПОЛ, непрерывное накопление которых дестабилизирует мембраны.Рядом авторов показано, что инициация ПОЛ вызывает нарушение конформации и повышение проницаемости клеточных мембран, выход ферментов из митохондрий и лизосом, инактивацию аэробного окисления, торможение окислительного фосфорилирования в дыхательной цепи митохондрий [10]. Потеря липидными молекулами мембран белкового покрытия приводит к усиленному проникновению кислорода и прооксидантов, что способствует обратной диффузии ионов водорода через слизистую оболочку желудка [9].
Накопление ТБК- активних продуктов является результатом несоответствия между возможностями антиоксидантных ферментов и скоростью свободнорадикального окисления. Об этом свидетельствует отмеченное нами компенсаторное увеличение каталазной активности (на 22, 40 та 50 %) направленную на инактивацию H2О2. Следует отметить, что параллельное снижение активности СОД (19 %, 25 % и 34 %) приводит к усиленному образованию гидроперекисей липидов и снижет эффективность антирадикальной защиты. Несмотря на то, что СОД является весьма стабильным ферментом, ее активность может ингибироваться H2O2 или супероксидными радикалами (продуцируемыми ксантиноксидазой) по принципу обратной связи [7].
Обращает на себя тот факт, что изменение активности СОД в ответ на стрессовые воздействия имело одинаковую направленность с изменение продукции оксида азота. В ходе эксперимента (рис. 1, рис. 2) было установлено возрастание активности NO-синтазы (на 234, 485 и 670 %) и как результат увеличение содержания нитрит иона (NO-2) на 191, 396 и 575 %. Повышенный уровень NO неизбежно опосредует участие этого метаболита в свободнорадикальных реакциях (происходит накопление активных форм кислорода). Вследствие этого возрастает уровень пероксинитрит-аниона (ONOO-) который являясь сильным окислителем, может приводить к образованию гидроксильного радикала (ОН.) и активировать ПОЛ [11].
При этом наиболее значительный прирост образования пероксинитрита (на 47 %) установлен после 3-часового влияния стрессового фактора (рис. 3). Считается, что цитотоксические свойства пероксинитрита определяются его распадом с образованием гидроксильного радикала и диоксида азота [11].
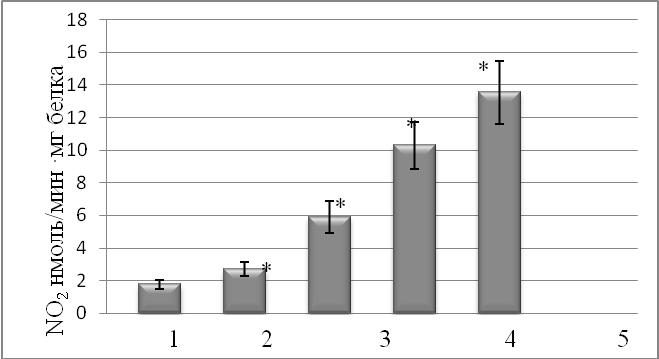
Рис. 1. NO-синтазная активность в клетках слизистой оболочки желудка крыс в условиях развития стресс-индуцированнх повреждений желудка
|
1– контроль, |
2 – 30 мин стресса, |
3 – 1 час стресса, |
4 – 2 часа стресса, |
5 - 3 часа стресса
* - р£0,05 по сравнению с контролем
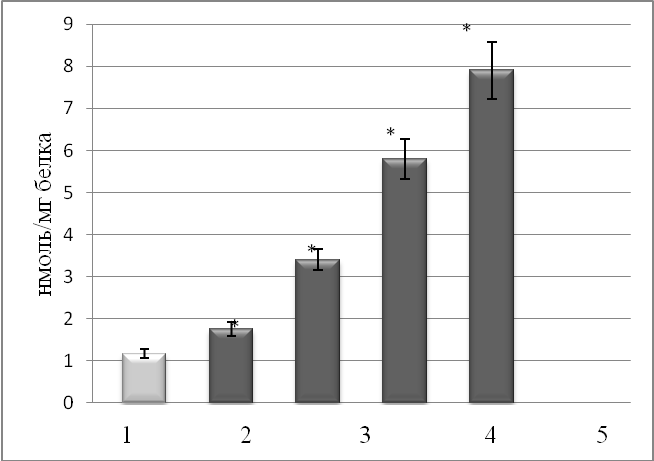
Рис. 2 Содержание нитрит-иона в клетках слизистой оболочки желудка в условиях развития стресс-индуцированных повреждений
|
1– контроль, |
2 – 30 мин стресса, |
3 – 1 час стресса, |
4 – 2 часа стресса, |
|
|
5 – 3 часа стресса |
|
|||
* - р£0,05 по сравнению с контролем
Возникающие при этой реакции свободные радикалы могут окислять липиды, белки и ДНК. Пероксинитрит способен инициировать свободнорадикальные реакции, способствует вазоконстрикции, агрегации и адгезии лейкоцитов. Инициирование этих процессов приводит к нарушению микроциркуляции, активации циклооксигеназы (основного фермента синтеза простагландинов) и как результат к тканевой гипоксии вследствие снижения регионарного кровотока [11].
Необходимо отметить, что активация NO-системы и процессов липопероксидации на фоне разобщенной работы основных ферментов антиоксидантной защиты коррелировало с интенсификацией процесс сов ульцерогенеза приводит и язвенным поражениям слизистой оболочки желудка крыс. Нами установлено, что в зависимости от срока действия стрессового фактора увеличивалась степень поражения ткани желудка. Так, через 1 час количество и площадь язв (мм2) была 1,3±0,28 и 2,16±0,31, через 2 часа - 5,0±0,98 и 8,38±1,78, через 3 часа - 10,5±1,7 17,68±3,5 из расчета на 1 желудок. При этом были зафиксированы массовые кровоизлияния в просвет желудка.
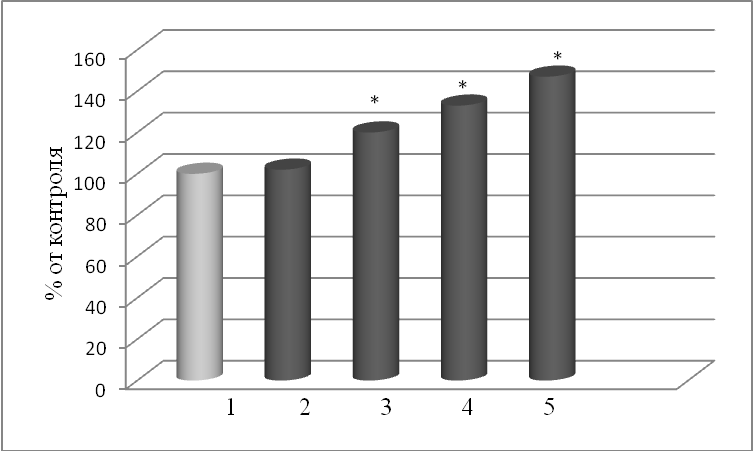
Рис 3. Содержание пероксинитрита в клетках слизистой оболочки желудка при действии стресса
1 – контроль, 2 – 30 мин стресса, 3 – 1 час стресса, 4 - 2 часа стресса, 5 – 3 часа стресса
* - р£0,05 по сравнению с контролем
Таким образом, анализируя данные литературы и результаты собственных исследований, можно предположить, что одной из основных причин, ведущих к снижению резистентности и развитию стресс-индуцированных поражений желудка является нарушение процесса становления и последующего согласованного взаимодействия антиоксидантной и NO-эргической стресс-лимитирующих систем, обеспечивающих поддержание адекватного метаболического статуса в организме.
Список литературы:
- Язвенная болезнь / Под ред. Ю. Ю. Елисеева. – М.: КРОН-ПРЕСС, 2000. – 304 с.
- Green L. C., David A. W., Glosgowski J. [et al.] Analysis of nitrate, nitrit and [15N] nitrate in biological fluids // Anal. Biochem. – 1982. – 126, N 1. – Р. 131—138.
- Hevel J. M., White K. A., Marletta M. A. Purification of the inducible murine macrophage nitric oxide synthase // J. Biol. Chem. – 1991. – V.266, №34. – P. 22789—22791.
- Kooy N. W. Oxidation of 2',7'-dichlorofluorescin by peroxynitrite / Kooy N.W., Royall J.A., Ischiropoulos H. // Free Radic Res. – 1997. – Vol .27. – Р. 245—254.
- Kountouras J, Chatzopoulos D, Zavos C. Reactive oxygen metabolites and upper gastrointestinal diseases // Hepatogastroenterology. – 2001. – Vol. 48, № 39. – P. 743—751.
- Kwiecie Ò. S, Brzozowski T., Konturek P. Ch. [et al.] The role of reactive oxygen species in action of nitric oxide–donors on stress–induced gastric mucosal lesions // J. Physiol. Pharmacol. – 2002. – Vol. 53. – P. 761—773.
- Liochev S., Fridowich I. Copper, Zinc Superoxide Dismutase and H2O2 // The Journal of biological chemistry. – 2002. – Vol. 277, № 38. – P. 34674—3468.
- Takagi K., Okabe S. The effects of drugs on the production and recovery processes of the stress ulcer // Jpn. J. Pharmacol – 1968. – Vol. 18. – P. 918.
- Tandon R., Khanna H. D., Dorababu M. Oxidative stress and antioxidants status in peptic ulcer and gastric carcinoma // Indian. J. Physiol. Pharmacol.–2004. – Vol. 48, № 1. – P. 115—8.
- Toyokuni S. Reactive oxygen species–induced moleculer damage and its application in pathology // Pathol. Int. – 1999. – Vol. 49. – P. 91—102.
- Trujillo M. Peroxynitrite detoxification and its biologic implications / Trujillo M., Ferrer-Sueta G., Radi R. // Antioxid. Redox. Signal. – 2008. – Vol. 10, № 9. – P. 1607—1620.
дипломов
