Статья опубликована в рамках: XXVII Международной научно-практической конференции «Современная медицина: актуальные вопросы» (Россия, г. Новосибирск, 15 января 2014 г.)
Наука: Медицина
Секция: Организация фармацевтического дела
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
ОСОБЕННОСТИ ФОРМИРОВАНИЯ ТЕРРИТОРИАЛЬНОЙ СИСТЕМЫ УПРАВЛЕНИЯ КАЧЕСТВОМ ОБРАЩЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ НА ПРИМЕРЕ ВОРОНЕЖСКОЙ ОБЛАСТИ
Лаврова Надежда Николаевна
соискатель кафедры организации и экономики фармации Пятигорского медико-фармацевтического института-филиала ГБОУ ВПО ВолгГМУ Минздрава России, РФ, г. Пятигорск
E-mail: lavrova.05@mail.ru
Гацан Владимир Владимирович
д-р фармацевтических наук, профессор, зав. кафедрой организации и экономики фармации Пятигорского медико-фармацевтического института-филиала ГБОУ ВПО ВолгГМУ Минздрава России, РФ, г. Пятигорск
.
PECULIARITIES OF FORMATION OF THE TERRITORIAL SYSTEM OF QUALITY CONTROL OF THE CIRCULATION OF MEDICINES ON THE EXAMPLE OF VORONEZH REGION
Lavrova Nadezhda
applicant of the Department of organization and economics of pharmacy of Pyatigorsk medico-pharmaceutical Institute, Russia Pyatigorsk
Gatsan Vladimir
doctor of Pharmaceutical Science, professor, head of the Department of organization and economics of pharmacy of Pyatigorsk medico-pharmaceutical Institute, Russia Pyatigorsk
АННОТАЦИЯ
В современных условиях роль системы контроля качества фармацевтической продукции имеет особое значение. Целью настоящего исследования был анализ эффективности работы территориальной системы управления качеством обращения лекарственных средств. Объектами являлись статистические данные по информационно-аналитическому мониторингу качества лекарственных средств на территории Воронежской области за период с 2001 г. по сентябрь 2013 г. Проведенное исследование свидетельствуют о тенденции уменьшения количества выявленных недоброкачественных и фальсифицированных лекарственных средств на территории области.
ABSTRACT
In modern conditions the role of the system of quality control of pharmaceutical products has a special importance. The purpose of this study was to analyze the efficiency of the work of territorial system of quality control of medicines. The objects include statistical data of information-analytical monitoring the quality of medicines on the territory of the Voronezh region for the period from 2001 to September 2013. This study shows a reduction of the number of substandard and counterfeit medicines on the territory of the region.
Ключевые слова: лекарственное средство; контроль качества; сертификация.
Keywords: medicine; quality control; certification.
Повышение качества лекарственного обеспечения населения и медицинских организаций является приоритетным направлением деятельности фармацевтической службы для реализации национальной политики в сфере здравоохранения.
Историко-правовой анализ эволюции государственной системы лекарственной помощи свидетельствует о необходимости обеспечения качества фармацевтической продукции посредством контрольно-надзорных мероприятий. Так, Указом Петра I от 1721 года приоритетными были признаны вопросы регулирования цен на лекарственные средства (ЛС) и системного контроля над деятельностью аптек [1, с. 22]. Значительным этапом развития системы управления фармацевтическим рынком с позиции качества продукции стало издание в 1789 г. Аптекарского устава, в котором предусматривалось ведение реестра разрешенных к применению лекарств. Контроль качества ЛС во второй половине XX века претерпел существенные изменения, обусловленные резким увеличением количества используемых в практической деятельности медикаментов как отечественного, так и зарубежного происхождения.
В современных условиях значительного роста фармацевтического рынка, в том числе за счет нелегальной, фальсифицированной продукции, информатизации общества, создания условий межгосударственной торговли роль системы контроля качества лекарственных средств приобретает особое значение. В настоящее время государственный надзор в сфере обращения ЛС, согласно Федеральному закону № 61-ФЗ от 12.04.2010 «Об обращении лекарственных средств», отнесен к компетенции федеральных органов исполнительной власти и включает в себя, в том числе, лицензионный контроль в сфере фармацевтической деятельности [3, с. 4].
Объем и структура фармацевтического рынка России обуславливают необходимость построения на территориальном уровне системы, осуществляющей мониторинг качества и безопасности ЛС и, тем самым, обеспечивающей присутствие на региональном рынке эффективных медикаментов, с гарантированным, стабильно высоким уровнем качества, соответствующим ожиданиям потребителей.
Основными исполнительными элементами системы, отвечающей за своевременное выявление и предупреждение реализации недоброкачественной фармацевтической продукции, являются органы управления здравоохранением субъектов Российской Федерации и, непосредственно, фармацевтические организации, осуществляющие деятельность на всех этапах обращения ЛС — от стадии производства до реализации конечным потребителям. Достичь максимальной эффективности во всех аспектах деятельности любой фармацевтической организации в целях обеспечения потребителей лекарственными средствами требуемого уровня качества позволяет формирование и внедрение Системы менеджмента качества (СМК) на базе постоянно эволюционирующих международных стандартов ISO серии 9000 [2, .с 34].
В российской системе сертификации стандарты, входящие в серию ISO 9000, имеют аналоги в виде государственных стандартов ГОСТ ISO 9000:2011, ГОСТ ISO 9001:2011 и ГОСТ Р ИСО 9004:2010. Стандарты ISO предусматривают варианты общепризнанных требований, предъявляемых к СМК организации для обеспечения необходимого уровня качества предоставления услуг.
Документом, подтверждающим проведение независимой и квалифицированной оценки соответствия СМК организаций, осуществляющих деятельность в сфере обращения лекарственных средств, установленным требованиям нормативных актов, определяющих модель системы качества, является сертификат, выданный соответствующим органом по сертификации.
Впервые в России, на территории Воронежской области разработана и внедрена Система добровольной сертификации «Фармконтроль» (свидетельство о регистрации от 21.06.2011 г. выдано Федеральным агентством по техническому регулированию и метрологии), предусматривающая стандартизацию СМК фармацевтических и медицинских организаций.
В ходе настоящего исследования был проведен анализ эффективности работы территориальной системы управления качеством обращения лекарственных средств.
В качестве объектов были использованы статистические данные БУЗ ВО «Воронежский центр контроля качества и сертификации лекарственных средств» (ЦКК и СЛС) по информационно-аналитическому мониторингу качества лекарственных средств на территории Воронежской области за период с 2001 г. по сентябрь 2013 г.
Исследование результатов производственной деятельности БУЗ ВО «ЦКК и СЛС» показало, что с 2001 по сентябрь 2013 г. на территории Воронежской области обнаружено в реализации 1359 партий недоброкачественных ЛС на общую сумму 12 229 838,92 руб. Графически полученные результаты приведены в нормированных показателях на рис. 1.

Рисунок 1. Графический анализ выявленных на территории Воронежской области недоброкачественных лекарственных средств в 2001—2013 гг.
За анализируемый период на территории области приняты меры к изъятию из обращения 216 партий фальсифицированных ЛС на общую сумму 16 127 425,5 руб., причем наибольшее их количество было отмечено в 2003 г. (58) и в 2005 г. (49), а наименьшее количество — в 2008, 2012 и 2013 годах — по одному наименованию. Динамика выявленных на территории Воронежской области фальсифицированных лекарственных средств в 2001—2013 гг. в нормированных показателях представлена на рис. 2.
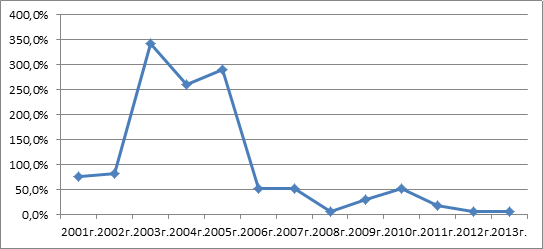
Рисунок 2. Графический анализ выявленных на территории Воронежской области фальсифицированных лекарственных средств в 2001—2013 гг.
Анализ динамики количества выданных сертификатов по Системе «Фармконтроль» организациям, участвующим в обороте лекарственных средств на различных стадиях жизненного цикла продукции, позволил установить, что в общей структуре выданных сертификатов за 2011 г. — сентябрь 2013 г. наибольший удельный вес имеют розничные фармацевтические организации (65 %, или 103 сертификата из 158), меньше сертификатов было выдано медицинским организациям (27 %, или 43) и оптовым фармацевтическим компаниям (8 %, или 12). Анализ изменения количества выданных сертификатов в разрезе 2011—2013 гг. выявил увеличение их количества в 2012 г. в 2,4 раза по сравнению с предыдущим годом.
Таблица 1.
Количество выданных сертификатов по Системе «Фармконтроль» за 2001—2013 гг.
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таким образом, проведенное исследование свидетельствуют о положительной тенденции уменьшения количества выявленных недоброкачественных и фальсифицированных лекарственных средств на территории области за последнее время, что подтверждает обоснованность внедрения Системы добровольной сертификации и позволяет сделать вывод о необходимости системного подхода к разработке модели управления качеством обращения лекарственных средств на территориальном уровне.
Список литературы:
1.Гусаков Н.И. Петр I и медицина (очерк). М., 1994. — 47 с.
2.Никитин В.А., В.В. Филончева Управление качеством на базе стандартов ИСО 9000:2000. СПб.: Питер, 2005. — 126 с.
3.Федеральный закон Российской Федерации от 12.04.2010 № 61-ФЗ «Об обращении лекарственных средств» (в ред. от 25.06.2012).
дипломов

