Статья опубликована в рамках: XVI Международной научно-практической конференции «Современная медицина: актуальные вопросы» (Россия, г. Новосибирск, 11 марта 2013 г.)
Наука: Медицина
Секция: Кардиология
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
ПОЧЕЧНАЯ ДИСФУНКЦИЯ КАК МАРКЕР НЕБЛАГОПРИЯТНОГО ТЕЧЕНИЯ ХРОНИЧЕСКОЙ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА
Филипюк Анжелика Левоновна
канд. мед. наук,и.о.доцента ЛНМУ, г. Львов
Е-mail: Filipyuk_a@ukr.net
Актуальность темы. Ишемическая болезнь сердца (ИБС) в настоящее время является основной причиной смертности от болезней системы кровообращения [1], что требует поиска информативных прогностических критериев ее течения. Дисфункция почек является независимым фактором риска неблагоприятного течения ИБС у больных, перенесших острый инфаркт миокарда, часто ассоциируется с сахарным диабетом (СД), артериальной гипертензией (АГ), сердечной недостаточностью (СН), развитием повторного инфаркта міокарда [2, 3, 4, 5, 7, 8]. Именно поэтому привлекает внимание течение хронической ИБС на фоне дисфункции почек, а выявление ее признаков требует особого внимания со стороны практических врачей.
Целью данной работы является оценка взаимосвязей между уровнем клубочковой фильтрации и развитием острых сердечно-сосудистых осложнений и СН у больных с хронической ИБС.
Материалы и методы исследования. Был обследован 121 пациент (мужчины) в возрасте 36—78 лет (медиана 58 лет) с ИБС, стабильной стенокардией (n=49) и постинфарктным кардиосклерозом (n=72). У всех больных течение ИБС было осложнено развитием хронической СН I-III функционального класса (ФК) по Нью-Йоркской ассоциации сердца (NYHA).
Диагноз устанавливался на основании клинико-лабораторного обследования, данных электрокардиографии, велоэргометрии, коронарографии.Alpha
Всем больным проведено эхокардиографическое исследование с определением показателей структурно-функционального состояния сердца. Гипертрофию миокарда левого желудочка (ЛЖ) определяли, вычисляя индекс массы миокарда ЛЖ по рекомендациям ASE [6]. Для оценки функции почек использовали показатель клубочковой фильтрации (КФ), который рассчитывали по формуле MDRD: КФ=186ÍКРс–1,154Íвозраст–0,203, где КРс - креатинин сыворотки в мг/дл [9]. Kреатинин определяли тест-системой CREATINE liquicolor фирмы Human.
Статистическую обработку полученных результатов проводили с использованием статистических пакетов программ "Statistica for Windows 5.0" (Statsoft, USA). Параметрические показатели сравнивали с помощью U-критерия Манн-Уитни (медиана [нижний-верхний квартиль]). Связь между качественными характеристиками определяли по критерию Фишера, а корреляционные связи — по критерию Кендалла (τ). Влияние прогностических факторов на развитие острых сердечно-сосудистых осложнений оценивали путем построения кривых выживания (методом Kaплана-Mайера) с определением достоверности разницы между группами с помощью F-критерия Кокса.
Результаты исследования. Только у половины больных (n=62; 51,2 %) наблюдался нормальный уровень КФ (>90 мл/мин), тогда как у 38 (31,4 %) выявлено умеренное снижение КФ (60—90 мл/мин) и у 21 (17,4 %) — средняя степень снижения КФ (60—30 мл/мин). Всех пациентов разделили на 2 группы в зависимости от уровня КФ: 1 группу составили больные с уровнем КФ ≤60 мл/мин (n=21), 2 группу — с уровнем КФ >60 мл/мин (n=100).
Пациенты обеих групп получали медикаментозное лечение, которое существенно не отличалось по основным классам препаратов (дезагреганты, нитраты, ингибиторы ангиотензинпревращающего фермента, β-адреноблокаторы, антагонисты кальция, диуретики, статины).
Группы больных с разным уровнем КФ были сопоставимы по возрасту и клиническим характеристикам. Возраст пациентов 1 группы составлял 62 года [56—69], 2 группы — 58 лет [52—67], р>0,05. У больных 1 группы в отличие от лиц 2 группы чаще выявляли постинфарктный кардиосклероз (71 % против 58 %), хроническую СН III ФК по NYHA (43 % против 18 %), СД 2 типа (24 % против 11 %), АГ II-III стадии (90 % против 84 %), однако различия между группами не существенны. Достоверно чаще в 1 группе выявляли нарушения ритма и проводимости (57 % против 13 %, р=0,0001).
Корреляционный анализ выявил достоверную обратную связь КФ с уровнем систолического артериального давления (τ= –0,223, р=0,011), а также тенденцию к снижению КФ с возрастом (τ= –0,129, р=0,05). Кроме того, увеличение степени почечной дисфункции и снижение КФ четко ассоциируется с наростанием тяжести хронической СН (КФ и ФК СН: τ= –0,284, р=0,03), дилатацией ЛЖ (по конечно-диастолическому размеру ЛЖ (КДР ЛЖ): τ= –0,212, р=0,007), и его систолической дисфункцией (КФ и фракция выброса левого желудочка (ФВ ЛЖ): τ=0,182, р=0,02).
Сравнив все эхокардиографические (Эхо-КГ) показатели у пациентов двух групп, мы обнаружили, что уровень КФ ≤60 мл/мин ассоциируется с меньшей ФВ левого желудочка и большими размерами левого предсердия и ЛЖ (р <0,05) (табл. 1).
Таблица 1.
Параметры ЭхоКГ больных с ИБС и разным уровнем КФ
|
Показатели ЭхоКГ, единицы |
КФ ≤60 мл/мин |
КФ >60 мл/мин |
р |
|
ФВ ЛЖ, % |
50 [44—53] |
55 [48—60] |
0,033 |
|
КДР ЛЖ, см |
5,7 [5,2—6,2] |
5,4 [4,8—5,7] |
0,037 |
|
Левое предсердие, см |
4,4 [4,1—4,7] |
4,2 [3,9—4,4] |
0,042 |
|
Задняя стенка ЛЖ, см |
1,2 [1,1—1,2] |
1,2 [1,1—1,3] |
>0,05 |
|
Межжелудочковая перегородка, см |
1,2 [1,1—1,3] |
1,2 [1,1—1,3] |
>0,05 |
|
Правый желудочек, см |
2,5 [2,2—2,7] |
2,5 [2,2—2,6] |
>0,05 |
|
Индекс массы миокарда ЛЖ, г/м² |
140 [129—149] |
135 [113—165] |
>0,05 |
У 35 % больных с уровнем КФ ≤60 мл/мин диагностирована систолическая дисфункция ЛЖ и в 45 % случаев — дилатации левых камер сердца, тогда как у больных с уровнем КФ >60 мл/мин — в 17 % и 26 % случаев соответственно (р>0,05).
Для оценки течения хронической ИБС пациенты были под наблюдением в течение трех лет после первичного клинического обследования. Конечной точкой наблюдения была регистрация острых сердечно-сосудистых осложнений: острый коронарный синдром, инсульт, тромбоз периферических артерий. Осложненное течение ИБС наблюдалось у 20 (16,5 %) больных. Выявлено, что хроническая ИБС при уровне КФ >60 мл/мин реже осложнялась развитием острых сердечно-сосудистых событий (13 %), тогда как у больных с КФ ≤60 мл/мин они были диагностированы в 48 % случаях (р=0,001). Следует отметить, что кумулятивная доля выживших больных с КФ ≤60 мл/мин составляла 38,1 %, а у больных с КФ более 60 мл/мин — 81,1 % (F-критерий Кокса р <0,0001) (рис. 1).
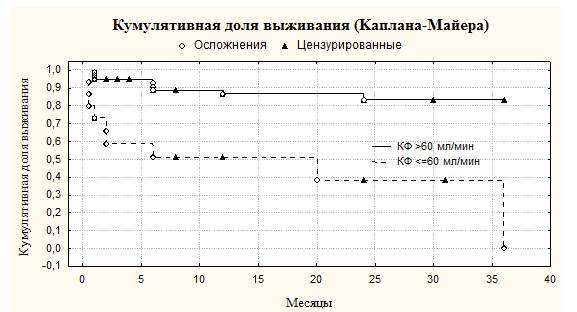
Рисунок 1. Виживаемость больных с хронической ИБС в зависимости от уровня КФ
Таким образом, КФ менее 60 мл/мин сопровождается ухудшением прогноза выживаемости больных хронической ИБС.
Одновременно худший прогноз для выживания больных с ИБС имел повышенный уровень креатинина крови. Так, у пациентов с уровнем креатинина >115 мкмоль/л кумулятивная доля выживших больных составляла 63,1 %, а с уровнем креатинина менее 115 мкмоль/л — 84,1 % (F-критерий Кокса р=0,01).
Определены и другие неблагоприятные прогностические факторы выживания пациентов, к которым относятся ІІІ ФК хронической СН, систолическая дисфункция ЛЖ (фракция выброса <45 %), увеличение размера левого предсердия (≥4,2 см), КДР левого желудочка (≥6 см), выраженная гипертрофия левого желудочка (индекс массы миокарда ЛЖ >170 г/м ²).
Выводы.
1.У больных с хронической ИБС нарушение функции почек с уменьшением КФ ≤60 мл/мин является предиктором развития острых сердечно-сосудистых осложнений в течение трех лет наблюдения.
2.Почечная дисфункция ассоциируется с более высоким ФК сердечной недостаточности и со структурно-функциональными изменениями левых камер сердца — их дилатацией и систолической дисфункцией.
3.Неблагоприятными прогностическими факторами выживания больных с хронической ИБС являются ІІІ ФК СН, систолическая дисфункция ЛЖ, дилатация левых камер сердца, выраженная гипертрофия ЛЖ.
Cписок литературы:
1.Гайдаєв Ю.О. Розробка і впровадження Державної програми профілактики та лікування серцево-судинної і судинно-мозкової патології // Український кардіологічний журнал. — 2007. — № 4. — С. 8—12.
2.Грудецька Ю.В., Сидорчук Л.П., Гресько Л.М. Особливості функціональних змін у нирках у хворих на ішемічну хворобу серця, серцеву недостатність та артеріальну гіпертензію // Буковинський медичний вісник. — 2007. — Т. 11, № 3. — С. 26—29.
3.Дзяк Г.В., Василенко А.М., Шейко С.О., Василенко В.А. Кардіоренальний анемічний синдром у хворих з хронічною серцевою недостатністю // Серцева недостатність. — 2010. — № 3. — С. 10—17.
4.Пархоменко О.М., Гур'єва О.М. Дисфункція нирок як маркер несприятливого перебігу інфаркту міокарда // Серце та судини. — 2008. — № 3. — С. 51—59.
5.Anavekar N.S., Solomon S.D., McMurray J.J. et al. Comparison of renal function and cardiovascular risk following acute myocardial infarction in patients with and without diabetes mellitus // Amer. J. Cardiology. — 2008. — Vol. 101 (7). — Р. 925—929.
6.Lang R.M., Bierig М., Devereux R.B. et al. Recommendations for Chamber Quantification: A Report from the American Society of Echocardiography's Guidelines and Standards Committee and the Chamber Quantification Writing Group, Developed in Conjunction with the European Association of Echocardiography // JASE. — 2005. — Vol. 18. — Р. 1440—1463.
7.Mielniczuk L.M., Pfeffer M.A., Lewis E.F. et al. Estimated glomerular filtration rate, inflammation, and cardiovascular events after an acute coronary syndrome // Amer. Heart J. — 2008. — Vol. 155 (4). — Р. 725—731.
8.Smith G.L., Masoudi F.A., Shlipak M.G. et al. Renal impairment predicts long-term mortality risk after acute myocardial infarction // J. Amer. Society of Nephrology. — 2008. — Vol. 19 (1). — Р. 141—150.
9.Snyder S., Pendergraph В. Detection and Evaluation of Chronic Kidney Disease // Amer. Fam. Physician. — 2005. — Vol. 72 (9). — Р. 1723—1734.
дипломов

