Статья опубликована в рамках: XV Международной научно-практической конференции «Современная медицина: актуальные вопросы» (Россия, г. Новосибирск, 11 февраля 2013 г.)
Наука: Медицина
Секция: Онкология
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
КОРРЕЛЯЦИЯ АКТИВНОСТИ ОКСИДА АЗОТА И ПЛАТИНОРЕЗИСТЕНТНОСТИ У БОЛЬНЫХ РАКОМ ЯИЧНИКОВ
Дубинина Владлена Геннадьевна
д-р мед. наук, профессор
Рыбин Андрей Игоревич
канд. мед. наук
E-mail: Andrey_Rybin@inbox.ru
Лукьянчук Олег Валерьевич
канд. мед. наук, доцент
Кузнецова Ольга Владимировна
канд. мед. наук, доцент
Одесский национальный медицинский университет
Проблема диагностики и лечения злокачественных новообразований яичников является одним из самых трудных разделов онкогинекологии. У большинства больных раком яичников (РЯ) заболевание выявляется на поздних стадиях, а результаты их лечения остаются неутешительными. Несмотря на высокую чувствительность многих современных методов диагностики, их специфичность недостаточна для дифференциации доброкачественного и злокачественного процессов в яичниках [1; 2; 4; 6; 7].
По данным Международного агентства по изучению рака ежегодно в мире регистрируется более 165 000 новых случаев РЯ, и более 100 тыс. женщин погибают от злокачественных новообра-зований яичников. По показателям смертности РЯ опережает рак тела и шейки матки, занимая 5-е место среди причин смерти от всех опухолей у женщин. Летальность больных РЯ на первом году после установления диагноза составляет 35 %. По сводным данным популяционных раковых регистров стран Европы, однолетняя выживаемость больных раком яичников составляет 63 %, трехлетняя — 41 %, пятилетняя — 35 %. За последнее десятилетие отмеченное в Европе увеличение пятилетней выживаемости больных злокачественными опухолями яичников на 3 % (с 32 % до 35 %), а в США — на 4 % (с 36 % до 39 %) объясняется не столько улучшением диагностики, сколько эффективным применением платиновой химиотерапии в лечении диссеминированных форм рака яичников и герминогенных опухолей. Такие неутешительные данные имеют определенное объяснение [1; 3; 7; 8—10; 14].
На сегодняшний день «золотым стандартом» лечения РЯ стадий IB-IIIC является оперативное вмешательство с последующим курсом послеоперационной химиотерапии. При этом, препаратом выбора в настоящее время (а по мнению большинства ученых, — и в ближайшие 30—40 лет) являются препараты платины.
Известно, что платина, обладающая мощным цитостатическим эффектом, действует системно и вызывает ряд так называемых побочных эффектов (side-effects). При этом цитостатический эффект платины реализуется посредством такого варианта гибели клеток, как некроз, приводя к системной интоксикации и, следовательно:
· отказу от дальнейшего лечения со стороны пациентки;
· отказу от дальнейшего лечения пациентки со стороны врача;
· невозможности продолжения терапии ввиду декомпенсации одной из систем организма пациентки.
Данные обстоятельства приводят к нарушению необходимых лечебных доз применяемого препарата, и, следовательно, являются одной из причин неэффективности проводимого лечения и высокой летальности больных с РЯ [11; 13].
Кроме того, по данным ряда исследователей, примерно в 20—30 % случаев у больных РЯ отмечается первичная резистентность к препаратам платины, а в 38—50 % случаев регистрируется вторичная резистентность [9; 10; 11; 13].
Таким образом, прогнозирование чувствительности опухоли яичника к препаратам платины является одной из актуальных проблем современной онкогинекологии.
Целью настоящей работы явился сравнительный анализ чувствительности аденокарциномы яичников стадии IC-IIIC к адъювантной химиотерапии препаратами платины в зависимости от состояния системы оксида азота в организме пациенток, являющегося одним из маркеров дизрегуляционной патологии и состояния саногенеза.
Материал и методы исследования. С 2007 года на базе отделения онкогинекологии Одесского областного онкологического диспансера был проведен сравнительный анализ 54 клинических случая рака яичников стадии IC-IIIC, которым была выполнена оптимальная либо субоптимальная циторедуктивная операция в объеме пангистерэктомии I типа, оментэктомии с последующей адъювантной химиотерапией препаратами платины. Во всех случаях гистологическим вариантом РЯ была аденокарцинома. Отбор больных для исследования осуществлялся по принципу «случай-контроль». До начала специального лечения всем пациенткам было проведено анкетирование с целью определения клинико-анамнестических характеристик заболевания, а также оценка состояния системы оксида азота. Критерием деления пациенток на группы была выбрана чувствительность РЯ к препаратам платины. Первую группу составили 32 пациентки с рецидивом РЯ в течение трех лет наблюдения. Вторую группу составили 22 пациентки с отсутствием рецидива заболевания в течение пяти лет наблюдения. Исследование проводилось по схеме «случай-контроль». Критерием резистентности к препаратам платины служила регистрация рецидива РЯ путем выполнения компьютерной томографии органов малого таза и определения уровней СА-125 в крови в течение 5 лет наблюдения.
Состояние системы оксида азота оценивали по величинам его основного метаболита — NO2- в плазме крови и моче. Определение проводили по методике, в основу которой положен способ определения конечного стабильного продукта неферментативного окисления NO, нитрит — аниона [NO2-], образующегося в результате взаимодействия NO с водой, что дает возможность судить о качестве образованного оксида азота. Для обнаружения [NO2-] использовали реактив Грисса (раствора сульфаниламида и N-нафтил этилендиамин дигидрохлорида в 30 % ледяной уксусной кислоте) в качестве цветообразующего реагента (дает малиновое окрашивание при наличии NO2 в жидкостях). Полученные результаты соотносили со стандартной калибровочной кривой, полученной на основе серийных разведений растворов нитрита натрия в диапазоне концентраций от 10 до 1000 мкмоль. Содержание NO2 — в биологических жидкостях рассчитывали по формуле:
NO2 (мкмоль/л) = Еиссл. х К(NaNO2) мкмоль/л: ЕстNaNO2
где: Еиссл. и Ест. — поглощение исследуемой пробы и стандартного образца соответственно;
К — концентрация NaNO2 , рассчитанная по калибровочной кривой.
В качестве объекта гистохимических исследований использовались столбики яичниковой ткани, полученные посредством биопсии яичниковой ткани. Полученный материал фиксировался 4 % раствором параформальдегида на протяжение 24 часов. Из фиксированного материала изготавливались криостатные срезы толщиной 11 мкм. На полученных срезах по прописи Д.Э. Коржевского (1996) определялась активность маркера NO-синтазы. Полученные препараты изучались с помощью светового микроскопа. Оценка результатов гистохимических реакций осуществлялась по количеству, размерам и цветности гранул фармазанов следующим образом:
· серое, серовато-желтое окрашивание мелких гранул фармазанов свидетельствует о следовой активности NO-синтазы в ткани яичников;
· серо-желтое окрашивание мелких и средних гранул фармазанов говорит о слабой активности NO-синтазы в ткани яичников;
· желтое, желто-коричневатое окрашивание мелких и средних гранул фармазанов означает, что тканевая активность NO-синтазы умеренная;
· желто-коричневое, коричневое окрашивание средних гранул фармазанов является показателем высокой активности NO-синтазы в ткани яичников.
По характеру локализации гранул выделяли следующие факторы:
· наличие изучаемых гранул по внутреннему контуру сосудов является показателем активности эндотелиальной NO-синтазы в ткани яичников;
· окрашивание цитоплазмы стромальных и эпителиальных клеток — свидетельствует о суммарной активности макрофагальной и эндотелиальной NO-синтазы.
Оценка активности NO-синтазы проводилась по всей площади изготовленного препарата. Полученные результаты подвергались статистической обработке.
Результаты исследования.
Средний возраст пациенток составил 55±8,1 лет и достоверно не отличался между группами.
Сравнительный анализ распределения РЯ по стадиям в обеих группах показал отсутствие достоверных различий между исследуемыми группами (табл. 1).
Таблица 1.
Распределение стадий РЯ у больных исследуемых групп, абс. (%)
|
Стадия РЯ |
I группа (n=32) |
II группа (n=22) |
Р |
|
IC |
3 (9,4 %) |
2 (9,1 %) |
> 0,05 |
|
IIA |
2 (6,3 %) |
2 (9,1 %) |
> 0,05 |
|
IIB |
5 (15,6 %) |
4 (18,2 %) |
> 0,05 |
|
IIC |
4 (12,5 %) |
3 (13,6 %) |
> 0,05 |
|
IIIA |
5 (15,6 %) |
4 (18,2 %) |
> 0,05 |
|
IIIB |
7 (21,8 %) |
4 (18,2 %) |
> 0,05 |
|
IIIC |
6 (18,8 %) |
3 (13,6 %) |
> 0,05 |
Анализ клинико-анамнестических характеристик пациенток обеих групп показал достоверное отсутствие различий по всем исследуемым показателям (табл. 2).
Таблица 2.
Клиническая характеристика групп больных
|
Рассматриваемый критерий |
I группа (основная) n=32 |
II группа (контрольная) n=22 |
p |
||
|
Абс. |
% |
Абс. |
% |
|
|
|
Профессиональные вредности |
21 |
65,6 |
14 |
63,6 |
>0,05 |
|
Нарушения индекса массы тела |
17 |
53,1 |
11 |
50,0 % |
>0,05 |
|
Нарушения менструальной функции |
18 |
56,3 |
15 |
68,2 |
>0,05 |
|
Отягощенный репродуктивный анамнез |
11 |
34,4 |
7 |
31,8 |
>0,05 |
|
Отягощенный генеалогический анамнез |
25 |
78,1 |
16 |
72,7 |
>0,05 |
|
Сопутствующая эндокринная патология |
10 |
31,3 |
7 |
31,8 |
>0,05 |
|
Сопутствующая патология молочных желез |
13 |
40,6 |
8 |
36,4 |
>0,05 |
|
Сопуствующая патология органов желудочно-кичшеного тракта |
11 |
34,4 |
7 |
31,8 |
>0,05 |
Таким образом, полученные данные позволяют говорить о том, что исследуемые группы были сформированы рандомизированно и могут быть сравнимы.
Сравнительный анализ состояния системы оксида азота в организме больных РЯ, резистентных и чувствительных к химиотерапии препаратами платины показал следующее (табл. 3).
Таблица 3.
Содержание нитритов в плазме крови и моче (M±m)
|
Исследуемая среда |
I группа (n=32) |
II группа (n=22) |
Достоверность P |
|
Плазма крови |
6,1±1,5 мкмоль/л |
10,3±1,2 мкмоль/л |
p<0,05 |
|
Моча |
3,9±0,6 мкмоль/л |
4,1±0,4 мкмоль/л |
p>0,05 |
При анализе активности оксида азота в крови пациенток первой группы было обнаружено, что средняя концентрация нитритов в плазме крови больных РЯ с резистентностью опухоли к химиотерапии препаратами платины составила 6,1±1,5 мкмоль/л, тогда как в группе больных без выявленного рецидива опухоли (чувствительных к препаратам платины) — 10,3±1,2 мкмоль/л, т. е. наблюдаемое различие статистически достоверно. Более того, сравнение активности оксида азота в моче пациенток обеих групп не выявило достоверного различия этих показателей. Содержание нитритов в моче женщин первой группы составило 3,9±0,6 мкмоль/л, тогда как концентрация данного метаболита оксида азота в моче больных РЯ, чувствительных к платиновой химиотерапии, была равна 4,1±0,4 мколь/л. Данное обстоятельство позволяет говорить о том, что различная активность оксида азота в плазме крови пациенток обеих групп не является результатом усиления экскреции метаболитов данного вещества мочевыделительной системой, либо отличий в содержании прекурсоров NO в рационах питания.
При гистохимической оценке активности NO-синтазы в сосудах опухолевой яичниковой ткани больных, чувствительных к препаратм платины, определялись мелкие сероватые, с легким желтоватым оттенком, гранулы диформазанов. Гранулы были рассеяны ближе к внутреннему контуру сосуда. Эпителий слизистой оболочки характеризовался наличием части клеток с серовато-желтой или серовато-коричневой окраской цитоплазмы. В остальных клетках контур тела обозначен мелкими сероватыми гранулами. В строме ткани яичников определялись поля серовато-коричневой диффузной окраски, на фоне которой имелись клетки с телами, контурированными мелкими сероватыми или черными гранулами. Также определялись отдельные железистые крипты, в которых тела части клеток имели желтоватый контур. В первой группе распределение активности NO-синтазы в ткани яичников было следующим (табл. 4).
Таблица 4.
Активность оксида азота в яичниковой ткани, абс. (%)
|
Активность NO-синтазы |
I группа (n=32) |
II группа (n=22) |
Достоверность P |
|
Высокая активность |
- |
3 (13,6 %) |
p<0,05 |
|
Умеренная активность |
- |
8 (36,4 %) |
p<0,05 |
|
Слабая активность |
3 (9,4 %) |
11 (50,0 %) |
p<0,05 |
|
Следовая активность |
11 (34,4 %) |
- |
p<0,05 |
|
Отсутствие активности |
18 (56,3 %) |
- |
p<0,05 |
Высокая тканевая активность оксида азота в первой группе не наблюдалась, а во второй группе составила 13,6 % (3 женщины). Умеренная активность NO-синтазы в ткани яичников была выявлена у 8 (36,4 %) пациенток с аденокарциномой яичников, чувствительной к химиотерапии препаратами платины, тогда как в группе больных с резистентными к платине опухолями умеренной активности оксида азота в ткани яичников выявлено не было. При этом слабая и следовая активность оксида азота были зарегистрированы у 3 (9,4 %) и 11 (34,4 %) больных первой группы соответственно, тогда как отсутствие активности NO-синтазы было выявлено в 56,3 % (18 пациенток) случаев. В то же время, умеренная и слабая активность NO-синтазы отмечалась у 8 (36,4 %) и 11 (50,0 %) пациенток второй группы соответственно. Следовая либо отсутствие активности оксида азота не отмечались ни в одном случае в группе больных РЯ без выявленного рецидива в течение 5 лет наблюдения.

Рисунок 1. Активность оксида азота в ткани яичника платиночувствительной пациентки с РЯ
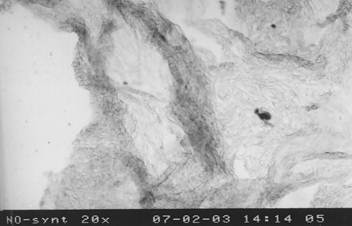
Рисунок 2. Активность оксида азота в ткани яичника платинорезистнтной пациентки с РЯ
Следует отметить, что у женщин, у которых при гистологическом исследовании выявлялась: сочность окраски ядер и выраженность цитоплазмы клеток стромы; визуальный эффект нагромождения ядер цитоплазмы; неправильность конфигурации расширенных крипт, что явилось основанием для диагностики у них пролиферативных процессов ткани яичников, проведение гистохимического исследования активности NO-синтазы показало следующее. В просвете сосудов и в лакунах определялись эритроциты желтовато-коричневой или коричневой окраски. Строма проявляла сероватую диффузную окраску, на фоне которой видны клетки с серовато окрашенной цитоплазмой, имеющей мягкий желтоватый оттенок. В деформированных клетках цитоплазма эпителиоцитов сероватой, но более густой, чем в строме, окраски, с легким розоватым оттенком. Обследование пациенток, у которых пролиферация яичниковой ткани дополнялась наличием полипозных разрастаний по внутренней оболочке капсулы, не выявило отличий активности NO-синтазы по отношению к вышеприведенному описанию. Единственной особенностью данных случаев было наличие в строме ткани яичников отдельных вытянутых клеток, цитоплазма которых имела диффузную, желтовато-коричневатую окраску цитоплазмы.
Выводы.
1.В исследуемых группах не было выявлено достоверной корреляции между стадией заболевания, клинико-анамнестическими характеристиками больных раком яичников и чувствительностью опухоли к препаратам платины.
2.Общая активность оксида азота у больных аденокарциномой яичников, резистентных в платиновой химиотерапии, достоверно ниже таковой в группе пациенток с аденокарциномой яичников, чувствительной к терапии препаратами платины.
3.Местная активность оксида азота у больных аденокарциномой яичников, резистентных в платиновой химиотерапии, достоверно ниже таковой в группе пациенток с аденокарциномой яичников, чувствительной к терапии препаратами платины.
4.Выявленное достоверное снижение активности системы оксида азота у больных с аденокарциномой яичников, резистентной к препаратам платины, является свидетельством достоверное более выраженной дизрегуляционной патологии и снижения саногенеза у таких больных. Состояние системы оксида азота в организме пациенток влияет на чувствительность либо резистентность опухоли к химиотерапии препаратами платины.
Список литературы:
1.Аксель М.А., Баринов В.В., Бокина Л.И.. Лекции по онкогинекологии. — М.: МЕДпресс-информ, 2009. — 425 с.
2.Бохман Я.В. Лекции по онкогинекологии. — М.: МИА, 2007. — 304 с.
3.Важенин А.В., Жаров А.В., Шимоткина И.Г. Актуальные вопросы клинической онкогинекологии М.: СТРОМ, 2010. — 128 с.
4.Винокуров В.Л. Рак яичников: закономерности метастазирования и выбор адекватного лечения больных. — СПб.: Фолиант, 2004. — 333 с.
6.Запорожан В.М., Цегельський М.Р. Гінекологічна патологія: Атлас: Навч. Посібник. — Одеса: ОДМУ, 2002. — 308 с.
7.Запорожан В.М., Цегельський М.Р., Рожковська Н.М. Акушерство і гінекологія. Підручник: У двох томах. — Одеса: Одес. Держ. Мед. ун-т, 2005. — 420 с.
8.Клиническая онкогинекология / под ред. В.П. Козаченко. — М.: Медицина, 2005. — 376 с.: ил.
9.Корман Д.Б. Основы противоопухолевой химиотерапии. — М.: Практическая медицина. — 2006. — 503 с.
10.Онкология: национальное руководство / Под ред. В.И. Чиссова, М.И. Давыдова. — М.: ГЭОТАР-Медиа, 2008. — 1072 с.
11.Переводчикова Н.И. Руководство по химиотерапии опухолевых заболеваний. — М.: Мед. — 2005. — 698 с.
12.Урманчеева А.Ф., Тюляндина С.А., Моисеенко В.М. Практическая онкогинекология: избранные лекции. — СПб.: «ТОММ», 2008. — 400 с.
13.Химиотерапия злокачественных новообразований / Под ред. Э. Чу и В.Т. де Вита (перевод с англ.) — М.: Практика. — 2008. — 447 с.
14.Щепотин И.Б., Бондарь Г.В., Ганул В.Л. Алгоритмы современной онкологии. — Киев: Книга плюс, 2006. — 304 с.
дипломов

