Статья опубликована в рамках: XV Международной научно-практической конференции «Современная медицина: актуальные вопросы» (Россия, г. Новосибирск, 11 февраля 2013 г.)
Наука: Медицина
Секция: Кардиология
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
ХРОНИЧЕСКАЯ ПОСЛЕИНФАРКТНАЯ АНЕВРИЗМА ЛЕВОГО ЖЕЛУДОЧКА: ОЦЕНКА ЖИЗНЕСПОСОБНОСТИ МИОКАРДА
Свитлык Галина Владимировна
канд. мед. наук, доцент ЛНМУ, г. Львов, Украина
E-mail: docsvit@gmail.com
Кияк Юлиан Григорьевич
д-р мед. наук, профессор, зав. кафедрой ЛНМУ, г. Львов, Украина,
E-mail: juliankiyak@yahoo.com
Беш Дмитрий Игоревич
канд. мед. наук, ассистент, ЛНМУ, г. Львов, Украина
E-mail: besh.dmytro@gmail.com
Чнгрян Гаянэ Вачиковна
ассистент, ЛНМУ, г. Львов, Украина
E-mail: chngryan@lycos.com
Гарбар Мирослава Орестовна
канд. мед. наук, ассистент, ЛНМУ, г. Львов, Украина
E-mail: mirasvit@yahoo.com
CHRONIC POSTINFARCTION ANEURISM OF LEFT VENTRICLE: ASSESSMENT OF VIABILITY OF THE MYOCARDIUM
Svitlyk Galina Vladimirovna
Kyyak Yulian Grigorevich
Besh Dmitriy Igorevich
Chngryan Gayane Vachikovna
Harbar Miroslava Orestovna
Ключевые слова: острый инфаркт миокарда с элевацией сегмента ST, хроническая послеинфарктная аневризма левого желудочка, перирубцовая зона, гибернация и оглушение кардиомиоцитов, реваскуляризация миокарда.
Key words: acute myocardial infarction with ST-segment elevation, chronic postinfarction left ventricular aneurysm, near scare zone, hibernation and stunning of cardiomyocytes, myocardial revascularization.
В течение последних десятилетий одной из основных причин смертности населения в разных странах мира является ишемическая болезнь сердца (ИБС). Так, в Украине 67,5 % смертей от сердечнососудистых заболеваний обусловлено именно этой патологией [3, c. 1].
Одним из основных методов лечения пациентов с ИБС является реваскуляризация миокарда — чрезкожные коронарные вмешательства и коронарное шунтирование (КШ). Стратегия лечения определяется результатами коронаровентрикулографии [3, c. 7].
Особенного внимания заслуживают больные с хронической послеинфарктной аневризмой. Их количество в Украине, в частности, в 22 раза превышает соответственное в Великобритании [3, c. 14]. Все эти пациенты для определения оптимальной лечебной тактики требуют проведения коронаровентрикулографии и консультации кардиохирурга. Как правило, данная категория больных поддается резекции аневризмы и КШ (в отдельных случаях — чрезкожному коронарному вмешательству), в результате чего удаеться достичь улучшения прогноза и качества жизни пациентов [3, c. 14; 5, c. 88; 7, c. 1833]. Решение кардиохирурга о необходимости коронарной реваскуляризации базируется на данных инструментальной оценки жизнеспособности миокарда [3, c. 14; 5, c. 88; 7, c. 1833].
Жизнеспособность акинетических и гипокинетических зон миокарда можно оценить с помощью стресс-эхокардиографии с добутамином; качество оценки при этом повышает применение в процессе добутаминового теста магнитно-резонансного исследования. Выявить с высокой точностью и оценить количественно ишемию и жизнеспособность миокарда дает возможность однофотонная эмисионная и позитронная эмисионная компьютерная томография [2, с. 83; 5, c. 70; 7, c. 1803—1804].
Цель исследования. Оценить жизнеспособность миокарда перирубцовых полей на основании изучения его ультраструктуры с целью определения целесообразности проведения реваскуляризации миокарда у пациентов с хронической послеинфарктной аневризмой.
Материал и методы исследования. Обследовано 115 пациентов (средний возраст 52,06±7,33 года) с ишемической болезнью сердца (ИБС), перенесших 5—6 лет назад острый инфаркт миокарда с элевацией сегмента ST. Контрольную группу составили 12 практически здоровых лиц (средний возраст 54,06±3,74 года).
Геометрию камер сердца оценивали с помощью эхокардиографического обследования. Фракцию выброса (ФВ) левого желудочка (ЛЖ) определяли согласно формуле Simpson biplane.
У 5 пациентов проведено ультраструктурное исследование биоптата, полученного из перирубцовой зоны левого желудочка во время операции с резекцией аневризмы левого желудочка (АЛЖ).
Результаты. При проведении эхокардиографии АЛЖ выявлено у 18 (15,65 %) больных. Средние значения конечнодиастолического размера ЛЖ у этих пациентов были достоверно выше (5,89±0,41 и 5,48±0,43 см, соответственно, р≤0,05), а ФВ ЛЖ (интегрального показателя систолической функции сердца) — достоверно ниже (37,31±4,37 % и 51,7±5,42 %, соответственно, р≤0,05), по сравнению с больными без осложненного течения ИБС.
Пяти больным по показаниям (мешковидная аневризма, склонная к образованию тромбов в полости аневризматического мешка и угрожающая возникновением тромбоэмболий и внезапной смертью пациента; не отвечающая на оптимальную медикаментозную терапию сердечная недостаточность ІІ-ІІІ ФК по NYHA) выполнено оперативное вмешательство с резекцией аневризмы и коронарным шунтированием.
Ультраструктурное исследование биоптатов из перирубцовой зоны выявило в области кровоснабжения критически суженной или окклюзированной коронарной артерии (согласно данных коронаровентрикулографии), наряду с практически неизмененными, гибернированные и оглушенные кардиомиоциты, а также клетки с признаками апоптоза и вторичного некроза (рис. 1, рис. 2).
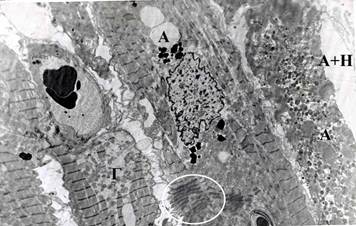
Рисунок 1. Электронная микрофотография пораженных кардиомиоцитов: гибернация (Г), оглушенность (О), апоптоз (А) и вторичный некроз (А+Н) апоптически измененного кардиомиоцита в результате отслоения сарколемы и отека саркоплазмы. Увеличение х 3 000
Гибернированные кардиомиоциты, в отличие от функционально сохраненных клеток, характеризуются потерей сократительного материала, уменьшением размеров и количества миофибрилл, заполнением гликогеном пространства, которое занимали миофиламенты, вакуолизацией каналов саркоплазматического ретикулума, в частности Т-системы саркоплазматической сетки. Одновременно в этих клетках отсутствуют признаки острой ишемии органелл, прежде всего такие, как вакуолизация, отек и набухание митохондрий, деформация сарколеммы, что свидетельствует об их тяжелой хронической ишемии. В отдельных участках наблюдается замещение капилляров гистиоцитами (рарификация микроциркуляторного русла), что, в свою очередь, инициирует появление фиброза и содействует развитию гибернации (рис. 2, рис. 3).
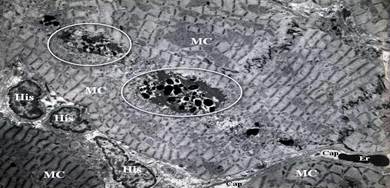
Рисунок 2. Электронная микрофотография гибернированного кардиомиоцита: компактные массы гликогена (O) в центральном участке клетки, вокруг липофусцина; между кардиомиоцитами имеются гистиоциты (His). Увеличение х 2 000
Классический признак гибернированных кардиомиоцитов — появление мелких, заокругленной формы митохондрий с проявлениями разрушения крист и накопление гликогена в местах разрушенных митохондрий и миофибрилл. Что наиболее часто возникает в центральной (возле ядра) и периферической зонах кардиомиоцитов (рис. 1).

Рисунок 3. Электронная микрофотография фрагмента гибернированного кардиомиоцита. Аккумуляция гликогена (О) вокруг дегенеративно измененных и гомогенизированных митохондрий (М) и вдоль саркомеров (СМ). Увеличение х 14 000
В ишемизированных зонах миокарда встречаются также участки с гипертрофированными кардиомиоцитами с признаками гибернации. Ультраструктурные критерии гипертрофии кардиомиоцитов — увеличение количества митохондрий в каждом саркомере, деструкция саркомеров с их замещением митохондриями или одиночно размещенными гранулами гликогена (рис. 4).

Рисунок 4. Электронная микрофотография части гипертрофированного кардиомиоцита, в саркоплазме которого одиночно размещены гранулы гликогена (О) между миофибриллами (МФ) и вокруг митохондрий (М), что характерно для гибернации. Увеличение х 20 000
Согласно данных электронных микрофотографий, в ишемизированном участке миокарда имеются оглушенные кардиомиоциты (рис. 5). Таким образом, оглушение кардиомиоцитов может возникать не только при остром коронарном синдроме [10, с. 103; 14, с. 1848; 15, с. 153], но и при стабильной коронарной болезни. Эти изменения имеют обратимый характер и относительно быстро исчезают после устранения ишемии. Характерными для оглушенных кардиомиоцитов являются участки пересокращения и перерастяжения миофибрилл, отсутствие митохондрий в этих участках и их миграция в зоны релаксации саркомеров (рис. 5). Контакты между Z-дисками миофибрилл и сарколеммой часто разрываются, что ведет к дисфункции кардиомиоцитов и снижению их способности к сокращению и релаксации. Такие функциональные изменения содействуют развитию гибернации кардиомиоцитов (рис. 1), а при длительном существовании последней — их апоптозу. В условиях тяжелой ишемии (рис. 5) наряду с оглушенностью кардиомиоцитов возникает отек митохондрий, фрагментация миофибрилл и лизис кардиомиоцитов. При разрыве сарколеммы развивается некроз кардиомиоцитов.

Рисунок 5. Электронная микрофотография оглушенного кардиомиоцита из перирубцовой зоны миокарда.
Кол — коллагеновые фибриллы; Ер — эритроцит; О — участки пересокращения; М — отечные митохондрии. Увеличение х 2 000
Таким образом, в перирубцовой зоне ишемизированных участков миокарда присутствуют кардиомиоциты в состоянии хронической гибернации и оглушения, что является следствием ишемии и своеобразным адаптивным состоянием, преследующим сохранение жизнеспособности миокарда [1, с. 4; 6, с. 43; 11, с. 1006; 12, с. 310; 13, с. 1006; 17, с. 588]. Улучшение коронарного кровотока способно приостановить дальнейшее развитие этого процесса и восстановить функцию ишемизированного миокарда [4, с. 32; 8, с. 985; 9, с. 186; 16, с. 212; 18, с. 388].
Выводы. Почти у каждого пятого больного, перенесшего острый инфаркт миокарда с элевацией сегмента ST, развивается хроническая аневризма левого желудочка, способствующая прогрессированию сердечной недостаточности.
Перирубцовая зона ишемизированных участков миокарда содержит кардиомиоциты в состоянии хронической гибернации и оглушения, что является адаптивной реакцией клеток в ответ на ишемию и преследует сохранение жизнеспособности миокарда.
Аневризмэктомия во всех случаях должна сопровождаться реваскуляризацией миокарда (коронарным шунтированием или стентированием коронарной артерии, за показаниями), способной улучить его функцию и качество жизни пациента.
Резюме. Обследовано 115 пациентов (средний возраст 52,06±7,33 года) с ишемической болезнью сердца, перенесших 5—6 лет назад острый инфаркт миокарда с элевацией сегмента ST. У 18 из них выявлено хроническую аневризму левого желудочка. Проведено ультраструктурное исследование биоптата, полученного из перирубцовой зоны левого желудочка во время аневризмэктомии (5 случаев). Выявлено кардиомиоциты в состоянии хронической гибернации и оглушения, что является адаптивной реакцией клеток в ответ на ишемию с целью сохранения жизнеспособности миокарда. Аневризмэктомия, исходя из результатов исследования, во всех случаях должна сопровождаться реваскуляризацией миокарда (коронарным шунтированием или стентированием коронарной артерии, за показаниями), способной улучить его функцию и качество жизни пациента.
Summary. We have examined 115 patients (mean age 52.06 ± 7.33 years) with coronary artery disease who underwent acute myocardial infarction with ST-segment elevation 5—6 years ago. In 18 of them was formed a chronic left ventricular aneurysm. Ultrastructural study of biopsy obtained from the near scar zone of left ventricle during aneurism excision was performed (in 5 cases). Cardiomyocytes were founded in a state of chronic hibernation and stunning, which is an adaptive response of cells to ischemia in order to preserve the viability of the myocardium. Due to this excision of aneurism should be accompanied by myocardial revascularization (coronary bypass surgery or coronary artery stenting) that can improve the function of the heart and quality of life.
Список литературы:
1.Апоптоз и гибернация кардиомиоцитов перирубцовой зоны как фактор прогрессирования хронической аневризмы сердца. Т.А. Браниште, Р.И. Соколова, В.С. Жданов и др. // Кардиология. — 2004. — № 5. — С. 4—7.
2.Долженко М.Н. Проведение стресс-эхокардиографии с добутамином у пациентов с ишемической болезнью сердца. Выявление ишемии миокарда // Український кардіологічний журнал. — 1998. — № 7—8. — С. 83—87.
3.Клиника, диагностика и показания к хирургическому лечению ишемической болезни сердца. Информационный бюллетень. А.Н. Руденко, В.И. Урсуленко, Е.К. Гогаева, А.В. Купчинский. — Киев, 2012. — 16 с.
4.Михаил Лутай. Систолическая дисфункция левого желудочка у больных с ИБС. Клиническое значение гибернированного миокарда // Doctor. — 2001. — № 4. — С. З0—34.
5.Рекомендації з діагностики та лікування хронічної серцевої недостатності (2012). Асоціація кардіологів України. Українська Асоціація фахівців з серцевої недостатності // Серцева недостатність. — 2012. — № 3. — С. 60—96.
6.Цыпленкова В.Г. Критические заметки по поводу парадигмы «гибернирующий и оглушенный миокард» // Кардиология. — 2005. — № 9. — С. 43—46.
7.ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2012 // European Heart Journal. — 2012. — V 33. — P. 1787—1847.
8.Gerd Heusch, Rainer Schulz, Shahbudin H. Rahimtoola. Myocardial hibernation: a delicate Balance // Am. J. Physiol. — 2005. March 1. — V. 3, № 288. — P. 984—999.
9.Gerd Heusch, Rainer Schulz. Features of short-term myocardial hibernation // Molecular and Cellular Biochemistry. — 1998. — V. 186. — P. 185—193.
10. Heusch G, Schultz R. Characterization on hibernating and stunned myocardium // Eur. heart J. — 1997. — V. 18 (Suppl. D). — P. 102—110.
11.Heusch G. Myocardial Hibernation // Circulation research. — 2004. —V. 8, № 94. — P. 1005—1007.
12.Heusch G., Schuitz R. A radical view on the contractile machinery in human heart failure // J. Am. Coll. Cardiol. — 2011. — Vol. 57(3). — P. 310—312.
13.Heusch G., Sipido K. Myocardial Hibernation. A Double-Edged Sword // Circulation research. — 2004. — V. 8, № 94. — P. 1005—1007.
14.Kloner R.A., Bolli R., Marban E. et al. Medical and cellular implications of stunning, hibernation, and precondicioning: an NHLBI workshop // Circulation. — 1998. — Vol. 97. — P. 1848—1867.
15.Laky D., Parascan L., Candea V. Myocardial stunning. Morphological studies in acute experimental ischemia and intraoperatory myocardial biopsies // Rom J. Morphol. Embryol. — 2008. — V. 49, № 2. — P. 153—158.
16.Rahimtoola S.H. The hibernating myocardium // American heart journal. — 1989. — Vol. 117. — P. 211—221.
17.Schulz R., Heusch G. Myocardium Hibernating // Heart. — 2000. — V. 84. — P. 587—594.
18.Vanoverschelde J.J., Melin J.A. The Pathophisiology of Myocardial Hibernation: Current Controversies and Future Directions // Progr. Cardiovasc. Dis. — 2001. — V. 43, № 5. — P. 387—398.
дипломов

