Статья опубликована в рамках: XIV Международной научно-практической конференции «Современная медицина: актуальные вопросы» (Россия, г. Новосибирск, 14 января 2013 г.)
Наука: Медицина
Секция: Фармацевтическая химия, фармакогнозия
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
ИЗУЧЕНИЕ КУМАРИНОВ ТРЁХРЁБЕРНИКА НЕПАХУЧЕГО И НИВЯНИКА ОБЫКНОВЕННОГО
Горячкина Елена Геннадьевна
канд. фармацевт.наук, доцент ИГМУ,
г. Иркутск
Е-mail: rosforest@mail.ru
Мазунова Ольга Игоревна
аспирант, ИГМУ,
г. Иркутск
Федосеева Галина Михайловна
д-р фармацевт.наук, профессор ИГМУ,
г. Иркутск
Основными действующими веществами надземной части трёхрёберника непахучего (ТН) и нивяника обыкновенного (НО) являются полифенольные соединения — флавоноиды, фенолкарбоновые кислоты, дубильные вещества и кумарины [2, c. 23].
Для установление содержания кумаринов в траве изучаемых растений разработан метод дифференциальной фотоэлектроколориметрии, основанный на реакции кумаринов с диазотированной сульфаниловой кислотой в щелочной среде [1, с. 8].
Расчёт содержания суммы кумаринов проводили в пересчёте на эскулетин.
Методика: 0,50 г (точная навеска) измельчённого сырья помещали в колбу на 100 мл, добавляли 50 мл спирта этилового 70 % и нагревали на водяной бане с обратным холодильником в течение 30 минут, затем извлечение фильтровали в колбу на 200 мл, фильтр промывали 2 раза горячим спиртом этиловым 70 % по 10 мл. В колбу с объединёнными фильтратами добавляли 2 мл свинца ацетата основного 10 % и кипятили 3 минуты для полного осаждения сопутствующих фенольных соединений. Горячее извлечение фильтровали через бумажный фильтр диаметром 7 см, вложенный в воронку. Колбу и фильтр промывали 3 раза горячим спиртом этиловым 70 % по 20 мл.
К фильтрату добавляли 1 г натрия фосфата однозамещённого и кипятили 3 минуты. Горячий раствор фильтровали через бумажный фильтр в колбу со шлифом на 300 мл, фильтр промывали спиртом этиловым 70 % 3 раза по 20 мл, спирт отгоняли на водяной бане, водный остаток переносили в делительную воронку и четырёхкратно обрабатывали 25 мл хлороформа. Хлороформный слой каждый раз отделяли и фильтровали через 5 г натрия сульфата безводного, помещенного на фильтр, в сухую колбу. К сухому остатку после отгонки хлороформа прибавляли 7 мл спирта этилового 96 %, полученный раствор переносили в мерную колбу на 50 мл, колбу ополаскивали 5 мл спирта этилового 96 % и переносили в ту же мерную колбу. Затем добавляли 10 мл натрия гидроксида 0,1 М, нагревали на водяной бане 5 минут и доводили до метки натрия гидроксидом 0,1 М (раствор А).
Готовили разведения: в две пробирки помещали по 0,5 мл раствора А, затем в первую добавляли 6,5 мл натрия гидроксида 0,1 М (раствор сравнения), во вторую 1 мл свежеприготовленного диазореактива и 5,5 мл натрия гидроксида 0,1 М.
Измерение оптической плотности проводили через 20 минут на КФК — 2 МП при длине волны 490 нм.
Расчётная формула:
Х ( %) = ![]() =
= ![]() ,
,
где: V1 — объём общий, равный 50 мл;
V2 — объём разбавления, равный 7 мл;
V3 — объём, взятый для разбавления, равный 1 мл;
с — содержание эскулетина в 1 мл колориметрируемого раствора, найденное по калибровочному графику, г;
W — потеря в массе при высушивании сырья, %;
M — масса сырья, в граммах.
Для построения калибровочного графика использовали РСО эскулетина (производство «Chemapol» PragueCzechoslovakia), предварительно очищенный методом двойной перекристаллизации.
0,5000 г (точную навеску) эскулетина растворяли в 50 мл спирта этилового 96 % и готовили разведения (табл. 1):
Таблица 1.
Данные для построения калибровочного графика по эскулетину
|
№ |
1 % раствора эскулетина,мл |
Диазо-реактив,мл |
0,1 М р-ра NaOH,мл |
Спирт этиловый 96 %,мл |
Концентрация эскулетина,г/ мл |
Оптическая плотность |
|
1 |
0,1 |
2 |
5 |
2,9 |
1∙10-5 |
0,155 |
|
2 |
0.2 |
2 |
5 |
2,8 |
2∙10 |
0,211 |
|
3 |
0,3 |
2 |
5 |
2,7 |
3∙10 |
0,315 |
|
4 |
0,4 |
2 |
5 |
2,6 |
4∙10 |
0,384 |
|
5 |
0,5 |
2 |
5 |
2,5 |
5∙10 |
0,522 |
|
6 |
0,6 |
2 |
5 |
2,4 |
6∙10 |
0,787 |
|
7 |
0,7 |
2 |
5 |
2,3 |
7∙10 |
0,871 |
|
8 |
0,8 |
2 |
5 |
2,2 |
8∙10 |
0,868 |
|
9 |
0,9 |
2 |
5 |
2,1 |
9∙10 |
0,956 |
|
10 |
1,0 |
2 |
5 |
2,0 |
10∙10 |
1,093 |
В полученных растворах через 20 минут определяли оптическую плотность на приборе КФК — 2МП при длине волны 490 нм и строили калибровочный график, представленный на рисунке.
Коэффициент корреляции для калибровочного графика r = 0,985.
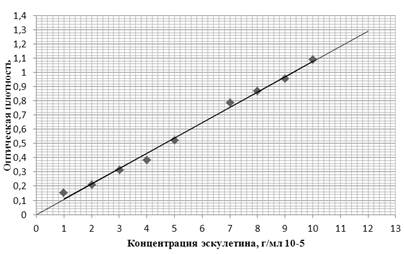
Рисунок 1. Калибровочный график для количественного определения кумаринов в пересчёте на эскулетин
В таблице 2 представлены результаты исследования 6 испытуемых образцов травы ТН и НО, собранные в период цветения (июнь—июль 2011 и 2012 года) в Иркутской области: районы Большого и Малого Голоустного, Оёка, Пивоварихи, Горячих ключей.
Статистическая обработка результатов анализа представлена в таблице 3.
Отсутствие систематической ошибки метода доказано в опытах с добавками (табл. 4).
Таблица 2.
Количественное содержание кумаринов в траве трёхрёберника непахучего и нивяника обыкновенного, %
|
Исследуемое растение |
Пробы |
|||||
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
Трёхрёберник непахучий |
0,31 |
0,30 |
0,25 |
0,32 |
0,35 |
0,39 |
|
Нивяник обыкновенный |
1,12 |
1,18 |
1,05 |
0,88 |
0,91 |
1,10 |
Таблица 3.
Метрологическая характеристика фотоколориметрического определения суммы кумаринов в траве ТН и НО
|
Исследуемое растение |
f (n=6) |
|
S2 |
S |
P % |
t (P,f) |
Δ |
|
|
|
ТН |
5 |
0,32 |
0,0022 |
0,0473 |
90 |
2,01 |
0,03 |
|
|
|
НО |
5 |
1,04 |
0,0144 |
0,1202 |
90 |
2,01 |
0,10 |
|
|
Таблица 4.
Результаты количественного определения суммы кумаринов в траве трёхрёберника непахучего с использованием метода добавок эскулетина
|
Содержание суммы кумаринов в 1 г сырья, мг |
Добавлено эскулетина, мг |
Сумма кумаринов, мг |
Относительная ошибка, % |
|
|
вычислено |
найдено |
|||
|
3,2 |
0,22 |
3,44 |
3,34 |
-2,91 |
|
3,2 |
0,29 |
3,49 |
3,57 |
2,29 |
|
3,2 |
0,33 |
3,53 |
3,60 |
1,98 |
Таким образом, обнаружено, что наиболее богата кумаринами трава нивяника обыкновенного.
Список литературы:
1.Прокопенко О.П. Колориметричный метод кiлькiсного визначения кумаринев / О.П. Прокопенко // Фармацевтичний журнал, 1992. — Т. 17, № 6. — с. 18—22.
2.Федосеева Г.М. Фармакогностическое изучение представителей семейства астровых, произрастающих в Восточной Сибири// Федосеева Г.М., Горячкина Е.Г., Бочарова Г.И. и др. Разработка, исследование и маркетинг новой фармацевтической продукции : сборник научных трудов. Пятигорск, 2008 — вып. 63. — с. 23—24.
дипломов