Статья опубликована в рамках: XXXV Международной научно-практической конференции «Инновации в науке» (Россия, г. Новосибирск, 27 июля 2014 г.)
Наука: Химия
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
Статья опубликована в рамках:
Выходные данные сборника:
ПОТЕНЦИОМЕТРИЧЕСКИЕ КРИТЕРИИ ПЕРЕМЕЩЕНИЯ ИОНОВ ZN 2+ В РАСТВОРАХ СОЛЕЙ ZNSO4 И ZN(NO3)2
Ларин Сергей Леонидович
аспирант кафедры общей и биоорганической химии Курского государственного медицинского университета, РФ, г. Курск
Ямпольский Леонид Михайлович
канд. хим. наук, доцент, заведующий лабораторией физико-химических исследований НОУ ВПО РОСИ, РФ, г. Курск
Будко Елена Вячеславовна
д-р ф. наук, профессор, зав. кафедрой общей и биоорганической химии, Курского государственного медицинского университета, РФ, г. Курск
POTENTIOMETRIC CRITERIA OF DISPLACEMENT ZN2+ IN THE SOLUTIONS OF ZNSO4 AND ZN(NO3)2
Larin Sergei
graduate student of the Department of General and Bioorganic Chemistry, Kursk State Medical University, Russia, Kursk.
Yampolsky Leonid
head of the Laboratory of Physicochemical Research ROSI, PhD docent, Russia, Kursk
Budko Elena
head Department of General and Bioorganic Chemistry, PhD professor of Kursk State Medical University, Russia, Kursk
АННОТАЦИЯ
В работе изложены результаты потенциометрического исследования свойств растворов ZnSO4 и Zn(NO3)2. Дано сравнительное описание роли противоионов SO42- и NO3- как потенциалопределяющего фактора. Показано их участие в обеспечении подвижности ионов Zn2+. Предложены принципы моделирования растворов электролитов с заданными свойствами ЭДС и подвижностью ионов, что позволяет использовать их в качестве экспериментальных сред для изучения биодоступности ионов цинка.
ABSTRACT
This work presents some results of studies different properties of solutions ZnSO4 and Zn(NO3)2 by potentiometry. It allow to give a comparative description of the role of SO42- and NO3- like a factor that affects the potential of solutions; show their part in ensuring the mobility of ions Zn2+; suggest modeling principles of electrolyte solutions with desired properties of EMF and ion mobility, that allow to use this data to study bioavailability of zinc ions.
Ключевые слова: ионы цинка; противоионы; потенциометрическое определение ЭДС; подвижность ионов; моделирование свойств растворов электролитов; биодоступность.
Keywords: zinc ions; counterions; potentiometric determination of EMF; ion mobility; modeling properties of electrolyte solutions; bioavailability.
Динамика ионов в растворе является их важнейшей функцией, определяющей основные количественные характеристики растворов электролитов. Очевидна ее зависимость от размера, заряда, степени сольватированности ионов. Важнейшей энергетической характеристикой, отражающей способность заряженных частиц формировать в растворе электрическое поле определенной напряженности, способное переносить единичный точечный заряд является ЭДС. Ее величина позволяет судить об энергетическом усилии раствора по переносу заряженной частицы в том числе, через различные биологические мембраны, капсулы и т. д. [2].
Важной характеристикой поведения ионов в растворе является их способность к перемещению в объеме под воздействием ЭДС. Очевидно, что эта особенность позволяет характеризовать активность частиц по преодолению мембранных структур.
Все это в полной мере относится к свойствам Zn2+ в составе растворов сульфата и нитрата цинка. Выбор соединений в качестве объектов исследования определяется биологической значимостью ионов цинка, сульфата и нитрата, необходимостью исследования физико-химических проблем их биодоступности, интересом к моделированию процессов проникновения в клеточные структуры ионов цинка, входящих в электролитный состав жидкостей организма или вводимых искусственно [3].
Выбор потенциометрии в качестве основного метода исследования определяется избранными характеристическими параметрами состояния растворов и селективностью оборудования [1].
Целью данной работы является изучение сравнительных характеристик поведения Zn2+ и его противоионов в растворах сульфата и нитрата цинка. Для этого необходимо: провести оценку факторов, определяющих их способность к перемещению; предложить системы приемов, позволяющих делать выводы о преимуществах и недостатках каждой из указанных систем относительно возможности перемещения в них ионов цинка; сформировать предложения по критериям проектирования модельных систем для изучения биодоступности Zn2+ в жидкостях организма.
Материалы и методы
Эксперимент выполнялся с использованием pH-метра/иономера S500 SevenExcellence (Mettler Tolledo, Германия). Для измерений применялась двухэлектродная ячейка состоящая из индикаторного цинкселективного электрода ХС-Zn-001 (ООО «Сенсорные системы», Санкт-Петербург, РФ, внесен в гос. реестр под № 20946 от 28.06.2005) и хлоридсеребряного электрода сравнения ЭСО-01 (ОАО «Гомельский завод измерительных приборов», РФ, ГОСТ 17792-72). Для приготовления растворов использовались: цинк азотнокислый шестиводный (ХЧ, ООО «Реахим», Санкт-Петербург, РФ, ГОСТ 5106-77), цинк сернокислый семиводный (ХЧ, ООО «Реахим», Санкт-Петербург, РФ, ГОСТ 4174-77), вода дистиллированная (ОАО «ХимПрибор», Калуга, РФ, ГОСТ 6709-72). Исследуемые растворы готовились последовательным десятикратным разбавлением исходного 1М раствора, который был приготовлен весовым методом. Измерения проводились при стандартных условиях (298 К, 101,3 кПа). Стабильности измерений добивались путем проведения электрокинетического исследования до 5—6 стабильной точки. Перед началом работы проводилась калибровка иономера стандартными растворами хлорида цинка (ЧДА, ООО «Реахим», Санкт-Петербург, РФ, ГОСТ 4529-78) в диапазоне 10-6 —5´10-2 моль/дм3, приготовленными весовым методом. Контроль состояния электрода проводился по сопоставлению крутизны электродной функции с данными паспорта. Полученная электродная функция для нитрата цинка имеет вид: у=30,056x+242,615, для раствора сульфата цинка: у=31,222x+270,319. Таким образом, тангенс угла наклона равен значению, указанному в паспорте электрода — 27±5 мВ.
Результаты и обсуждение
В результате экспериментального исследования получены зависимости ЭДС (Е) от концентрации (с) для растворов для растворов Zn(NO3)2 и ZnSO4 в диапазоне концентраций от 10-6 до 1 моль/дм3 (рис. 1).
При сопоставлении ЭДС эквимолярных концентраций растворов ZnSO4 и Zn(NO3)2 (рис. 1) выявлена стабильность значений (∆Е) на основном исследуемом концентрационном интервале. Сравнение одинаковых значений Е на кривых зависимости Е(с) для указанных растворов показывает, что одна и та же ЭДС достигается большим количеством нитрата цинка. Очевидно, что для данных систем мощность ЭДС растворов определяют противоионы, и сульфат-ион оказывает в этом случае значительно большее воздействие.
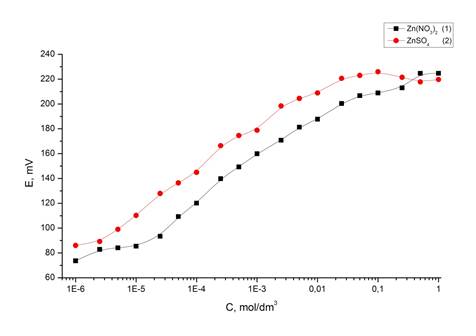
Рисунок 1. Зависимость величины потенциала (E) от концентрации (c ) раствора сульфата и нитрата цинка
В тоже время, стабильно высокая величина ЭДС в растворах сульфата цинка показывает его большую, относительно эквимолярного раствора нитрата цинка, мощность по переносу заряда. Сравнительный анализ зависимости Е(с) для эквимолярных растворов сульфата и нитрата цинка показал различия величин ЭДС. Поскольку данные системы отличаются только природой противоионов, очевидно, что именно в этом основная причина различий уровня Е.
Постоянство изменения ЭДС в диапазоне концентраций от 10-5 до 0,1 моль/дм3 позволяет судить о системных различиях в способности потенциалообразования противоионов SO42- и NO3-, которые определяются их структурными и функциональными особенностями. Таким образом, при формировании системы, обеспечивающей то или иное значение ЭДС, необходимо учитывать не только катионный, но и ее анионный состав.
Построение дифференциальных кривых в координатах ∆E/∆C (c) позволяет проанализировать скорость изменения ЭДС растворов при различных значениях концентраций (рис. 2).
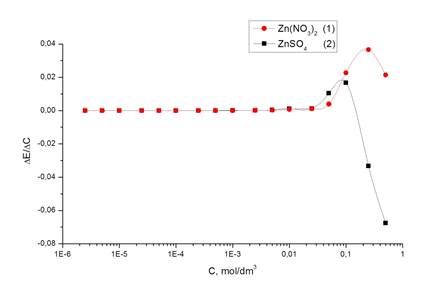
Рисунок 2. Дифференциальная кривая зависимости изменения ЭДС от концентраций растворов нитрата (1) и сульфата (2) цинка
Постоянство скорости изменения потенциала для растворов (1) и (2) (рис. 2) наблюдается в диапазоне концентраций 10-6—0,15 моль/дм3. На графике можно выделить три зоны. На линейном участке прирост потенциала постоянен, что говорит об отсутствии потенциометрических различий в растворах в этих граничных условиях. При достижении определенных концентраций происходит скачок потенциала, вызванный существенной структурной перестройкой. Значительно больший динамизм изменений наблюдается для раствора нитрата цинка (рис. 2). Учитывая то, что сам противоион измениться в данных экспериментальных условиях не мог, скачок потенциала связан со способностью ионов нитрата быстрее перемещаться в приэлектродную зону. Подтверждает это и участок такого же резкого падения ЭДС, отражающий возникший градиентный концентрационный фактор ионов нитрата, который принуждает их к более равномерному размещению в объеме. В растворах сульфата цинка этот процесс менее выражен, что определяется меньшей подвижностью ионов Zn2+ в данном растворе, следовательно, скорость формирования двойного электрического слоя (ДЭС) в приэлектродном пространстве у ионов сульфата ниже. Размещение точек максимума показывает условия достижения максимальной скорости роста разности потенциалов — условий наиболее выгодных, с позиции ЭДС, для перемещения ионов цинка.
Для оценки подвижности ионов в растворах сульфата и нитрата цинка исследована зависимость ЭДС от времени. На рис. 3 приведены графические зависимости Е(t) для различных концентраций раствора сульфата цинка.

Рисунок 3. Зависимость величины потенциала (E ) от времени (t) в растворах ZnSO4 различных концентраций
Рост потенциала с течением времени сменяется стабилизацией его значений для всех концентраций, но наиболее резкий рост ЭДС отмечается при с = 0,5 и 10-3 моль/дм3 (рис. 3). Очевидно, что для данных значений концентраций это связано со структурной перестройкой системы.
Изменение ЭДС в растворе нитрата цинка от времени для разных концентраций (рис. 4.) характеризуется падением потенциала со временем до его стабилизации. Нитрат ионы с течением времени уходят из приэлектродного пространства, в то время как сульфат ионы к нему только перемещаются. Очевидно, что определяющим фактором этих процессов является структура самих частиц, растворителя, градиент концентрации. Таким образом, подвижность нитрат ионов гораздо больше и градиент концентрации для них играет роль значительно большую, чем для сульфат-ионов.
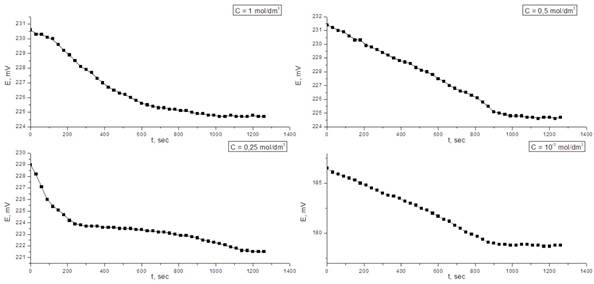
Рисунок 4. Зависимость величины потенциала (E ) от времени (t) в растворах Zn(NO3)2 разных концентраций
Результаты данной части исследования физико-химического процесса биодоступности ионов цинка позволяют считать, что основными факторами, определяющими способность ионов к перемещению, в частности, через различные мембранные структуры, являются ЭДС раствора электролита и подвижность ионов. Причем, эти функции противоположно направлены: так большая подвижность ионов снижает величину разности потенциалов по причине дестабилизации структуры двойного электрического слоя. Раствор с меньшим значением подвижности ионов обладает более структурированным ДЭС и, соответственно, большей разностью потенциалов, т. е. способностью к перемещению точечного заряда. Использование растворов электролитов в концентрациях области скачка потенциала обеспечит большую эффективность перемещения частиц за счет резкого роста ЭДС. При этом раствор электролита должен обладать подвижностью ионов достаточной для перемещения необходимого количества вещества.
Из всего сказанного следует, что среда, применяемая для транспортировки ионов, в частности, в мембранные системы должна сочетать достаточную мощность ЭДС, предельный скачок потенциала и подвижность ионов, что можно заранее моделировать по сопоставлению приведенных выше результатов исследования. Методика конструирования сред, обладающих необходимыми свойствами транспортировки ионов, и необходимый для расчетов математический аппарат будут приведены в следующей работе нашей авторской группы
Список литературы:
1.Егоров В.В. Ионоселективные жидкостные электроды: проблемы описания и экспериментального определения селективности // Рос. хим. ж. — 2008 — № 2. — С. 37—51.
2.Калугин О.Н. Динамика сольватированного иона в бесконечно разбавленном растворе: от феноменологии до микроскопического описания // Вестник Харьковского национального университета. — 2002. — № 573. — С. 13—45.
3.Сырников Ю.П., Пенкина Н.В., Родникова М.Н. Вопросы микродинамики в жидкостях и растворах // Журнал физической химии. — 2006. — № 10. — с. 1743—1746.
дипломов

