Статья опубликована в рамках: XXXI Международной научно-практической конференции «Инновации в науке» (Россия, г. Новосибирск, 31 марта 2014 г.)
Наука: Химия
Скачать книгу(-и): Сборник статей конференции, Сборник статей конференции часть II
- Условия публикаций
- Все статьи конференции
дипломов
Статья опубликована в рамках:
Выходные данные сборника:
ОБ ЭЛЕКТРОПРОВОДНОСТИ АЦЕТАТОВ ЩЕЛОЧНЫХ МЕТАЛЛОВ И ЦИНКА
Надиров Ермурат Галымбекович
канд. хим. наук, доцент Алматинского университета энергетики и связи, Республика Казахстан г. Алматы
Иманбекова Тохтабуби Джумадиловна
канд. техн. наук, доцент Алматинского университета энергетики и связи, Республика Казахстан г. Алматы
Е-mail:
Мустафаева Назира Маматкуловна
старший преподаватель Алматинского университета энергетики и связи, Республика Казахстан г. Алматы
ON CONDUCTIVITY OF ACETATES OF ALKALI METALS AND ZINC
Ermurat Nadirov
candidate of chemical sciences associate professor of Almaty University of Power Engineering and Telecommunications, Republic of Kazakhstan Almaty
Tokhtabuby Imanbekova
candidate of engineering sciences associate professor of Almaty University of Power Engineering and Telecommunications, Republic of Kazakhstan Almaty
Nazira Mustafayeva
senior Lecturer of Almaty University of Power Engineering an Telecommunications, Republic of Kazakhstan Almaty
АННОТАЦИЯ
В работе исследованы удельные электропроводности чистых ацетатов щелочных металлов и цинка в зависимости от температуры. Экспериментальные данные показали, что электропроводность солей ацетатов щелочных металлов уменьшается при неизменном анионе с уменьшением радиуса катиона и с увеличением энергии решетки. Такая зависимость указывает на связь между кристалической решеткой и электропроводностью ацетатов щелочных металлов.
ABSTRACT
In this paper studies were made on specific conductivity of pure acetates of alkali metals and zinc in different temperatures. Experimental data revealed that given consistent anion conductivity of salts of alkali metals acetates decreases with the decrease of cation’s radius and with increase of the lattice energy. Such dependence shows relationship between the crystal lattice and the conductivity of acetates of alkali metals.
Ключевые слова: электропроводность; кристаллическая решетка; энергия активации; степень ионности; энергия дрейфа; анион; катион; электроотрицательность вещества.
Keywords: electric conductivity; crystal lattice; activation energy; degree of iconicity; energy drift; anion; cation, electronegativity of a substance.
Известно, что электропроводность от температуры у твердых солей подчиняется экспоненциальной зависимости
![]() ,
,
где: ![]() постоянный коэффициент проводимости;
постоянный коэффициент проводимости;
![]() энергия активации удельной электропроводности;
энергия активации удельной электропроводности;
![]() постоянная Больцмана;
постоянная Больцмана;
![]() абсолютная температура.
абсолютная температура.
Изменение электропроводности с температурой у ряда солей в расплавленном состоянии не всегда подчиняется экспоненциальной зависимости.
Повышение температуры увеличивает «свободный» объем расплава, разрушаются комплексные частицы, т. е. идет перестройка кристаллической решетки в целом.
При плавлении ионной соли происходит резкое увеличение электропроводность. Процесс является следствием нарушения дальнего порядка расположения ионов и увеличения их подвижности, при этом энергия активации катионов и анионов сильно отличаются друг от друга и перенос тока производится в основном наиболее подвижными из них. Если энергия активации катионов и анионов достаточно близки, то удельная электропроводность будет выражаться суммой двух или нескольких экспоненциальных выражений.
Изменения энергий активаций как основного переносчика тока, так и ионов, не принимавших ранее участие в переносе могут привести к возникновению искривлений на прямой или изломам на линии логарифма электропроводности от ![]() .
.
По данным изотерм проводимости можно рассчитать энергию активации и связать их с изменением энергии кристаллической решетки.
В исследованиях, проведенных рядом авторов [1, 3, 4], показано существование прямой связи между проводимостью и постоянной решетки, уменьшение энергии активации электропроводности с увеличением радиуса аниона щелочно-галоидных соединений.
Целью настоящей работы явилась попытка установить связь между кристаллической решеткой и электропроводностью ацетатов щелочных металлов.
Экспериментально найденные и рассчитанные нами величины энергии активации собственной проводимости ![]() и энергии активации проводимости расплавов
и энергии активации проводимости расплавов ![]() , энергии решетки
, энергии решетки ![]() , радиусы ионов
, радиусы ионов ![]() , удельные заряды
, удельные заряды ![]() , приведенные моменты µ ионов и степени ионности
, приведенные моменты µ ионов и степени ионности ![]() ацетатов щелочных металлов, цинка и кадмия приведены в таблице 1.
ацетатов щелочных металлов, цинка и кадмия приведены в таблице 1.
Таблица 1.
Значения энергий кристаллических решеток, энергий активации и степени ионности ацетатов
|
Ионы |
Для ацетатов соответствующих ионов |
|
эл.ст. единиц |
µ |
|||
|
|
|
|
|
||||
|
|
219,6 |
0,657 |
1,330 |
67,6 |
0,68 |
0,691 |
1,47 |
|
|
199,2 |
0,201 |
0,649 |
70,5 |
0,98 |
0,210 |
1,03 |
|
|
178,4 |
0,161 |
0,458 |
72,7 |
1,33 |
0,122 |
0,75 |
|
|
170,6 |
0,561 |
0,765 |
72,7 |
1,49 |
0,056 |
0,68 |
|
|
162,6 |
0,773 |
1,378 |
75,5 |
1,65 |
0,036 |
0,60 |
|
|
625,9 |
0,460 |
1,105 |
47,4 |
0,83 |
0,146 |
2,41 |
|
|
597,7 |
0,366 |
- |
44,1 |
0,97 |
0,083 |
2,06 |
Энергия кристаллической решетки ![]() рассчитывается по видоизмененному уравнению А.Ф. Капустинского [2]:
рассчитывается по видоизмененному уравнению А.Ф. Капустинского [2]:
![]() ккал/моль,
ккал/моль,
где: ![]() число ионов;
число ионов;
![]() заряды ионов;
заряды ионов;
![]() их радиусы,
их радиусы, ![]() .
.
Энергии активации электропроводности ![]() и
и ![]() для низко- и высокотемпературных участков определяли по графикам политерм электропроводности.
для низко- и высокотемпературных участков определяли по графикам политерм электропроводности.
Степень ионности ацетатов рассчитывали по формуле Полинга: ![]() , где
, где ![]() разность электропроводностей катиона и аниона.
разность электропроводностей катиона и аниона.
Графики удельной электропроводности (рисунок 1), как функции обратной абсолютной температуры ацетатов щелочных металлов, цинка и кадмия — ломанные линии, отрезки которых характеризуют собственную и примесную проводимость.
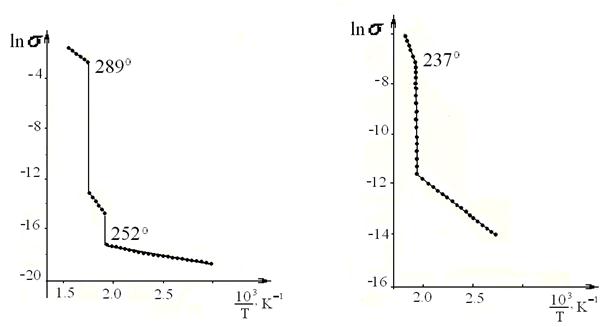
а б
Рисунок 1. Зависимость ![]() от
от ![]() для ацетатов а)
для ацетатов а) ![]() б)
б)![]()
В точках фазовых превращений первого рода электропроводность ацетатов меняется скачком. Она возрастает при переходе из нецентросимметричной структуры в центросимметричную. Изменение ионного состава в ряду ацетатов щелочных металлов порождает закономерное изменение параметров и сингонии кристаллической решетки.
Энергия активации удельной электропроводности, как в низкотемпературной ![]() , так и в высокотемпературной области
, так и в высокотемпературной области ![]() , уменьшается в ряду ацетатов от лития к калию и от цинка к кадмию, затем вновь начинает возрастать в ряду от калия к цезию. Таким образом, энергия активации имеет минимум у ацетата калия.
, уменьшается в ряду ацетатов от лития к калию и от цинка к кадмию, затем вновь начинает возрастать в ряду от калия к цезию. Таким образом, энергия активации имеет минимум у ацетата калия.
По-видимому, энергия активации, вычисленная по кривым ![]() , включает в себе энергию образования дефекта и энергию дрейфа иона.
, включает в себе энергию образования дефекта и энергию дрейфа иона.
Энергия образования дефекта зависит от энергии кристаллической решетки, удельных зарядов ионов, ее составляющих, и понижается с уменьшением последних.
Энергия дрейфа иона зависит от его размеров. Она возрастает с увеличением радиуса иона и с уменьшением его удельного заряда. У ацетата лития преобладает энергия образования дефектов. Она же уменьшается в ряду от лития к цезию. Энергия дрейфа иона, наоборот, увеличивается в указанной последовательности, достигая максимума у солей цезия. Таким образом, энергия активации у солей щелочных металлов складывается из величин с противоположной тенденцией. С уменьшением энергии кристаллических решеток и удельных зарядов ионов она падает за счет снижения энергии образования дефекта. С ростом радиуса мигрирующих ионов от лития к цезию возрастает энергия дрейфа ионов и энергия активации, достигнув минимума у солей калия, начинает возрастать за счет увеличения энергии дрейфа. Для солей ацетатов щелочных металлов энергия активации несколько меньше, чем для нитратов и нитритов. По-видимому, это объясняется относительно малой энергией дрейфа и малой энергией образования дефекта, хотя характер зависимости энергии активации от энергии кристаллической решетки совершенно аналогичный (рисунок 2).
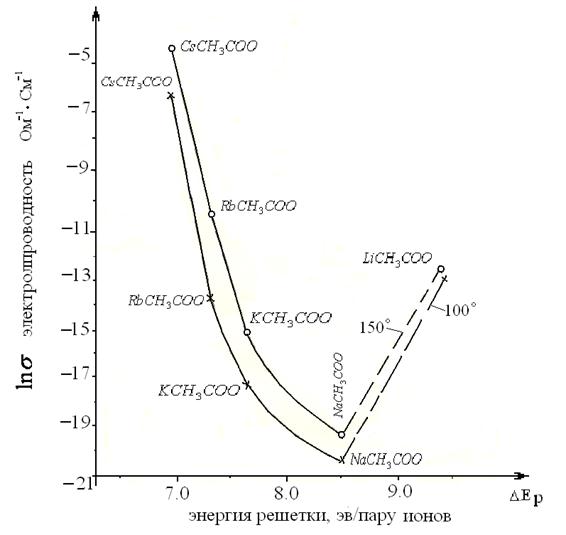
Рисунок 2. Зависимость ![]()
![]() при температурах 100 и 150 °С от энергии решетки для кристаллов ацетатов щелочных металлов
при температурах 100 и 150 °С от энергии решетки для кристаллов ацетатов щелочных металлов
На рисунке 2 приведена зависимость логарифма ионной электропроводности при 100 и 150 °С для кристаллов ацетатов щелочных металлов от энергии кристаллической решетки. Электропроводность кристаллов уменьшается при неизменном анионе с уменьшением радиуса катиона и с увеличением энергии решетки.
Электропроводность, соответствующая температуре плавления соли, повышается с переходом от ацетата цезия к ацетату натрия. Это обстоятельство свидетельствует об активной роли катиона при переносе тока через кристалл.
Таким образом, энергии активации ![]() ,
, ![]() , определяющие характер электропроводности вещества, зависят от энергии кристаллической решетки, радиуса ионов, удельных зарядов и электроотрицательности самих веществ. Электроотрицательность имеет прямую связь со степенью ионности вещества. Как видно из данных расчета существует обратная связь между энергией кристаллической решетки и степенью ионности данного ряда солей ацетатов.
, определяющие характер электропроводности вещества, зависят от энергии кристаллической решетки, радиуса ионов, удельных зарядов и электроотрицательности самих веществ. Электроотрицательность имеет прямую связь со степенью ионности вещества. Как видно из данных расчета существует обратная связь между энергией кристаллической решетки и степенью ионности данного ряда солей ацетатов.
Степень повышения ионной связи, несомненно, уменьшает энергию кристаллической решетки, понижает силу связи, закрепляющих ионы в структуре.
Энергия кристаллических решеток, удельные заряды и приведенные моменты ионов убывают от ![]() к
к ![]() от
от ![]() к
к ![]() , а ионные радиусы и степень ионности увеличивается в той же последовательности.
, а ионные радиусы и степень ионности увеличивается в той же последовательности.
Известно, что ацетаты относятся к классу ионных кристаллических соединений с функциональной группой ацетат-иона (![]() , характеризующегося угловым строением и довольно значительным удельным зарядом —
, характеризующегося угловым строением и довольно значительным удельным зарядом — ![]() эл.ст.единиц.
эл.ст.единиц.
К особенности строения ацетат-иона относится неравномерность распределения в нем плотности электрического заряда. Последнее указывает на реакционную способность ацетатов образовывать координационные соединения.
Выводы.
1. Изучены удельные электропроводности чистых ацетатов щелочных металлов и цинка в зависимости от температуры. Изменение электропроводности твердых солей ацетатов с температурой подчиняется уравнению ![]() а удельные электропроводности расплавов ацетатов меняются в зависимости от характера изменения энергии кристаллической решетки.
а удельные электропроводности расплавов ацетатов меняются в зависимости от характера изменения энергии кристаллической решетки.
2. Значения энергий активаций, энергий кристаллических решеток, удельные заряды ионов ацетатов в низкотемпературной области убывают в ряду от лития к цезию и от цинка к кадмию, а в высокотемпературной области для этого ряда функция энергии активации от температуры образует экстремальную кривую с минимумом у ацетата калия.
3. Электропроводность твердых солей ацетатов щелочных металлов уменьшается при неизменном анионе с уменьшением радиуса катиона и с увеличением энергии решетки.
Список литературы :
1.Воробьев А.А. Изоляционные свойства, прочность и разрушение диэлектриков. Новосибирск: Изд-во СО АН СССР, 1960. — 202 с.
2.Краснова К.С. Физическая химия. В 2 кн. М.: Высшая школа, 2001. — 512 с.
3.Кузьмина М.Ю. Электрохимия расплавленных солей. Иркутск: 2008. — 84 c.
4.Лидьярд А.А. Ионная проводимость кристаллов. М.: ИЛ, 1962. — 224 с.
дипломов

