Статья опубликована в рамках: LI Международной научно-практической конференции «Инновации в науке» (Россия, г. Новосибирск, 30 ноября 2015 г.)
Наука: Химия
Скачать книгу(-и): Сборник статей конференции, Сборник статей конференции часть II
- Условия публикаций
- Все статьи конференции
дипломов
Статья опубликована в рамках:
Выходные данные сборника:
ИССЛЕДОВАНИЕ РЕАКЦИОННОЙ СПОСОБНОСТИ СЕРУСОДЕРЖАЩИХ АМИНОКИСЛОТ
Васина Янина Александровна
канд. хим. наук, доцент кафедры химии ННГАСУ, РФ, г. Нижний Новгород
Е-mail: vasina1@rambler.ru
Яблоков Вениамин Александрович
д-р хим. наук., профессор, зав. кафедрой химии ННГАСУ, РФ, г. Нижний Новгород
REACTIVITY STUDIES OF SULPHUR CONTAINING AMINO ACIDS
Yanina Vasina
candidate of Chemical Science, Assistant Professor of Chemistry Department of Nizhniy Novgorod State University of Architecture and Civil Engineering, Russia, Nizhniy Novgorod
Veniamin Yablokov
doctor of Chemical Sciences, Professor, Head of Chemistry Department of Nizhniy Novgorod State University of Architecture and Civil Engineering, Russia, Nizhniy Novgorod
АННОТАЦИЯ
Исследована термическая стабильность серусодержащих аминокислот, рассчитаны кинетические и активационные параметры, установлен механизм твердофазного термического превращения L-α-метионина, L-α-цистеина, L-α-цистина в вакуумированной системе.
ABSTRACT
The thermal stability of the sulfur-containing amino acids has been determined, the kinetic constants of rate reaction and the activation parameters were calculated, the mechanism of thermal conversion of solid phase of L-α-methionine, L-α-cysteine, L-α-cystine in evacuated system is obtained.
Ключевые слова: L-α-метионин; L-α-цистеин; L-α-цистин; вакуумированная система; кинетика; константы скорости; энергия активации; продукты реакции; механизм твердофазного превращения.
Keywords: L-α-methionine; α-L-cysteine; L-α-cystine; evacuated system; the kinetics; the constant of rate; the activation of energy; the products of reaction; solid phase of converting mechanism.
Микроорганизмы, растительный и животный мир на планете своим бесконечным разнообразием обязан уникальным молекулам белка. Белки выступают в качестве опорного структурообразующего полимера, построенного из 20 L-α-аминокислот. Это природные высокомолекулярные соединения обеспечивают все жизненные процессы любого организма. Серусодержащие аминокислоты входят в состав многих белков [1; 2; 4; 6]. Поэтому исследование термической стабильности этих аминокислот, их возможное участие в процессах образования полимеров явилось основанием для изучения их реакционной способности. Подобные данные в литературе практически отсутствуют. В работе [8] определена энергия активации разложения кристаллического метионина в присутствии кислорода воздуха. Согласно литературным данным по исследованию кинетики термического разложения серусодержащих аминокислот [9–11] получены кинетические и активационные параметры.
Целью нашей работы является исследование реакционной способности серусодержащих аминокислот и установление механизма твердофазного термического превращения L-α-метионина, L-α-цистеина и L-α-цистина в вакуумированой системе.
Мы использовали навески аминокислот (50 мг), включающий весь возможный спектр размеров частиц дисперсной фазы от 0,1 до 1,0 мм. Кинетические измерения проводили компенсационным методом в вакуумированной системе в статических условиях, которые описаны в [9]. С точки зрения кинетики химических процессов нет принципиальных различий в способе измерения скорости реакции по изменению количества прореагировавшего вещества (степень превращения) или количества продукта реакции. Убыль массы кристаллической аминокислоты пропорциональна количеству моль газообразных продуктов реакции. Поэтому мы рассчитывали константы твердофазного термического превращения аминокислот по уравнению реакции первого порядка. Состав газообразных продуктов реакции идентифицировали на хромато-масс-спектрометре Trace GC Ultra/DSQII.
На рис. 1–3 приведены кинетические кривые превращения L-α-метионина (Met), L-α-цистеина (Cys) и L-α-цистина (Cys2), снятые в координатах давление (р) – время реакции (t).

Рисунок 1. Зависимость давления газообразных продуктов превращения Met от времени в интервале температур: 1 – 216, 2 – 221, 3 – 226, 4 – 231, 5 – 236 0С

Рисунок 2. Зависимость давления газообразных продуктов превращения Cys от времени реакции при следующих температурах: 1 – 194, 2 – 198, 3 – 201, 4 – 206, 5 – 225 0С
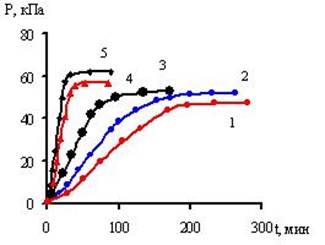
Рисунок 3. Зависимость давления газообразных продуктов превращения Cys2 от времени реакции в интервале температур: 1 – 199, 2 – 204, 3 –210, 4 – 218, 5 – 224 0С
Термическое разложение аминокислот подчиняется уравнению реакции первого порядка до глубины превращения 30–50 %.
Температурная зависимость констант скорости реакции описывается уравнением Аррениуса k = k0×e-E/RT (рис. 4). Кинетические и активационные параметры превращения серусодержащих аминокислот приведены в табл. 1.
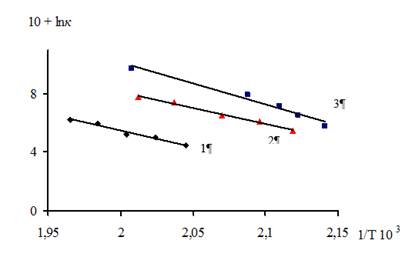
Рисунок 4. Температурная зависимость констант скорости реакции термического превращения 1 – Met, 2 – Cys2, 3 – Cys
Таблица 1.
Кинетические и активационные параметры превращения серусодержащих аминокислот
Аминокислота |
Т, ºС |
k×103, мин-1 |
k230 ×103,мин-1 |
Е, кДж/моль |
lnk0 |
Met |
216 221 226 231 236 |
4 6 7 17 22 |
15.1 |
195 ± 10 |
42.7±8
|
Cys |
194 198 201 206 225 |
25 53 85 190 728 |
1567 |
193±15 |
46.6±5
|
Cys2 |
199 204 210 218 224 |
13 17 27 75 117 |
223
|
184±7 |
42.5±6
|
Константы скорости превращения аминокислот растут в ряду Met<Cys2<Cys, (табл. 1, рис. 4) и отличаются в указанной последовательности на порядок. Кажущиеся энергии активации термораспада (Е) лежат в пределах 184–195 кДж/моль, lnk0 в интервале 42–47.
Серусодержащие аминокислоты, такие как Cys и Cys2, относятся к классу тиолов, Met – замещенных тиолов. Большинство реакций тиолов относится к гетеролитическим реакциям нуклеофильного присоединения или замещения. Однако, тиолы особенно при высоких температурах также склонны к образованию тиольных радикалов за счет гомолиза S-C связи [3].
При термическом превращении Met образуется полимерная масса вещества, дающая положительную биуретовую реакцию на амидную группу в олигопептиде. В газовой фазе масс-спектрометрическим методом найдены СО2, метилтиол СН3SH, а также следы H2S и (СН3)2S2; по остаточному давлению при комнатной температуре определено, что 50 % газовой фазы составляет вода-продукт поликонденсации. Хромато-масс-спектрометрическим методом в конденсированной фазе обнаружены: 3-метилтио-1-пропиламин, метилтиол и 1-аминопропен-2. Вероятная схема термического превращения Met может быть представлена следующими параллельно и последовательно протекающими реакциями.
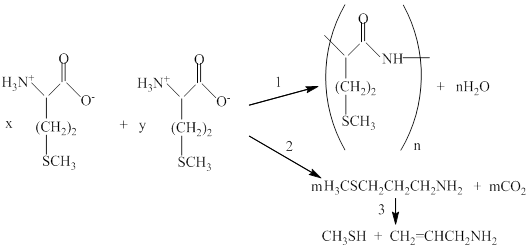
Вода, метилтиол и СО2 переходят из кристалла в газовую фазу и вместе с водой определяют в ней состав продуктов превращения Met.
В отличие от гетеролитической реакции поликонденсации 1 появление СО2 и метилтиола является следствием гомолитического расщепления связей С-S и С-O в кристалле (реакции 2 и 3).
Термическое превращение Cys и Cys2, также как и Met, сопровождается образованием олигомера (положительная биуретовая реакция). Газовая фаза состоит наполовину из воды, H2S и СО2 для Cys и Cys2 соответственно. Как показали рассчеты, на моль Cys образуется примерно 2 моль летучих веществ - Н2О и H2S. Количества СО2 в газовой фазе незначительны. В кристаллических структурах Cys и Cys2 происходит, вероятно, гетеролитический процесс поликонденсации и последуюший гомолитический разрыв связи С-S в образующемся олигомере, приводящий к образованию H2S.
Судьба образующихся радикалов очевидна. Это подтверждается образованием значительного количества H2S в газовой фазе.

Вероятно, существенную роль играют также внутримолекулярные процессы циклизации, приводящие к образованию незначительных количеств метилтиазола, метилтиоазолидиена и производных пиридина и тиофена. Связь С–N в процессе термораспада этих аминокислот не подвергается разрыву. Об этом свидетельствует отсутствие в продуктах NH3.
Из литературных источников [7] известна реакция взаимопревращения Cys и Cys2.

Найдено, что для этих аминокислот практически одинаковые продукты термопревращения, что свидетельствует о возможности протекания этой равновесной реакции в условиях нашего эксперимента.
Таким образом, формально скорость брутто-процесса превращения L-α-Met, L-α-Cys и L-α-Cys2 при небольших глубинах разложения исходных соединений (30-50%) можно рассматривать как «кооперативную» химическую реакцию поликонденсации [5] первого порядка, протекающую в кристаллической фазе. Несмотря на близкие значения кажущихся энергий активации термопревращения L-α-Met, L-α-Cys и L-α-Cys2 соответственно равных 195, 193 и 184 кДж/моль, эффективные константы реакции при одной и той же температуре отличаются один от другого на порядок в ряду Met<Cys2<Cys. При температурах выше 200 ºС их превращение в вакууме сопровождается образованием серусодержащих газообразных продуктов и жидких азотсодержащих гетероциклических соединений.
Список литературы:
- Гринштейн Дж. Химия аминокислот и пептидов / Гринштейн Дж., Винниц М., под ред. Шемякина М.М. – М.: Мир, 1965. – 821 с.
- Мазо В.К. Глутатион как компонент антиоксидантной системы жедудочно-кишечного тракта / Мазо В.К. //Журнал гастроэнтерологии, гепатологии. – 1998. – № 1. – С. 47.
- Общая органическая химия / Под ред. Кочеткова Н.К. и Нифантьева Э.Е. – Т. 5. – М: Химия, – 1983. – С. 130–163.
- Овчинников Ю.А. Биоорганическая химия / Овчинников Ю.А. М: Просвещение, 1987. – 815 с.
- Семчиков Ю.Д. Высокомолекулярные соединения / Семчиков Ю.Д. «Академия», – 1983. – 368 с.
- Торгинский Ю.М. Сера в белках / Торгинский Ю.М. М.: Наука, 1977. – 302 с.
- Тюкавкина Н.А. Биоорганическая химия / Тюкавкина Н.А., Бауков Ю.А. – М.: Дрофа, – 2010. – 544 с.
- Vicol O. Some complex combinations of Pd(II) with methionine / Vicol O., Hurduc N., Schneider I.A. // J. Inorg. nucl. chem. – 1979. – Vol. 41. – Р. 309.
- Яблоков В.А. Кинетика термического разложения серусодержащих аминокислот / Яблоков В.А., Васина Я.А., Зеляев И.А., Митрофанова С.В // Ж. общ. хим. – 2009. – Т. 79. – Вып. 6. – С. 969–971.
- Яблоков В.А. Исследование реакционной способности метионина и его комплекса с хлоридом ртути / Яблоков В.А., Васина Я.А., Зеляев И.А., Митрофанова С.В. //Приволжский научн. ж. Изд. Н. Новгород: ННГАСУ, – 2008. – № 1. – С. 110–112.
- Яблоков В.А. Сравнительная кинетика термического разложения глутатиона, цистеина и глицина / Яблоков В.А., Васина Я.А. // Приволжский науч. жур. Изд. Н. Новгород: ННГАСУ, – 2012 – № 4 – С. 169–171.
дипломов

