Статья опубликована в рамках: III Международной научно-практической конференции «Научное сообщество студентов: МЕЖДИСЦИПЛИНАРНЫЕ ИССЛЕДОВАНИЯ» (Россия, г. Новосибирск, 23 мая 2012 г.)
Наука: Химия
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
ИССЛЕДОВАНИЕ ВЛИЯНИЯ УСЛОВИЙ СИНТЕЗА ГИДРОКСИЛАПАТИТА НА РН НУЛЕВОГО ЗАРЯДА И РАЗМЕР КРИСТАЛЛИТОВ
Васина Яна Александровна
студентка 2 курса, кафедра химии БГУ, г. Брянск
Е-mail: Kisunya 25@mail.ru
Стринадкина Юлия Александровна
студентка 2 курса, кафедра химии БГУ, г. Брянск
Абросимова Валерия Сергеевна
ученица 10 класса, лицей № 27, г. Брянск
Зубкова Кира Алексеевна
ученица 10 класса, лицей № 27, г. Брянск
E-mail: KiraBr1995@yandex.ru
Кузнецов Сергей Викторович
Научный руководитель, канд. хим. наук, доцент БГУ, г. Брянск
Шевко Оксана Анатольевна
учитель химии, лицей №27, г. Брянск
Гидроксилаппатит (ГА) является основной минеральной составляющей костной ткани. В связи с этим он используется в качестве временного замещающего агента или основой в костной хирургии, а так же в качестве основы для создания напыленных биосовместимых покрытий на титане, оксидных керамиках и полимерных замещающих элементах. Гидроксилапатит и покрытие на его основе обладают высоким биологическим сродством.
Существует большое количество методик синтеза гидроксилапатита (твердофазный синтез, гидротермальный синтез, механотермический синтез, получение из растворов в результате обменных реакций и реакции нейтрализации) [1]. Наиболее чистые фазы гидроксилапатита получают по реакции:
10Ca(OH)2+6H3PO4 → Ca10(PO4)6(OH)2+18H2O
Метод осаждения из растворов отличается простотой аппаратного исполнения, контролируемостью, низкими энергетическими затратами и высокими выходами продукта. Но имеется большое количество работ, в которых указываются различные условия по концентрации гидроксида кальция, фосфорной кислоты, скорости прибавления растворов, температуры, значению рН конечной точки.
В предварительном эксперименте нами было выяснено, что все указанные факторы влияют на состав гидроксилапатита, степень сформированности кристаллической решетки и рН нулевого заряда (рН0).
рН0 определяется строением двойного электрического слоя [2] и в свою очередь определяет дальнейшее участие гидроксилапатита в адсорбционных процессах, процессах растворения или формирования костной ткани.
Если рН нулевого заряда больше рН раствора (крови, тканевой жидкости), то поверхность заряжается положительно. Если рН нулевого заряда меньше рН раствора, то поверхность заряжается отрицательно. При равенстве заряд поверхности равен нулю. Создание материала с заданным значением рН нулевого заряда позволяет управлять процессами адсорбции, растворения, замещения или формирования новой костной ткани.
Заряд поверхности определяет возможность или невозможность адсорбции белков - стимуляторов роста остеобластов.
В связи с вышесказанным, нами была поставлена цель: исследовать влияние различных факторов при синтезе гидроксилапатита по методу нейтрализации на рН0 и кристаллическое состояние.
Методика эксперимента:
1.Методика синтеза.
Для синтеза гидроксилапатита нами использовался метод осаждения из растворов (мокрый метод).
Этот метод отличает простота, контролируемость, низкие энергетические затраты, высокий выход продукта и возможность достичь хорошую воспроизводимость, сохранить стехиометрическое соотношение Са/Р в процессе синтеза, т.е. получить продукт с заданными химическими и физическими свойствами. Среди множества факторов (как было выяснено в предварительных экспериментах) наиболее критичными являются рН раствора, температура реакции и продолжительность процесса. В зависимости от условий синтеза, может быть получен порошок с различной морфологией, удельной поверхностью, стехиометрией и степенью кристалличности [1].
В качестве кальцийсодержащего реагента использовался насыщенный раствор гидроксида кальция, который получали растворением избытка оксида кальция в воде:
CaO + H2O → Ca(OH)2
В качестве фосфатсодержащего реагента – раствор ортофосфорной кислоты с массовыми долями 1%, 10%, 30%. Кислота прибавлялась по каплям с различной интенсивностью до установления рН 7,5-10,5. Затем суспензию гидроксилапатита оставляли на сутки для осаждения. Осадок многократно промывали декантацией, промытый продукт высушивался при 75°С.
2. Потенциометрическое титрование.
Нами была использована одна из разновидностей метода потенциометрического титрования - метод внесения отдельных навесок, или метод присыпания. В ячейку для измерения рН помещали 50 мл рабочего раствора (0,9% NaCl) c заданным значением рН и всыпали навеску гидроксилапатита 0,05![]() 0,0003 г, измеряли временную зависимость рН. рН исходных растворов изменяли с помощью концентрированной соляной кислоты и насыщенного раствора гидроксида натрия. Измерения проводили на иономере «Мультитест ИПЛ 112» со стеклянным и хлорсеребряным электродами. Полученные данные обрабатывали в программе Excel. При построении графика в координатах время (t) ‑ рН по точке схождения кривых, определяли рН0.
0,0003 г, измеряли временную зависимость рН. рН исходных растворов изменяли с помощью концентрированной соляной кислоты и насыщенного раствора гидроксида натрия. Измерения проводили на иономере «Мультитест ИПЛ 112» со стеклянным и хлорсеребряным электродами. Полученные данные обрабатывали в программе Excel. При построении графика в координатах время (t) ‑ рН по точке схождения кривых, определяли рН0.
3. Методика получения рентгеновских спектров.
Рентгеновские дифракционные спектры снимались на рентгеновском универсальном спектрометре СУР «Реном» 01 по геометрии Брэгга‑Брентано на медном К-α излучении, с последующей идентификацией по базам PDF‑2.
Экспериментальные данные и их обсуждение:
На рисунке 1 представлены характерные зависимости изменения рН раствора от времени после присыпания гидроксилапатита и найденное значение рН0. Из рисунка видно, что при внесении навески в раствор с меньшим значением рН, чем рН0, происходит увеличение рН раствора, а при внесении в раствор с большим значением - уменьшение, изменение тем больше, чем дальше значение рН раствора от рН0 гидроксилапатита. В таблице представлены условия и значения рН0 синтезированных образцов:
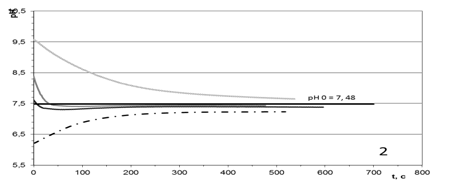
Рисунок 1. Кривые потенциометрического титрования методом присыпания.
Таблица.
Условия синтеза и значения рН0 синтезированных образцов.
|
№ |
ω(Н3РО4), % |
VCa(OH)2, мл |
V H2O, мл |
T, °С |
pH было |
рН стало |
рН0 |
|
1 |
30 |
2000 |
0 |
19 |
12.6 |
7.85 |
7.21 |
|
2 |
30 |
2000 |
0 |
20 |
12.63 |
10 |
7.25 |
|
3 |
10 |
2000 |
0 |
19 |
12.87 |
8 |
7.125 |
|
4 |
10 |
2000 |
0 |
20 |
12.94 |
9.88 |
7.12 |
|
5 |
1 |
2000 |
0 |
20 |
12.87 |
8.01 |
6.98 |
|
6 |
1 |
2000 |
0 |
22 |
13.32 |
8.1 |
7.33 |
|
7 |
1 |
2000 |
0 |
20 |
13.37 |
8.01 |
7.44 |
|
8 |
1 |
1000 |
1000 |
22 |
13.04 |
8 |
6.77 |
|
9 |
30 |
1500 |
1500 |
20 |
13 |
8.18 |
6.83 |
|
10 |
30 |
1500 |
1500 |
20 |
13 |
7.78 |
6.81 |
|
11 |
10 |
1500 |
1500 |
21 |
12.53 |
7.98 |
6.83 |
|
12 |
10 |
1500 |
1500 |
20 |
13.07 |
10.12 |
6.8 |
|
13 |
1 |
1500 |
1500 |
20 |
12.6 |
7.94 |
7 |
|
14 |
30 |
1500 |
1500 |
21 |
12.62 |
9.97 |
7.125 |
Из полученных данных следует, что высокая концентрация фосфорной кислоты и гидроксида кальция способствует формированию гидроксилапатита с высоким значением рН0. Как видно из рис. 2, кривые изменения рН раствора после присыпания навески такого гидроксилапатита имеют характерный s-образный изгиб указывающий на наличие избыточных прочно адсорбированных анионов (но рН0 при адсорбции поверхностно активных анионов должно смещаться в щелочную область [3])
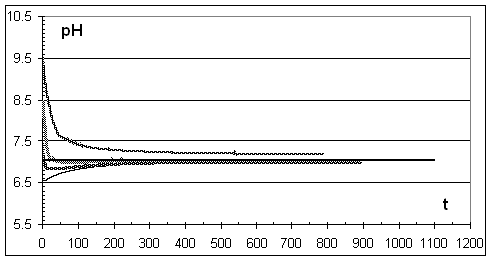
Рисунок 2. Кривые потенциометрического титрования методом присыпания.
Сравнение формы кривых потенциометрического титрования, рН конечного гидроксилапатита и диаграммы распределения форм фосфат-ионов от рН позволяет сделать вывод о том, что именно НРО42- ионы адсорбируются на поверхности. Что приводит к образованию на поверхности фосфата кальция и смещению рН0 в кислую область к значениям характерным для фосфата кальция.
На рис. 3 представлены дифракционные спектры образцов, синтезированных при различных температурах реакционной смеси. Сравнение полученных спектров, показало полную идентичность со спектрами гидроксилапатита. Сравнение спектров между собой указывает на увеличение степени кристалличности с повышением температуры синтеза. Спектры образцов, полученных при температурах 0˚С и 20˚С мало различаются между собой. Спектр образца, полученного при 60˚С, имеет хорошо выраженные более узкие пики, что указывает на высокую степень сформированности кристаллической решетки и более крупные кристаллиты.
Нами не выявлено значительного изменения ширины пиков после проведения промывки, хотя при промывке наблюдался частичный унос мелкодисперсной фазы и некоторое уширение полос. Из чего можно сделать вывод, что синтезированный образец имеет разделение не по степени кристалличности, а по количеству слипшихся кристалликов.
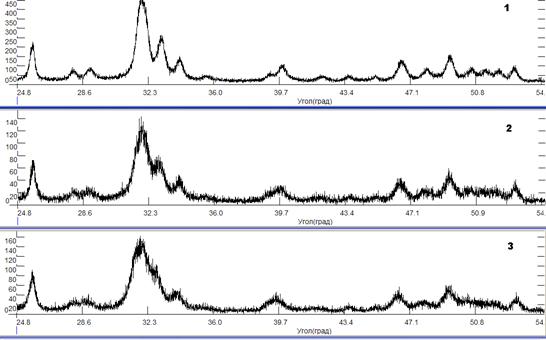
Рис. 3. Дифракционные спектры для ГА, синтезированного при 60˚С (1), 20˚С (2) и 0˚С (3).
Выводы:
1) Скорость приливания, различные соотношения концентраций реагентов, рН конечной точки не влияют на размер кристаллитов, а влияют на рН0 и чистоту фазы.
2) Повышение температуры проведения синтеза позволяет получать более крупные и правильно сформированные кристаллы.
3) Окончание синтеза при рН 9‑10 позволяет избежать загрязнение гидроксилапатита адсорбционным фосфатом, и получить продукт со стабильным рН0 (7,4).
Список литературы:
1.Баринов С. М., Комлев В. С. Биокерамика на основе фосфатов кальция. М.: Наука, 2005, с. 204.
2.Davis J. A., James R. D., Leckie J. O. Surface lonization and Complexaition at the Oxide/Water Interface. // J. Colloid Interface Sci. 1978. V. 63. № 3. Р. 480‑499.
3.Горичев И. Г., Батраков В. В., Шаплыгин И. С., Дятлова Н. М., Михальченко И. С. Комплексообразование на поверхности гидрооксидов железа. //Неорганические материалы. 1994, Т.30, № 10, С. 1203‑1218, С. 1219‑1234.
дипломов

