Статья опубликована в рамках: VI Международной научно-практической конференции «Научные достижения биологии, химии, физики» (Россия, г. Новосибирск, 04 апреля 2012 г.)
Наука: Химия
Секция: Неорганическая химия
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
НОВАЯ ФАЗА В ТРОЙНОЙ СИСТЕМЕ ИЗ ОКСИДОВ ЛИТИЯ, МАРГАНЦА (+2) И НИОБИЯ СО СЛОИСТОЙ СТРУКТУРОЙ
Ганноченко Алексей Анатольевич
преподаватель, ЮФУ, г. Ростов-на-Дону
E-mail: aaganochenco@rambler.ru
Впервые полученные в [3] слоистые соединения состава Li3M0,5Nb2O7 (М=Mg, Zn) являются изоструктурными фазами с общей формулой Li4-2xMxNb2O7. Учитывая близость ионных радиусов и координационных предпочтений Mn2+ к указанным двухвалентным катионам, изучен ряд возможных растворов состава Li4-2xMnxNb2O7 с 0,4<x<1,0.
Исследуемые образцы готовили с помощью твердофазного синтеза. На первом этапе синтезировали прекурсоры — ниобаты лития и марганца (+2). Порошки высшего оксида ниобия и оксида марганца (+3) (или карбоната лития) перетирали, прессовали в таблетки и обжигали в атмосфере водорода с промежуточным перетиранием при температурах 600—700 и 900—10000С соответственно. На втором этапе из полученных двойных оксидов готовили образцы тройной системы. Конечный синтез проходил в атмосфере водорода при температуре 10500С.
По данным рентгенофазового анализа, дифрактограмма образца состава Li2,2Mn0,9Nb2O7 (x=0,9) схожа с дифрактограммами аналогичных магниевой и цинковой фаз [1] с небольшим смещением интерференционных максимумов в низкоугловую область. Образцы с x=0,95 и 0,85 уже содержали примесные фазы, содержание которых закономерно увеличивалось по мере отдаления состава образцов от однофазного. Таким образом, область гомогенности полученного соединения практически отсутствует. Последующие опыты показали, что это соединение получается из различных исходных веществ, что доказывает его существование в системе, как равновесной фазы при температуре синтеза. Различие параметров решетки Li3Mg0,5Nb2O7 и Li3Zn0,5Nb2O7 и полученного в этой работе Li2,2Mn0,9Nb2O7 согласуются с различием ионных радиусов этих двухвалентных катионов [2] (табл. 1)
Таблица 1
Сравнение параметров решетки Li4-2xMxNb2O7, M = Mg, Zn, Mn (пр. гр. Сc).
|
|
a, Å |
b, Å |
c, Å |
β, 0 |
V, Å3 |
Лит. |
|
Li3Zn0,5Nb2O7 |
10,631 |
5,084 |
9,878 |
99,98 |
525,81 |
[3] |
|
Li3Mg0,5Nb2O7 |
10,649 |
5,091 |
9,868 |
100,2 |
526,53 |
[3] |
|
Li2,2Mn0,9Nb2O7 |
10,8273 |
5,1557 |
9,8947 |
99,988 |
543,98 |
[Наши данные] |
Проведено полнопрофильное уточнение структуры нового соединения с использованием программного комплекса GSAS. В качестве стартовой модели использованы структурные параметры цинкового аналога Li3Zn0.5Nb2O7 с пространственной группой Cc, которые получены из очень точных рентгеновских дифракционных данных на монокристалле. Конечные результаты уточнения представлены в табл. 2.
Таблица 2
Координаты атомов и заселенности позиций в структуре Li2,2Mn0,9Nb2O7.
|
Атом |
Позиции Вайкова |
Заселенность |
Координаты атомов |
||
|
x |
y |
z |
|||
|
Nb1 |
4a |
1 |
0,060 |
0,244 |
0,0580 |
|
Nb2 |
4a |
1 |
0,442 |
0,253 |
0,412 |
|
Mn1 |
4a |
0,21(1) |
0,363 |
0,26 |
0,734 |
|
Mn2 |
4a |
0,41(1) |
0,219 |
–0,24 |
0,403 |
|
Mn3 |
4a |
0,38(1) |
0,117 |
0,28 |
0,242 |
|
Mn4 |
4a |
0,04(1) |
0,260 |
0,27 |
0,15 |
|
O1 |
4a |
1 |
0,435 |
0,42 |
0,585 |
|
O2 |
4a |
1 |
0,065 |
0,06 |
0,392 |
|
O3 |
4a |
1 |
0,112 |
0,58 |
0,539 |
|
O4 |
4a |
1 |
0,377 |
–0,07 |
0,473 |
|
O5 |
4a |
1 |
0,005 |
0,396 |
0,758 |
|
O6 |
4a |
1 |
0,305 |
0,422 |
0,328 |
|
O7 |
4a |
1 |
0,205 |
0,106 |
0,682 |
Полученные результаты позволяют сделать заключение, что жесткая часть решетки нового соединения построена из искаженных октаэдров, соединенных ребрами в цепочки типа вольфрамита. Далее эти цепочки имеют угловое сочленение в параллельные вдоль (100) слои состава Nb2O7 (рис. 1). Эти цепочки соединены вершинами октаэдров так, что формируют бесконечные слои Nb2O7, параллельные (100). Это, в частности, объясняет преимущественную ориентацию зерен. Атомы лития и марганца распределены по четырем типам искаженных октаэдрических позиций. Как уже отмечалось ранее, нет специфических позиций марганца. Таким образом, полученное соединение по существу нестехиометрическое, и может рассматриваться как твердый раствор Li4-2xMnxNb2O7 на основе несуществующего Li4Nb2O7, т. е. является типичным бертоллидом, как и его цинковый и магниевый аналоги.
а)  b)
b) 
Рис. 1. Полиэдрическая модель структуры Li2,2Mn0,9Nb2O7;
a) вид перпендикулярно слоям остова, вдоль [100],
b) вид параллельно слоям остова, вдоль [010].
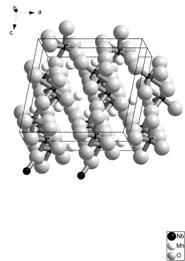
Рис. 2. Шаростержневая модель жесткого остова структуры Li2,2Mn0,9Nb2O7.
Мотив (Li,Mn)O6 — октаэдров, как (Li,Zn)O6 — октаэдров, идентичен мотиву ниобиевых октаэдров. Октаэдры NbO6 являются сильно ацентричными. Самые короткие и самые длинные связи Nb — O находятся в транс-положении и имеют длину 1,80 — 2,28 Å. Это типичное свойство оксониобатов, получающееся в результате сильной асимметрии p-связывания. Наличие ацентризма у ниобия в этой структуре объясняет отсутствие изоструктурного танталата, для которого ковалентные эффекты выражены слабее.
Список литературы:
- Шукаев И. Л. Твёрдофазные равновесия, кристаллохимия и ионная проводимость фаз в некоторых тройных системах, содержащих оксиды натрия (лития) и титана (ниобия, тантала): Дис. канд. химич. наук. Ростов-на-Дону. 1996. 217 с.
- Shannon R. D. / Revised effective ionic radii and systematic study of interatomic distances in halides and chalcogenides. //Acta Crystallografica. 1976. V. A32. N. 5. P. 751—767.
- Shukaev I. L., Shilov G. V., Avdeev M. Yu., Nalbandyan V. B., Medvedev B. S., Atovmyan L. O., Balagurov A. M./ Layered niobates with three-dimensional lithium ion conduction //In: The fourth conference Solid State Chemistry 2000, September 3 — 8, Prague, Czech Republic. P. 92—93.
дипломов
