Статья опубликована в рамках: XXXIII Международной научно-практической конференции «Инновации в науке» (Россия, г. Новосибирск, 28 мая 2014 г.)
Наука: Химия
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
Статья опубликована в рамках:
Выходные данные сборника:
КИНЕТИКА КАТАЛИТИЧЕСКОГО ОКИСЛЕНИЯ МЕТИЛЛИНОЛЕАТА В ПРИСУТСТВИИ ЭКСТРАКТА ЭЛЕУТЕРОКОККА И АСКОРБИНОВОЙ КИСЛОТЫ
Перевозкина Маргарита Геннадьевна
канд. хим. наук, старший преподаватель Государственного аграрного университета Северного Зауралья, РФ, г. Тюмень
KINETICS OF CATALYTIC OXIDATION METHYL LINOLEATE IN THE PRESENCE OF EXTRACT ELEUTHEROCOCCUS AND ASCORBIC ACID
Margarita Perevozkina
candidate of chemical sciences, Head teacher of State Agrarian University of Northern Transurals, Russia, Tyumen
АННОТАЦИЯ
В модельной системе каталитического окисления метиллинолеата установлен эффект синергизма в совместном антиоксидантном действии экстракта элеутерококка и аскорбиновой кислоты. Диапазоны оптимальных концентраций для экстракта элеутерококка и аскорбиновой кислоты, соответствующие максимальной эффективности антиоксидантной смеси, составляли (0,025—0,25) % и (2—8) ´ 10-4 М соответственно.
ABSTRACT
In the model system catalytic oxidation of methyl linoleate has the effect of synergism in joint antioxidant action of the extract of Eleutherococcus and ascorbic acid. The optimal ranges of concentrations for Eleutherococcus extract and ascorbic acid corresponding to the maximum efficiency of the antioxidant mixture was (0,025—0,25) % and (2—8) ´ 10-4 М, respectively.
Ключевые слова: антиоксиданты; пероксидное окисление; аскорбиновая кислота; экстракт элеутерококка.
Keywords: antioxidants; peroxide oxidation; ascorbic acid; Eleutherococcus extract.
В настоящей работе исследована антиоксидантная активность суммы компонентов экстракта корней элеутерококка (ЭЭ) и аскорбиновой кислоты (АК). Известно, что элеутерококк оказывает многостороннее действие на организм: возбуждает центральную нервную систему, усиливает двигательную активность и условнорефлекторную деятельность, повышает основной обмен, понижает содержание сахара в крови, обладает гонадотропными свойствами [3, 4]. Известна более высокая фармакологическая активность комплексного препарата ЭЭ по сравнению с его отдельными компонентами. Дардымовым И.В. [4] выделена гликозидная фракция из метанольного экстракта корней элеутерококка, в которой обнаружено семь гликозидов, названных элеутерозидами: 3-0-b-Д-глюкозид b-ситостерина (А), 4-b-глюкозид синапового спирта (В), 7-a-глюкозид изофраксидина (В1), этил-a-Д-гактозид (С), диглюкозиды (-) — сирингарезинола (Д и Е), а также гликозид F, которые находятся в соотношении : 8 : 30 : 10 : 12 : 24 : 2 : 1. Большинство гликозидов выделено в кристаллическом виде, установлена их химическая структура, которая приведена ниже.
Изученные гликозиды представляют собой моно- или биозиды. Кроме элеутерозидов, в экстрактах элеутерококка содержатся: глюкоза, сахароза, крахмал, полисахариды, воска, смолы, пектиновые вещества и многие другие соединения.
Аскорбиновая кислота (витамин С) является g-лактоном 2,3-дегидро-L-гулоновой кислоты. Характерной чертой структуры аскорбиновой кислоты является наличие ендиольной группы - C = C -, которая определяет высокую биологическую активность и окислительно-восстановительные свойства соединения [1]. Отсутствие токсичности, высокая физиологическая активность, лечебный эффект, окислительно-восстановительные свойства аскорбиновой кислоты стимулируют работы по ее использованию в качестве антиоксиданта для стабилизации качества пищевых продуктов или для антиоксидантотерапии. Целью настоящей работы являлось исследование антиоксидантной активности экстракта элеутерококка и аскорбиновой кислоты при совместном каталитическом окислении метиллинолеата.
Материалы и методы
Антиоксидантную активность (АОА) изучали манометрическим методом поглощения кислорода в модифицированной установке типа Варбурга при окислении модельного субстрата метиллинолеата (МЛ) в присутствии триметилцетиламмоний бромида (ЦТМАБ) в качестве поверхностно-активного вещества (ПАВ) 1×10-3 М, с добавками раствора хлорида меди (II) в количестве 2×10-3 М при t=(60±0,2)0С. Соотношение липидов и воды составляло 1: 3, а общий объем пробы 4 мл [7]. Графическим методом [9] определяли величину периода индукции (ti), представляющую собой отрезок оси абсцисс, отсекаемый перпендикуляром из точки пересечения касательных к кинетической кривой. Эффективность торможения процесса окисления липидного субстрата определяли совокупностью реакций ингибитора и обозначали как антиоксидантную активность, количественно рассчитанную по формуле АОА= ti-tS /tS, где tS и ti — периоды индукции окисления субстрата в отсутствие и в присутствии исследуемого антиоксиданта (АО) соответственно. Из наклона кинетических кривых (КК) определяли начальную (Wнач.) и максимальную (Wмак.) скорости окисления липидного субстрата с добавками АО. Скорость инициирования определяли уравнением Wi = f [InH] / ti, где f — стехиометрический коэффициент ингибирования, [InH] — концентрация стандартного ингибитора, ti — период индукции. В качестве стандартного ингибитора использовали дибунол. Для установления характера совместного действия двух ингибиторов сопоставляли между собой простую сумму периодов индукции отдельных компонентов (аддитивное действие Στі) и брутто эффективность их смеси (τΣ). Если в результате сочетания ингибиторов получили выигрыш в периодах индукции (Δτ) по сравнению с аддитивным действием АО, т. е. (τΣ > Στі), то в совместном действии ингибиторов определялся эффект синергизма. В случае если совместное действие двух АО было меньше, чем сумма эффектов ингибирования индивидуальных веществ (τΣ < Στі), то делалось заключение о проявлении антагонизма в совместном действии АО. Эффект синергизма оценивали по разности Δτ =τΣ -Στі и в относительных единицах Δτ/Στі×100 %. В нашем эксперименте использовался экстракт элеутерококка колючего заводского производства (Eleutherocóccus senticósus), который выпаривали до постоянной массы и получали (0,0075—2,5) % водные растворы.
Результаты и их обсуждение
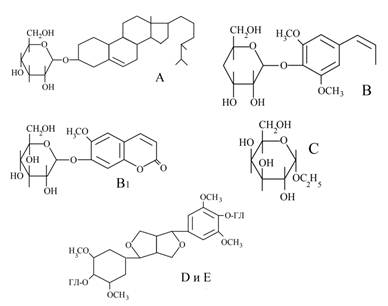
Гликозиды из корней элеутерококка
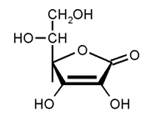
Схема 1. Аскорбиновая кислота
Исходя из структуры, первоначально предполагали, что аскорбиновая кислота не может проявлять антирадикальной активности, а должна быть синергистом в антиоксидантных композициях. К этому направлению относятся работы [13, 14, 15], в которых аскорбиновая кислота исследована как синергист в смеси с a-токоферолом. В работе [13] показано увеличение антиоксидантной активности a-токоферола в лярде в присутствии 0,01—0,05 % аскорбиновой кислоты. Подобные результаты получены для смесей a-токоферола с аскорбиновой кислотой в метилолеате, лярде [14]. Роль аскорбиновой кислоты связывают с восстановлением токофероксильных радикалов и регенерацией сильного ингибитора. В то же время синергическая активность аскорбиновой кислоты может быть обусловлена хелатированием катализаторов.
В обзоре Niki Е. [11, 12] аскорбиновая кислота отнесена к водорастворимым антирадикальным соединениям и показана ее возможность взаимодействия со свободными радикалами жирно-кислотных компонентов липидов. Между тем известно [5], что аскорбиновая кислота способна восстанавливать при окислении липидных субстратов менее активные Fe+3 до более активных Fe+2 или более активные Cu+2 до менее активных Cu+1. В клетке аскорбиновая кислота совместно с катионами может ускорять образование свободных, например, HO·- радикалов [2]. В этом случае добавки аскорбиновой кислоты будут ускорять или тормозить процесс окисления. Действительно, в ряде работ [8, 10, 16] показан прооксидантный эффект аскорбиновой кислоты in vitro. Известны работы по исследованию влияния приема аскорбиновой кислоты экспериментальными животными на уровень интенсивности ПОЛ [8]. Показано, что введение аскорбиновой кислоты снижает уровень ПОЛ. Выбор для исследований экстракта элеутерококка обусловлен высокой физиологической активностью его компонентов. Кроме того, известна [6] антиоксидантная активность экстракта элеутерококка в суспензии яичного желтка в присутствии катионов железа (II).
С целью прогнозирования антиоксидантной активности препарата изучено влияние отдельных его компонентов на окисление модельного субстрата. Установлено, что эффект аскорбиновой кислоты на каталитическое окисление МЛ зависит от концентрации и соотношения с катализатором. Добавки (1—10)×10-6 М аскорбиновой кислоты, соответствующие ее отношению с катализатором как 1:2000 и 1:200, вызывают ускорение процесса без изменения характера кинетических кривых (КК), при этом максимальная скорость процесса составляла (2,95—3,14)´10-4 М´с-1 (контроль МЛ 2,6´ 10-4 М´с-1). Вероятно, при избытке катализатора аскорбиновая кислота образует с ним комплексные соединения, катализирующие процесс окисления. В ряде работ показан прооксидантный эффект аскорбиновой кислоты. Известно, что аскорбиновая кислота является восстановителем и при ее избытке может происходить восстановление каталитически активной формы Cu2+ в неактивную Cu1+, что приводит к торможению процесса.

Рисунок 1. Кинетические кривые каталитического окисления МЛ в водно-липидной среде в присутствии добавок аскорбиновой кислоты, М: 1 — 1×10-6, 2 — 1×10-5, 3 — контроль, 4 — 1×10-3, 5 — 5×10-2, 6 — 1×10-1; CuCl2 2×10-3 М, t=600 C
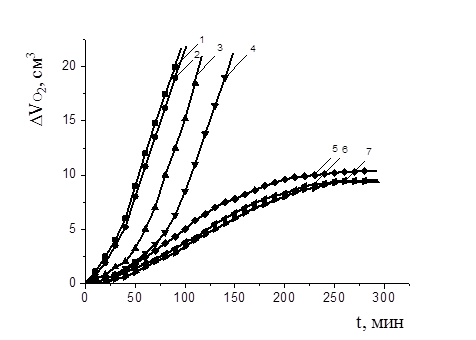
Рисунок 2. Кинетические кривые каталитического окисления МЛ в водно-липидной среде в присутствии добавок экстракта элеутерококка, %: 1 — контроль, 2 — 0,0075, 3 — 0,025, 4 — 0,125, 5 — 0,75, 6 — 1,25, 7 — 2,5; CuCl2 2×10-3 М, t=600C
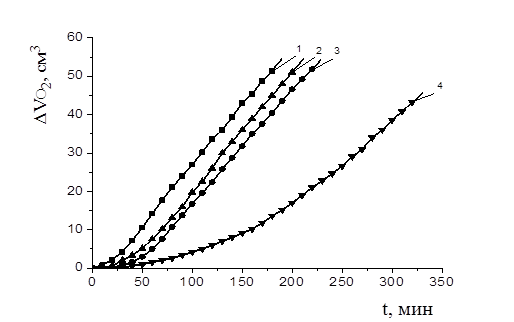
Рисунок 3. Кинетические кривые каталитического окисления МЛ в водно-липидной среде (1 — контроль) в присутствии добавок: 7,5×10-4 М аскорбиновой кислоты (2); 0,025 % экстракта элеутерококка (3) и их смеси в тех же концентрациях (4); CuCl2 2×10-3 М, t=600 C
В нашем эксперименте концентрации аскорбиновой кислоты, расположенные в диапазоне (1×10-4—1×10-1) М, существенно замедляли процесс (рис. 1). При этом значительно снижалась максимальная скорость окисления (3,35—9,60)´10-5 М´с-1, что связано со способностью аскорбиновой кислоты разрушать гидропероксиды с образованием молекулярных продуктов.
Таблица 1.
Результаты исследования антиоксидантных свойств аскорбиновой кислоты (АК), экстракта элеутерококка (ЭЭ) и их смесей
|
Состав |
С(АО)
|
tинд (AO), мин |
Sti, мин |
tΣ, мин |
Dt, мин |
(Dt/Sti)ґ100% |
|
АК |
7,5×10-4 М |
29 |
— |
— |
— |
|
|
АК |
2,5×10-3 М |
42 |
— |
— |
— |
— |
|
ЭЭ |
0,025 % |
40 |
— |
— |
— |
— |
|
ЭЭ |
0,125 % |
76 |
— |
— |
— |
— |
|
ЭЭ |
0,75 % |
80 |
— |
— |
— |
— |
|
АК |
7,5×10-4 М |
29 |
54 |
115 |
61 |
113,0 |
|
ЭЭ |
0,01 % |
25 |
||||
|
АК |
7,5×10-4 М |
29 |
69 |
180 |
111 |
160,9 |
|
ЭЭ |
0,025 % |
40 |
||||
|
АК |
7,5×10-4 М |
29 |
105 |
210 |
105 |
100,0 |
|
ЭЭ |
0,125 % |
76 |
||||
|
АК |
7,5×10-4 М |
29 |
114 |
220 |
106 |
93,0 |
|
ЭЭ |
0,25 % |
85 |
||||
|
АК |
7,5×10-4 М |
29 |
109 |
205 |
96 |
88,1 |
|
ЭЭ |
0,75 % |
80 |
Приведенные результаты показывают сложный характер воздействия аскорбиновой кислоты на процесс окисления: проявление каталитического действия и возможность ингибирования окисления. На основании экспериментальных данных были выбраны и использованы количества аскорбиновой кислоты, не обладающие инициирующим действием (7,5×10-4 М).
Это позволило описать действие бинарных концентраций аскорбиновой кислоты с суммой действующих веществ элеутерококка.
Экстракт элеутерококка представляет собой гликозиды по спиртовому или фенольному гидроксилу производных полициклических или ароматических углеводородов. Добавки экстракта элеутерококка при окислении модельного субстрата (0,025—0,125 %) воздействуют как типичные ингибиторы, тормозят начальные стадии при сохранении максимальной скорости (Рис. 2). Увеличение добавок экстракта (0,75—2,5 %) приводило к изменению формы КК: существенно снижалась начальная скорость окисления (3,40—4,20) ´ 10-5 М´с-1. За наблюдаемый период времени процесс не выходил на максимальную скорость окисления, описанную для малых концентраций.

Рисунок 4. Зависимость эффекта синергизма в композиции аскорбиновая кислота и экстракт элеутерококка от концентрации ЭЭ, %; С(АК) = const = 7,5´10-4 M, субстрат окисления – МЛ, Wi = 1,9×10-5 М×с-1, t = 600 C
Изучали совместное действие экстракта элеутерококка в концентрациях (0,025—0,75) % с аскорбиновой кислотой. При исследовании бинарных смесей аскорбиновой кислоты и экстракта элеутерококка было установлено проявление эффекта синергизма в их совместном действии. Периоды индукции, обеспечиваемые смесью веществ, значительно превышали простую сумму периодов индукции каждого компонента (аддитивное действие).
Так, величина периода индукции в присутствии индивидуальной аскорбиновой кислоты (С(АО) = 7,5×10-4 М) составляла 29 мин., для добавок экстракта элеутерококка (0,025 %) она равнялась 40 мин., бинарная смесь эффективно ингибировала окисление и обеспечивала период индукции, равный 180 мин. (рис. 3). Эффект синергизма составлял 160,9 % (рис. 4, табл. 1).
Механизм эффекта синергизма, установленного в совместном действии экстракта элеутерококка и аскорбиновой кислоты, связан с возможностью регенерации феноксильных радикалов, образующихся при окислении природных фенолов элеутерококка, вновь включающихся в процесс окисления в качестве ловушки свободных радикалов, ведущих процесс окисления.
Выводы:
1. Диапазоны оптимальных концентраций для экстракта элеутерококка и аскорбиновой кислоты, соответствующие максимальной эффективности антиоксидантной смеси, составляли (0,025—0,25) % и (2—8) ´ 10-4 М соответственно.
2. Обнаруженный эффект синергизма в сочетанном действии фенольных компонентов экстракта корней элеутерококка и аскорбиновой кислоты может иметь перспективы практического применения для стабилизации окисления природных липидов, фармацевтических препаратов, косметических средств.
Список литературы:
1.Гладких С.П. Аскорбиновая кислота и методы повышения ее устойчивости в лекарственных формах // Технология. — 1970. — С. 37—42.
2.Губский Ю.А. Регуляция перекисного окисления липидов в биологических мембранах // Биохимия животных и человека. — 1978. — № 2. — С. 72—76.
3.Дардымов И.В. Женьшень, элеутерококк. М.: Наука, 1976. — 184 с.
4.Дардымов И.В. Механизм действия препаратов женьшеня и элеутерококка Автореф. дис. … докт. мед. наук. Л.,1987. — 41 с.
5.Дремена Е.С., Шаров В.С. Кинетика Fe (2) — индуцированного перекисного окисления липидов в липосомах в присутствии аскорбиновой кислоты, концентрированные эффекты ионов Fe (2) // Биофизика. — 1995. — Т. 40. — № 2. — С. 335—340.
6.Еляков Г.Б., Оводов Ю.С. Гликозиды аралиевых // Химия природ. Соединений. — 1972. — № 6. — С. 697—709.
7.Перевозкина М.Г. Тестирование антиоксидантной активности полифункциональных соединений кинетическими методами. Новосибирск: Изд. СибАК, 2014. — 240 c.
8.Полякова Н.В., Шишкина Л.Н., Тырсин Ю.А. Влияние аскорбиновой кислоты и ее производных на перекисное окисление липидов in vitro и in vivo // Биоантиоксидант: Тез. докл. IV конф. М., — 1992. — Т. 1. — С. 39—40.
9.Цепалов В.Ф. Метод количественного анализа антиоксидантов с помощью модельной реакции инициированного окисления // Исследование синтетических и природных антиоксидантов in vivo и in vitro. М.: Наука, 1992. — С. 16—26.
10.Love Y.D., Plearson A.M. Lipid Oxidation in Meat and Meat Products A Rewiew // J. Amer. Oil Chem. Soc. — 1971. — Vol. 48. — № 10. — P. 547—549.
11.Niki E. Antioxidants in relation to lipid poroxidation // J. Chem. and Phys. Lipids. — 1987. — Vol. 44. — P. 227—253.
12.Niki E., Takahashi M., Komiko E. Antioxidant activi ty of vitamin E in liposomal membranes // Chemistry letters. — 1986. — № 9. — P. 1573—1576.
13.Privett O.S., Quackenbush A. The relation of synergist to antioxidant in fats // Amer. J. Oil Ehem. Poc. — 1954. — Vol. 31. — № 8. — P. 321—323.
14.Reinton R., Rogstad A. Antioxidant activity of tocopherols and ascorbic acid // J. Food. Sci. — 1981. — Vol. 46. — № 3. — P. 970—973.
15.Sedlacek B.A.Y. Mechanismus der Wirkung von A scorbylpalmitat und anderen Antioxidantien auf die Autoxidation der Fette // Nahrung. — 1975. — Vol. 19. — № 3. — P. 219—229.
16.Takahashi M., Niki E., Kawakami A. Oxidation of lipids. 14. Inhibition of oxidation of methyl linoleate by esters of ascorbic acid // Bull. Chem. Soc. Jan. — 1986. — Vol. 59. — № 10. — P. 3179—3183.
дипломов

