Статья опубликована в рамках: XLVII Международной научно-практической конференции «Инновации в науке» (Россия, г. Новосибирск, 29 июля 2015 г.)
Наука: Медицина
Скачать книгу(-и): Сборник статей конференции
- Условия публикаций
- Все статьи конференции
дипломов
Статья опубликована в рамках:
Выходные данные сборника:
МОРФОФУНКЦИОНАЛЬНАЯ ХАРАКТЕРИСТИКА СТРОМАЛЬНОГО КОМПОНЕНТА ПЕЧЕНИ БЕЛЫХ МЫШЕЙ, ПРИ ДЛИТЕЛЬНОМ ПОСТУПЛЕНИИ В ОРГАНИЗМ МАЛЫХ ДОЗ СВИНЦА И ФАРМАКОЛОГИЧЕСКОЙ КОРРЕКЦИИ ПРОЦЕССА
Купша Елена Ивановна
канд. мед. наук, ассистент кафедры гистологии и эмбриологии
Медицинской Академии Крымского федерального университета им. В.И. Вернадского,
РФ, г. Симферополь
E - mail : liver-life@yandex.ru
Бондаренко Владимир Витольдович
канд. мед. наук, доцент кафедры гистологии и эмбриологии
Медицинской Академии Крымского федерального университета им. В. И. Вернадского,
РФ, г. Симферополь
MORPHOFUNCTIONAL CHARACTERISTICS STROMAL COMPONENT LIVER OF WHITE MICE WITH PROLONGED ADMISSION INTO THE BODY SMALL DOSES OF LEAD ACETATE AND PHARMACOLOGICAL CORRECTION PROCESS
Elena Kupsha
c andidate of medical sciences, assistant of the Department of Histology and Embryology Medical Academy Crimean Federal University. V.I. Vernadsky,
Russia, Simferopol
Vladimir Bondarenko
candidate of medical sciences, associate professor of the Department of Histology and Embryology Medical Academy Crimean Federal University. V .I. Vernadsky,
Russia, Simferopol
АННОТАЦИЯ
Методами микроскопии, гисторадиоавтографии, морфометрии изучен стромальный компонент печеночных долек 54-х самцов белых мышей. Установлены морфофункциональные признаки срыва компенсаторно-приспособительных процессов при изолированном применении ацетата свинца. Применение витамина Е оказывает выраженный митогенный и мотогенный эффект с признаками избыточности. Эрбисол способствует наиболее полной реализации компенсаторно-приспособительных процессов, однако, может только отсрочить и минимизировать, а не предотвратить параллельно развертывающиеся дистрофические и деструктивные реакции.
ABSTRACT
By microscopy, gistoradioavtografii, morphometry studied stromal component of liver lobules of 54 male albino mice. Installed morfofunktcionalnye signs of failure of compensatory-adaptive processes in an isolated application of lead acetate. The use of vitamin E and has a pronounced mitogenic effect motogenic with signs of redundancy. Erbisol promotes the fullest realization of compensatory and adaptive processes, however, can only postpone and minimize, not prevent parallel unfolding dystrophic and destructive reactions.
К лючевые слова: печень; свинец; строма.
Keywords : liver; lead; stroma.
Актуальной задачей современной медицины является изучение клеток стромального дифферона обладающих профиброгенетическим потенциалом, выявление регуляторных путей их активации, реорганизации экстрацеллюлярной матрицы, модулирующих клеточную регенерацию гепатоцитов [9], с целью изыскания терапевтических подходов недопущения прогрессии в цирроз и печеночно-клеточной недостаточности. Фиброз печени при этом рассматривается, как динамический и специализированный процесс в ответ на хроническое гепатоцеллюлярное повреждение, развивающийся при накоплении экстрацеллюлярного матрикса (ЕСМ) включающего коллаген, протеогликан и адгезивные гликопротеиды, продуцируемые главным образом звездчатыми клетками, мезенхимального происхождения, локализованными между печеночными пластинками и синусоидальными эндотелиоцитами в пространстве Диссе. Неподвижные звездчатые клетки в физиологических условиях играющие важную роль в регуляции ретиноидного гомеостаза и ремоделировании ЕСМ продуцируя ее компоненты, так же как металлопротеиназы и их ингибиторы, в процессе фибриногенеза трансдифференцируются в миофибробластоподобные клетки, которые выполняют центральную роль в регуляции кровотока и развитие печеночного фиброза [5]. Фенотипическая трансформация (активация) звездчатых клеток характеризуется экспрессией генов обеспечивающие хемотаксис, пролиферацию, сократительную активность, ключевое участие в фиброгенезе и экстрацеллюлярной матричной деградации [10]. При прогрессирующем фиброзе, сопровождающем практически все хронические заболевания печени, возможно достижение конечной фатальной точки в виде цирроза, патологическим признаком которого является нарушение печеночной архитектуры, обширного накопления соединительной ткани и дисфункции печени, что закономерно ассоциируется с высоким уровнем смертности [8]. Также, кроме активизированных звездчатых клеток, миофибробласты печени, располагающиеся в перипортальных и перивенозных областях в нормальном состоянии, мигрируют к очагу повреждения и вовлекаются в фибротические изменения печени [3].
Целью нашей работы явилось определение морфофункциональных показателей стромальных компонентов печеночных долек для выявления степени выраженности развертывающихся компенсаторно-приспособительных реакций, в ответ на длительное поступление в организм малых доз свинца, а также при корригировании процесса фармакологическими препаратами.
Материал и методы
Трехмесячная свинцовая интоксикация моделировалась на 54-х половозрелых самцах белых мышей линии balb /c, которые получали перорально ацетат свинца в дозе 1 мг/100 г массы в течение 30, 60 и 90 суток. 15 животных служили контролем. Эксперимент включал 3 серии опытов. В 1-ой серии применяли ацетат свинца изолированно (18 мышей). Во 2-й серии использовали ацетат свинца в сочетании с пероральным введением альфа-токоферола (18 мышей). В 3-й серии использовали ацетат свинца в сочетании с подкожным введением препарата «Эрбисол» (18 мышей). Используемые методы: гистологический, электронномикроскопический, полутонких срезов, гисторадиоавтографии, морфометрический. Для получения сопоставимых результатов с применением метода гисторадиоавтографии эксперимент завершали в одно и то же время суток — 12 часов дня. За 1 час до взятия материала животным внутримышечно вводили меченный предшественник ДНК-3Н-тимидин в дозе 6,5 мкКu/г. Метод применен с целью установления активности синтеза ДНК клетками паренхимы и стромы печени [Епифанова]. Полутонкие срезы толщиной 1 мкм покрывали фотоэмульсией — М (разведение 1:3), экспозиция составляла 14 дней. После фиксации и проявки срезы окрашивали 1 % спиртовым раствором толуидинового синего. Гисторадиоавтографическую метку (зерна серебра) подсчитывали под световым микроскопом (глицериновая иммерсия, увеличение 90х10х1,25). Морфометрия проведена с применением оптического анализатора изображения «OLIMPUS BH-2» с использованием программного обеспечения «Видеотест-Морфология» (Свидетельство об официальной регистрации программы для ЭВМ № 990537 от 27 июля 1997 г.) и стандартного пакета статистических программ Excel с учетом числа срезов и количества животных (Г.Г. Автандилов, 1990). Использовали t-критерий Стьюдента. Статистически достоверными считали изменения при Р≤0,05.
Результаты и обсуждение
Предыдущими нашими исследованиями были установлены данные свидетельствующие о развитии тканевой и гемической гипоксии, опосредованной прямыми токсическими эффектами свинца, а также развивающимся оксидативным стрессом, при длительном поступлении в организм малых доз свинца [1]. Функционально-ведущая ткань печени — гепатоциты, в условиях сниженной доставки кислорода и нутриентов, в значительно меньшей степени выказывают способность к реализации регенераторных потенций, зачастую подвергаясь некрозу. Закономерно предположить, что активированные коллагенсинтезирующие непаренхиматозные клетки, участвуя в ремоделировании ЕСМ и компонентов сосудистого русла, примут непосредственное участие в развертывании компенсаторно-приспособительных реакциях носящих защитный и возможно избыточный характер. Современными исследованиями установлено, что острое поражение гепатоцитов активирует фенотипическую транс-дифференцировку неподвижных звездчатых клеток в миофибробластоподобные клетки, способные к пролиферации с последующим синтезом компонентов экстрацеллюлярной стромы, в основном коллагена I и III типа занимающие, таким образом, ключевую роль в развитии фиброза [6] а при экспонировании фенотипа гладких миоцитов содействуя развитию портальной гипертензии [2]. Отсутствующие в нормальной печени миофибробласты появляются в результате активации клеток прекурсоров, к которым относятся, помимо звездчатых клеток, при повреждении пограничной пластинки — свободные портальные фибробласты, а также фибробласты второго слоя клеток окружающих центролобулярные вены, расположенные в Глиссоновой капсуле, перибилиарные, адвентиции междольковой вены и гладкие миоциты медии междольковой артерии, экспрессирующие миофибробластический фенотип, способные к миграции внутрь дольки и вовлекаемые в фиброгенез [4; 7].
При изолированной экспозиции белых мышей ацетатом свинца на 30-е сутки эксперимента, наблюдается усиленный фибриллогенез внутри и вокруг перипортальных очагов некроза выполняющий разграничительные функции. Сужение части просвета синусоидных капилляров и гипертрофия наружной оболочки междольковых сосудов также можно трактовать как проявление защитной реакции, уменьшающей доставку свинца к гепатоцитам. На фоне продолжающегося воздействия экотоксиканта, при наблюдаемых прогридиентных поражениях паренхимы и сосудистого русла, следовало бы ожидать эффективных компенсаторных реакций со стороны соединительнотканного компонента печеночных долек. Однако, в серии Pb60 процессы внутриорганного саногенеза отличаются незавершенностью и крайне слабой выраженностью, особенно в группе защитных тканевых реакций. Не проявляются защитно-разграничительные свойства междольковой соединительной ткани, которая оказывается не в состоянии противодействовать пространственной экспансии некрозов в соседние дольки, так же как и не выявляются в достаточной мере защитные свойства адвентиции сосудов портальных трактов. В то же время умеренно выраженный интерстициальный фиброз, имеющий ту же защитную направленность выражен в сериях Pb60-90 и является скорее проявлением активации коллагенсинтезирующих клеток или миофибробластов, обеспечивающие накопление внеклеточной матрицы, которая наиболее выражена во временных рамках 30 и 90 суток эксперимента и ассоциируется с численным увеличением клеток стромы (Рис. 1).
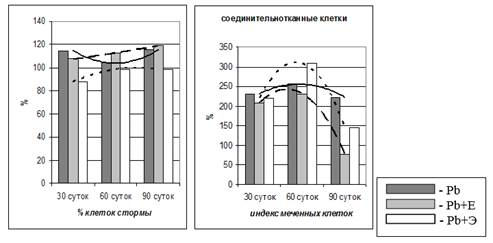
Рисунок 1. Динамические показатели коллагенсинтезирующих клеток стромы печеночной дольки при хронической свинцовой интоксикации и при фармакологическом корригировании (в процентах от контроля)
Численное возрастание клеток, синтезирующих компоненты межклеточного вещества, в серии Pb90 не обеспечивает, в должной мере, осуществление репарации стенок междольковых и вокругдольковых сосудов и волокнообразование внутри и вокруг перипортальных очагов некроза для реализации защитной разграничительной функции (табл.). Убыль паренхиматозных и эндотелиальных клеток закономерно активирует процессы тканевого саногенеза, в том числе, включающие активацию клеток с кислород-зависимым киллингом в зонах тканевой деструкции. На этом фоне капилляризацию синусоидных микрососудов и усиленное коллагенообразование, как в стенке междольковых сосудов, так и между гепатоцитами также можно отнести к тканевой ответной реакции защитной направленности, ограничивающей доступ токсических метаболитов в жизнеспособные гисторегионы. В то же время, появление в составе синусоидных капилляров, на отдельных участках, не характерной для них базальной мембраны и коллагеновых фибрилл в пространстве Диссе, трактуемое как фиброз, симптоматично для капилляро-трофической недостаточности и способствует убыли паренхиматозных клеток с возможным исходом в печеночно-клеточную недостаточность (Рис. 2).
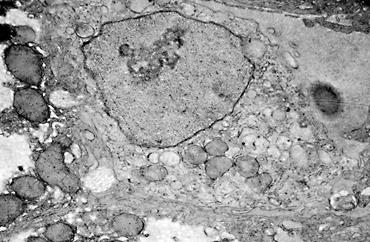
Рисунок 2. Pb 90. Явления усиленного фибриллогенеза с тенденцией к интерстициальному фиброзу. Электронная микрофотография. Ув.: 10000
Проведенное гисторадиоавтографическое исследование позволило обратить внимание на высокую функциональную активность эухроматина, который в 2—2,5 раза активнее, чем в контроле, стабильно, во все сроки эксперимента, включает 3Н-тимидин (табл.). Сопостовление этих данных с качественными и количественными светооптическими и электронномикроскопическими методами дает возможность констатировать нарушение реализации ответной реакции ядерного генома коллагенсинтезирующих непаренхиматозных клеток на тканевом уровне, что свидетельствует о срыве компенсаторно-приспособительных реакций.
Таблица 1.
Количество (%) коллагенсинтезирующих клеток стромы печеночной дольки и индекс включения 3Н-тимидина при изолированном и сочетанном поступлении в организм ацетата свинца, витамина Е и Эрбисола
|
|
|
K |
Pb |
Pb+E |
Pb+Э |
||||
|
|
|
% клеток стромы |
ИМК (‰) |
% клеток стромы |
ИМК (‰) |
% клеток стромы |
ИМК (‰) |
% клеток стромы |
ИМК (‰) |
|
30 сут. |
M m % |
57,22 3,01 |
52,19 13,03 |
65,72 2,16 114,85 |
120,51* 23,69 230,91 |
61,45 3,24 107,39 |
108,21 13,59 207,34 |
50,29 1,17 87,89 |
114,27 17,59 218,95 |
|
60 сут. |
M m % |
57,22 3,01 |
52,19 13,03 |
59,45 1,53 103,89 |
133,54* 22,56 255,87 |
64,51*** 2,02 112,74 |
120,53* 30,09 230,94 |
56,52 3,39 98,77 |
161,15* 20,26 308,77 |
|
90 сут. |
M m % |
57,22 3,01 |
52,19 13,03 |
66,06* 2,96 115,45 |
116,16*** 14,60 222,57 |
68,12* 2,12 119,05 |
40,61 17,84 77,81 |
56,46 1,05 98,67 |
75,85 11,49 145,33 |
Степень выраженности некротических процессов, в условиях сочетанного с ацетатом свинца применения альфа-токоферола, в сравнительном аспекте, ниже, чем в предыдущей серии, а на первый план выступают адаптивные дистрофические и пролиферативные реакции гепатоцитов и эндотелиоцитов, а также компенсаторные процессы стромального компонента печеночных долек, включающие активацию непаренхиматозных клеток. В серии Е30 выражена воспалительная макрофагально-лимфоцитарная инфильтрация, гиперпродукция основного вещества и волоконного компонента, со стороны портального тракта, причем активное участие в ответной реакции принимают гладкие миоциты стенки междольковых сосудов и клетки фибробластического дифферона — высокопластичных тканевых составляющих. Усиленная продукция межклеточного вещества фибробластами портальных трактов отграничивает зоны фокальных некрозов паренхимы, препятствует их распространению и создает благоприятное микроокружение для протекания реакций репарации. Вектор этой защитной реакции фиксируется на формировании локально расширенных соединительнотканных полей всегда с доминированием основного вещества над волоконным компонентом, что не позволяет обозначить эту защитную реакцию как фиброз. Характерной особенностью данной серии является регистрируемый мотогенный эффект с одновременным включением в эухроматин ядра меченного предшественника 3Н-тимидина. Так, фибробласты мигрирующие из Глиссоновой капсулы внутрь долек активно включают тимидин (Рис. 3).
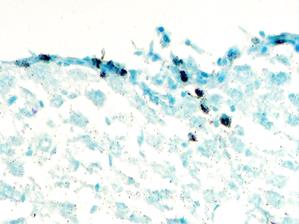
Рисунок 3. Серия Е30. Интенсивное включение метки в клетки, мигрирующие со стороны капсулы. Гисторадиоавтография. Фокусировка на уровне зерен серебра. Парафиновый срез. Докраска толуидиновым синим. Ув. Х 300
В сериях Е-60-90 также отмечена гиперпродукция межклеточного вещества, что свидетельствует об успешной реализации программы ген-белок-признак позволяющий продвинуть адаптивно-компенсаторные реакции с клеточного уровня на тканевую составляющую. Такие ответные реакции со стороны тканевых компонентов печени мышей, как гиперплазия клеточных элементов в стенке междольковых сосудов, усиление продукции ими межклеточного вещества, тем не менее можно отнести к несовершенным, незавершенным компенсаторно-адаптивным эффектам, как и наблюдаемые нами в серии Е30 (Рис. 4).
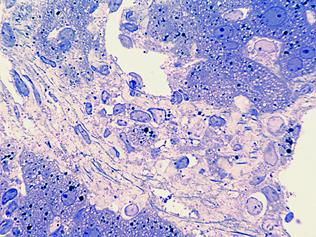
Рисунок 4. Е30. Фрагмент портального тракта. Защитная реакция со стороны портальной соединительной ткани. Высокая секреторная активность клеток фибробластического диферона. Количественное преобладание основного вещества над клеточным и волоконным компонентами. Вновь образованная портальная рыхлая соединительная ткань разграничивает некротические участки двух смежных первых зон ацинуса и содержит некротически измененные гепатоциты и клетки моноцитарного диферона. Полутонкий срез. Толуидиновый синий. Ув.: 400
Активирующее действие альфа-токоферола на секреторную активность соединительнотканных и гладкомышечных клеток в составе оболочек междольковых сосудов, что выявляется в форме усиленного коллагенообразования можно трактовать двояко. С одной стороны, эта защитная реакция отграничивает экспансию токсических метаболитов в центральные участки гепатических ацинусов, с другой несет черты компенсаторной патологии и служит морфологическим базисом возможного прогрессирования процессов фиброза паренхимы, особенно в условиях предполагаемого сочетанного действия нескольких гепатотоксикантов. В целом, учитывая прогридиентные количественные показатели коллагенсинтезирующих непаренхиматозных клеток к 90-м суткам, с одновременным снижением ИМК до значений ниже контроля (табл.), а также стабильно выявляемой гиперпродукцией межклеточного вещества, провомочно сделать вывод о достижении конечной точки их активации — белоксинтетической активности.
Совместное с ацетатом свинца применение эрбисола в более полной мере, чем альфа-токоферол, оказывает нормализующее влияние, в том числе на стромальный компонент. В целом адаптивно-компенсаторные процессы в сериях Э30—60 достигают степени выраженности позволяющие говорить о развертывании саногенетических реакций, которые характеризуются клеточной регенерацией гепатоцитов, ограниченностью фокусов некроза, привлечением иммунноцитов, усилением коллагенсинтетических процессов преимущественно в портальных трактах, успешной регенерацией синусоидных капилляров, выключением эритроцитов из цитотоксических мишеней свинца. ИМК достигает максимальных значений, по сравнению с другими сериями эксперимента, только в серии Э60, причем клетки включающие автограф визуализируются в перипортальном тракте (табл.). В серии Э90 отмечается компенсаторная дилатация сосудов портального тракта с фокусами пролиферации гепатоцитов и коллагенсинтезирующих клеток стромы, а также интерстициальный фиброз в зоне некробиотически измененных гепатоцитов. Некрозы и лейкоцитарные инфильтраты характерные для портального тракта в серии Э90 выказывают тенденцию к замещению соединительнотканными прослойками. Отмечена тенденция к увеличению количества моноцитов и плазмоцитов, в то время как нарастания количества коллагенсинтезирующих клеток не происходит (табл.). Зарегистрированные нами минимальные признаки пролиферации экстравазальных клеток Купфера позволяют говорить об иммуномодулирующих и иммунокорригирующих эффектах длительного применения эрбисола, что, несомненно, позитивно влияет на тканевой морфогенез и тканевую адаптацию. Однако, наличие очагов экстравазальной пролиферации гепатических макрофагов, инфильтрация паренхимы лимфоцитами и плазмоцитами на фоне присутствующих фокальных внутридольковых некрозов и признаков усиленного коллагенообразования в зонах тканевой деструкции (фиброз) рассматривается нами как совокупность патоморфологических признаков, характеризующих хроническое воспаление.
Выводы
1. 30—90-суточная изолированная экспозиция белых мышей ацетатом свинца, сопровождающаяся явлениями некроза и гипоксии паренхимы печеночных долек, является триггерным механизмом для адаптивно-компенсаторных реакций соединительнотканного компонента, реализующихся в процессе клеточной регенерации и активации коллагенсинтезирующих непаренхиматозных клеток, что подтверждается стабильно высокими показателями ИМК и увеличении, в сравнении с контролем, их количества.
2. Адаптивно-компенсаторные реакции в серии с изолированным введением свинца фиксируются на клеточном уровне ввиду способности коллагенсинтезирующих непаренхиматозных клеток отвечать на митогенный стимул, однако на тканевом уровне отличаются слабостью и незавершенностью, что свидетельствует о их срыве.
3. Применение альфа-токоферола совместно с ацетатом свинца стимулирует адаптивно-компенсаторные процессы, сначала, на уровне непаренхиматозных коллагенсинтезирующих клеток регистрируемые нами в виде митогенных и мотогенных эффектов. В дальнейшем, завершение активации миофибробластоподобных клеток, заключающееся в дифференцировке и белоксинтетической активности позволяет реализовать защитные разграничительные реакции на тканевом уровне, при этом нося черты компенсаторной патологии.
4. Применение эрбисола, на фоне введения ацетата свинца, способствует наиболее полной и адекватной реализации компенсаторно-приспособительных процессов со стороны стромальных компонентов печеночных долек, однако, может только отсрочить и минимизировать, а не предотвратить параллельно развертывающиеся дистрофические и деструктивные реакции.
Список литературы:
- Купша Е.И., Бондаренко В.В. Морфологические признаки гипоксий в печени белых мышей при длительном пероральном поступлении малых доз ацетата свинца в организм /Здоровье — основа человеческого потенциала: проблемы и пути их решения: труды IX всероссийской научно-практической конференции с международным участием// Санкт-Петербург. — 2014. — Т. 9, часть 1. — С. 136—141.
- Bosch J, Garcia-Pagan JC. Complications of cirrhosis. I. Portal hypertension. //J Hepatol. — 2000. — № 32. — Р. 141—156.
- 3.Growth Inhibition and Apoptosis in Liver Myofibroblasts Promoted by Hepatocyte Growth Factor Leads to Resolution from Liver Cirrhosis / Wook-Hwan Kim, Kunio Matsumoto[et al.]//American Journal of Pathology. — 2005. — Vol. 166. — № 4. — Р. 1017—1028.
- Hepatic fibrosis and cirrhosis: The (myo)fibroblastic cell subpopulations involved/ Christelle Guyota, Sébastien Lepreuxa.[et al.]// The International Journal of Biochemistry & Cell Biology. — 2006 — Vol. 38. — P. 135—151.
- Hepatic stellate cells: it's role in normal and pathological conditions/Sarem M, Znaidak R [et al.] //Gastroenterol Hepatol. — 2006. — Vol. 29. — № 2. — Р. 93—101.
- Mann D.A. and Smart D.E. Transcriptional regulation of hepatic stellate cell activation.// Gut. — 2002. — № 50. — Р. 891—896.
- Ramadori G. and Bernhard Saile. Portal tract fibrogenesis in the liver // Laboratory Investigation. — 2004. — Vol. 84. — Р. 153—159.
- Tangkijvanich P, Yee HF Jr. Cirrhosis-can we reverse hepatic fibrosis?// Eur J Surg Suppl. — 2002. — Vol. 587. — Р. 100—112.
- The Role of Collagen Structure in Mitogen Stimulation of ERK, Cyclin D1 Expression, and G1-S Progression in Rat Hepatocytes/ John T. Fassett, Diane Tobolt [et al.]//The journal of biological chemistry. — 2006. — Vol. 278. — № 34. — Р. 31691—31700.
- Wu J, Zern M.A: Hepatic stellate cells: a target for the treatment of liver fibrosis // J Gastroenterol. — 2000. — Vol. 35. — Р. 665—672.
дипломов

